
- •Углеводы, их классификация.
- •Функция углеводов.
- •Классификация углеводов
- •Обмен углеводов
- •Гликоген
- •Каскадный механизм мобилизации и синтеза гликогена
- •1 Стадия
- •2 Стадия
- •I Обходной путь (путь синтеза глюкозы из пирувата) Образование фосфоенолпирувата из пирувата в обход пируваткиназы
- •Гликолиз и глюконеогенез.
- •Пентозофосфатный цикл окисления глюкозы.
- •1 Этап – окислительная фаза – осуществляется дегидрогеназно-декарбоксилазной системой.
- •Суммарное уравнение окислительной стадии пфц
- •Биологическое значение пфц
- •Регуляция углеводного обмена.
- •Патология углеводного обмена.
- •Причины понижения и повышения уровня глюкозы в крови.
- •Определение и классификация липидов
- •I физиологическая
- •II физико-химическая
- •Функции липидов
- •2. Сфингофосфолипиды.
- •Функции желчных кислот
- •Всасывание триглицеридов и продуктов их расщепления
- •Внутриклеточный липолиз
- •1 Стадия
- •2 Стадия
- •Энергетический баланс β-окисления (четное число атомов углерода)
- •Окисление жирных кислот с нечетным количеством атомов углерода.
- •Особенности окисления ненасыщенных жиных кислот
- •Синтез жирных кислот
- •1 Стадия Образование малонил-КоА для синтеза жк
- •2 Стадия Синтеза жк на поверхности пальмитатсинтетазы
- •Суммарное уравнение биосинтеза пальмитиновой кислоты.
- •Регуляция обмена липидов
- •Нервно-гормональная регуляция липидного обмена
- •Метаболизм кетоновых тел в норме и патологии
- •Транспортные липопротеины (лп)
- •Липопротеинемии и атеросклероз.
- •Распространение и функции Хс.
- •Синтез Хс.
- •Транспорт Хс.
- •Сложные липиды и миелинизация.
1 Стадия
1.↓ Р-ция фосфорилирования глк, т.е. перенос остатка ортофосфата на глюкозу за счет АТФ. Реакция катализируется ферментом гексокиназой:
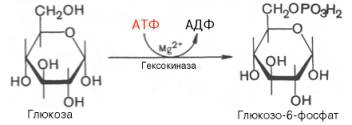
Образование глюкозо-6-фосфата в гексокиназной реакции сопровождается освобождением значительного количества свободной энергии системы и процесс практически необратим. Глк-6-ф в отличии от глк, не проходит через мембрану и как бы «запирается в клетке».
Гексокиназа существует в виде четырех изомеров. Первые три преобразуют различные виды гексоз, включая глк. Гексокиназа IV (глюкокиназа) фосфорилирует только глк, имеется в печени, включается в работу при значительных концентрациях глк в крови воротной вены. Остальные изоформы существуют во всех органах и тканях. Гексокиназа ингибируется глюкозо-6-фосфатом, т.е. последний служит одновременно и продуктом реакции, и аллостерическим ингибитором.
2.↓↑ Изомеризация глюкозо-6-фосфата в фруктозо-6-фосфат:
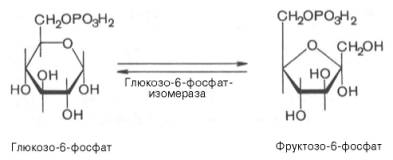
Эта реакция протекает легко в обоих направлениях, и для нее не требуется каких-либо кофакторов.
3.↓ Образовавшийся фруктозо-6-фосфат фосфорилируется за счет второй молекулы АТФ:
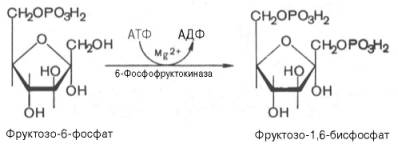
Данная реакция аналогично гексокиназной практически необратима и является наиболее медленно текущей реакцией гликолиза, так как здесь происходит резкое падение свободной энергии.
Фермент фосфофруктокиназа по своей природе аллостерический фермент. Она ингибируется АТФ и стимулируется АМФ. При значительных величинах отношения АТФ/АМФ активность фосфофруктокиназы угнетается и гликолиз замедляется. Напротив, при снижении этого коэффициента интенсивность гликолиза повышается. Во время работы мышцы происходит интенсивное потребление АТФ и активность фосфофруктокиназы повышается, что приводит к усилению процесса гликолиза.
Фосфофруктокиназа – это «ключевой» фермент гликолиза, он лимитирует скорость всего процесса гликолиза.
4.↓↑ Под влиянием фермента альдолаза фруктозо-1,6-дисфосфат расщепляется на две фосфотриозы:
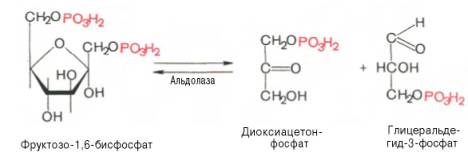
Эта реакция обратима. При повышении температуры реакция сдвигается в сторону большего образования триозофосфатов дигидроксиацетонфосфата (ДАФ) и глицеральдегид-3-фосфата (ГАФ)).
5.↓↑ Реакция изомеризации триозофосфатов.

Равновесие данной реакции сдвинуто в сторону дигидроксиацетонфосфата. Образуется ≈95% дигидроксиацетонфосфата и 5% глицеральдегид-3-фосфата. В последующие реакции гликолиза включается только глицеральдегид-3-фосфат. По мере его потребления в ходе дальнейших превращений дигидроксиацетонфосфат превращается в глицеральдегид-3-фосфат.
2 Стадия
6. ↓↑ Окисление глицеральдегид-3-фосфата в присутствии фермента глицеральдегид-фосфатдегидрогеназы, кофермента НАД и неорганического фосфата (гликолити-ческая оксидоредукция) с образованием 1,3-бисфосфоглицериновой кислоты и восстановленной формы НАД (НАДН2).
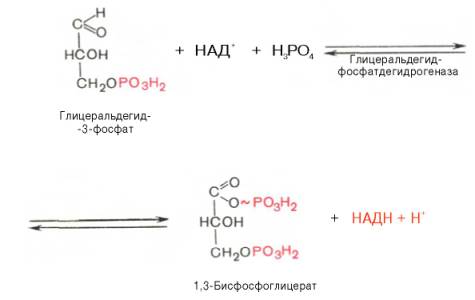
Реакция обратима, продукты реакции блокируют фермент, поэтому необходимо использовать их непрерывно в ходе реакции.
7. ↓↑ Передача богатого энергией фосфатного остатка (фосфатной группы в положении 1) на АДФ с образованием АТФ и 3-фосфоглицериновой кислоты (3-фосфоглицерата):
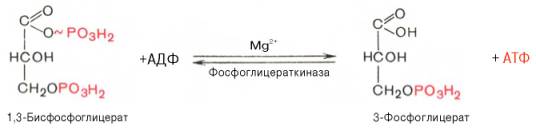
Р-ция экзергоническая, происходит значительное падение свободной энергии, равновесие сдвинуто влево.
Реакция обратима – это первая реакция гликолиза где образуется АТФ. В отличие от окислительного фосфорилирования образование АТФ из высокоэнергетических соединений называется субстратным фосфорилированием.
8. ↓↑ Реакция изомеризации. Сопровождается внутримолекулярным переносом оставшейся фосфатной группы.
Реакция легкообратима, протекает в присутствии ионов Mg2+.

9. ↓↑ Реакция дегидратации. Катализируется ферментом енолазой, при этом 2фосфоглицериновая кислота в результате отщепления молекулы воды переходит в фосфоенолпировиноградную кислоту (фосфоенолпируват). В результате образуется еще 1 макроэргическая связь. Реакция обратима.
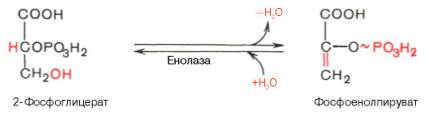
Енолаза активируется двухвалентными катионами Mg2+ или Мn2+ и ингибируется фторидом.
10. ↓ 2-ая реакция гликолитического фосфорилирования. Реакция необратима, т.к. характеризуется резким падением свободной энергии, разрывом высокоэргической связи и переносом фосфатного остатка от фосфоенолпирувата на АДФ (субстратное фосфорилирование). Синтезируется еще одна молекула АТФ.
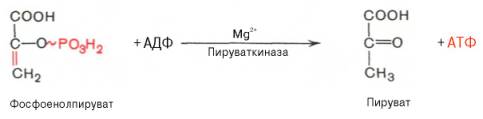
Активируется в присутствии ионов Mg2+, одновалентных катионов щелочных металлов (К+ или др.).
11. Восстановление пировиноградной кислоты до молочной кислоты. Реакция протекает при участии фермента лактатдегидрогеназы и кофермента НАДН2, образовавшегося в шестой реакции:

Продукт реакции лактат является «тупиком» в обмене веществ, т.к. не вступает ни в один биохимический процесс, кроме обратного превращения в ПВК. При накоплении лактата в клетке нарушается ее рН и останавливается гликолиз.
Т.о. Анаэробный гликолиз – это распад глюкозы до ПВК (с 1-ой до 10 р-ции). При потребности в большем количестве энергии происходит дальнейшее окисление ПВК (ее окислительное декарбоксилирование, преобразование в ацетил-КоА и полное окисление в ЦТК.
Энергетический баланс и биологическая функция гликолиза.
Распад АТФ происходит в 1-ой и 3-ей реакциях, на стадии фосфорилирования глк и фрк.
Если учесть, что весь дигидроксиацетон (5-я реакция), превращается в альдегид, то дальше происходят биохимические превращения двух триоз, а значит образование 4-х молекул АТФ в двух стадиях гликолитического фосфорилирования, т.е. образование двух молекул АТФ на одну молекулу глюкозы.
Три фермента – гексокиназа, фосфофруктокиназа, пируваткиназа (три необратимые реакции) лимитируют скорость гликолиза. Кроме того, контроль гликолиза осуществляется также ЛДГ и ее изоферментами. Воздействуя на них можно регулировать эту скорость.
Хотя анаэробный гликолиз дает малый выход энергии (2 молекулы АТФ на 1 мол глк), это единственный процесс в клетках организма, образующий энергию в отсутствии кислорода.
Поэтому в кризисных ситуациях (гипоксия) роль анаэробного гликолиза неоценимо велика, т.к. гликолиз протекает во всех клетках и тканях. В этом биологическая роль гликолиза.
Энергетическая ценность аэробного гликолиза.
При окислении 1 молекулы глюкозы в аэробных условиях (с 1-10 реакции) образуется 2 молекулы АТФ. 10-я реакция заканчивается образованием ПВК. Причем при распаде 1 молекулы глюкозы образуется 2 молекулы ПВК.
В реакциях окислительного декарбоксилирования 2-х ПВК
2 мол. НАД·H2 · 3 ═ 6 мол АТФ
В ЦТК 6 мол. НАД·H2 · 3 ═ 18 мол АТФ
2 мол. ФАД·H2 · 2 ═ 4 мол АТФ
Субстр. Фосфорилир-е = 2 мол АТФ
В гликолизе 2 мол АТФ
32 молекулы АТФ образуется при окислении 1 молекулы глюкозы в аэробных условиях.

Регуляция гликолиза. Эффект Пастера – снижение скорости потребления глюкозы и накопления лактата в присутствии кислорода.
Эффекта Пастера объясняется наличием конкуренции между ферментами аэробного (ПВК ДГ, ПВК карбоксилаза, ферменты цепи окислительного фосфорилирования) и анаэробного (ЛДГ) пути окисления за общий метаболит ПВК и кофермент НАДН2.
Без О2 митохондрии не потребляют ПВК и НАДН2, в результате их концентрация в цитоплазме повышается и они идут на образование лактата. Так как анаэробный гликолиз дает из 1 глюкозы только 2 АТФ, для образования достаточного количества АТФ необходимо много глюкозы (в 19 раз больше чем в аэробных условиях).
В присутствии О2, митохондрии выкачивают ПВК и НАДН2 из цитоплазмы, прерывая реакцию образования лактата. При аэробном окислении из 1 глюкозы образуется 38 АТФ, соответственно для образования достаточного количества АТФ необходимо мало глюкозы (в 19 раз меньше чем в анаэробных условиях).
ТЕМА: УГЛЕВОДЫ III
Цель: Дать представление о основных путях тканевых превращений глюкозы, механизмы регуляции углеводного обмена, патологии, возникающие в результате его нарушения.
ПЛАН ЛЕКЦИИ
1. Глюконеогенез, обходные пути необратимых реакций
2. Пентозофосфатный цикл окисления глюкозы.
3. Регуляция углеводного обмена.
4. Патология углеводного обмена.
Глюконеогенез – это синтез глюкозы из неуглеводных продуктов: молочной и пировиноградной кислоты, так называемых гликогенных аминокислот, глицерина и т.д.
Главное место процесса печень, в меньшей степени почки и слизистая жкт.
Глюконеогенез протекает при длительном голодании. Можно было бы считать, что глюконеогенез это процесс обратный анаэробному гликолизу. Но 3 реакции гликолиза (гексокиназная, фосфофруктокиназная и пируваткиназная) необратимы, путь обратный гликолизу «снизу вверх» невозможен, поэтому в процесс глюконеогенеза на 3 этапах существуют обходные пути необратимых реакций и используются другие ферменты.
