
- •Билет 1: Отличие понятий «вещество» и «материал»
- •Билет 2: Типы сингоний кристаллов
- •Билет 3: Основные структурные типы
- •Билет 4: Примеры полиморфных переходов для сложных веществ
- •Билет 5: Рентгенофазовый анализ, закон Вегарда
- •Билет 6: Дефекты
- •Билет 7: Применение материалов на основе галогенидов
- •Билет 8: Огнеупоротые оксидные материалы
- •Билет 9: Оксидные магнитные материалы, эффект колоссального магнетосопротивления
- •Билет 10: Семейства оксидных высокотемпературных сверхпроводников
- •Билет 11: Основы зонной теории твердых тел. Металлы, полупроводники и изоляторы, зависимость их электрического сопротивления от температуры.
- •Эти предположения нужны для:
- •Билет 12: Эффекты Зеебека и Пельтье, термоэлектрические материалы
- •Билет 13: Собственные и допированные полупроводники, p-n переход
- •Билет 14: Методы роста кристаллов
- •1) Из расплава:
- •3) Кристаллизация из газовой фазы:
- •Билет 15: Квантовые точки
- •Билет 16: Солнечные батареи
- •Билет 17: Применение графита
- •Билет 18: Применение материалов на основе SnO2
- •Билет 19: Применение материалов на основе свинца и его соединений
- •Билет 20. Применение материалов на основе кремния и его соединений
- •Билет 21: Применение фуллерена и углеродных нанотрубок
- •Билет 22: Применение материалов на основе бора и его соединений
- •Билет 23: Методы получения твердофазных материалов
- •Билет 24: Основные этапы получения керамики. Специфика получения нанокерамических материалов
- •Билет 27: Материалы на основе щелочных металлов и их соединений
- •Билет 28: Применение материалов на основе бериллия и его соединений
- •Билет 29: Применение материалов на основе магния и его соединений
- •Билет 30: Применение материалов на основе щелочноземельных металлов и их соединений
- •Билет 31: Сегнетоэлектрики и пьезоэлектрики, фазовые переходы первого и второго рода
- •Билет 32: Титанат бария: структура, получение и применение
- •Билет 33: Применение материалов на основе алюминия и его соединений
- •Билет 34: Применение материалов на основе галлия, индия, таллия и их соединений
- •Билет 35: Применение материалов на основе титана и его соединений
- •Билет 36: Принцип работы топливных элементов
- •Билет 37: Применение материалов на основе ванадия, ниобия, тантала и их соединений
- •Билет 38: Применение материалов на основе хрома, молибдена, вольфрама и их соединений
- •Билет 39: Принцип действия фото- и электрохромных устройств
- •Билет 41: Применение материалов но основе железа и его соединений
- •Билет 42: Применение материалов на основе кобальта и его соединений
- •Билет 43: Применение материалов на основе никеля и его соединений
- •Билет 44: Применение материалов на основе платиновых металлов и их соединений
- •Билет 45: Применение материалов на основе меди, серебра, золота и их соединений
- •Билет 46: Применение материалов на основе марганца, технеция, рения и их соединений. Элементы Лекланше
- •Билет 47: Применение материалов на основе цинка, кадмия, ртути и их соединений
- •Билет 48: Применение материалов на основе редкоземельных элементов и их соединений
- •Билет 49: Применение материалов на основе актиноидов и их соединений
- •Билет 50: Механическое поведение (зависимость деформации от напряжения) различных типов материалов (керамика, металлы, полимеры). Формула Холла-Петча.
Билет 1: Отличие понятий «вещество» и «материал»
Материалы – вещества, из которых делают вещи или то, из чего состоят окружающие человека и используемые им предметы.
Материал – необработанное вещество, сырье, из чего изготавливается, производится что-либо.
Вещество – один из видов материи, элементы которой – атомы, молекулы и т.п. – обладают массой покоя.
Билет 2: Типы сингоний кристаллов
Примеры веществ с подобными структурами: триклинная - дихромат калия, пентагидрат сульфата меди; моноклинная - гипс, винная кислота; орторомбическая - сульфат бария, гептагидрат сульфата магния; гексагональная - кварц, нитрат калия; тетрагональная - оксид олова, вольфрамат кальция, молибдат свинца; кубическая - фторид кальция, хлорид (хлорат) натрия. В кубической сингонии различают простую решётку (полоний), объёмоцентрированную решётку (натрий, ванадий, вольфрам, титан), гранецентрированную решётку (серебро, золото).
Билет 3: Основные структурные типы



(NaCl) (CsCl) (CaF2)
Структура хлорида натрия: кубическая гранецентрированная решётка, число формульных единиц = 4, КЧ(Na)=6 - октаэдрическое окружение, КЧ(Cl)=6 - октаэдрическое окружение. Трехслойная ПШУ, катион в октаэдрических пустотах. R-/R+=2,41. Примеры соединений: FeO, MnO, TiO.
Структура хлорида цезия: кубическая объёмоцентрированная решётка, число формульных единиц = 1, КЧ(Cs)=8 - кубическое окружение, КЧ(Cl)=8 - кубическое окружение. Примитивная кубическая упаковка. Катионы в кубических пустотах. R-/R+=1,37. Примеры соединений: CsI, NH4Cl, TlBr.
Структура фторида кальция: кубическая решётка составленная из двух: катионной гранецентрированной кубической подрешётки и анионной простой кубической подрешётки, число формульных единиц = 4, КЧ(Ca)=8 - кубическое окружение, КЧ(F)=4 - тетраэдрическое окружение. Простая кубическая кладка из F, где Ca занимают половину кубических пустот в шахматном порядке. Примеры соединений: CeO2, ThO2.
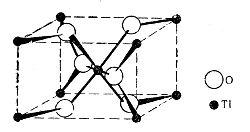


(рутил) (сфалерит) (вюрцит)
Структура рутила: тетрагональная решётка, число формульных единиц = 2, КЧ(Ti)=6 - искажённый октаэдр, КЧ(O)=3 - треугольное окружение. Примеры соединений: SnO2.
Стуктура сфалерита: кубическая решётка, в которой ионы серы серы составляют гранецентрированную кубическую подрешётку, а ионы цинка занимают половину тетраэдричеких пустот в ней, число формульных единиц = 4, КЧ(S)=4 - тетраэдрическое окружение, КЧ(Zn)=4 - тетраэдрическое окружение. t=(Ra+Ro)/√2(Rb+Ro), 0,85<t<1,06 Примеры соединений: CdS, AgI.
Структура вюрцита: гексагональная структура анионов серы, а катионы цинка занимают в ней половину тетраэдрических пустот, число формульных единиц = 6, КЧ(Zn)=4 - тетраэдрическое окружение, КЧ(S)=4 - тетраэдрическое окружение, примеры соединений: SiC, AlN.
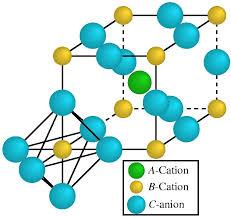
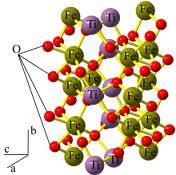
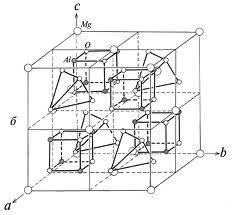
(перовскит) (ильменит) (шпинель)
Структура перовскита: (титаната бария): кубическая подрешётка катионов бария, кубическая подрешётка катионов титана, причём КЧ(Ba)=12 - антикубооктаэдрическое окружение, КЧ(Ti)=6 - октаэдрическое окружение, КЧ(O)=6 - искажённое октаэдрическое окружение, число формульных единиц = 1, примеры соединений: CaZrO3, KMgF3.
Структура ильменита: (титаната железа(II)): тригональная сингония, аналогичен структуре корунда, с поочерёдной заменой двух катионов алюминия (3+) на катионы железа (2+) и титана (4+), а анионы кислорода располагаются в плотнейшей гексагональной упаковке, и, соответственно, катионы располагаются в октаэдрических пустотах подрешётки кислорода, число формульных единиц = 6, КЧ(Fe)=6 - октаэдрическое окружение, КЧ(Ti)=6 - октаэдрическое окружение, КЧ(O)=4 - тетраэдрическое окружение, примеры соединений: MgTiO3, MnTiO3.
Структура шпинели: анионы кислорода расположены в кубической плотнейшей подрешётке, а катионы двухзарядного металла (Mg) занимают тетраэдрические позиции, а катионы трёхзарядного металла (Al) занимают октаэдрические позиции, на примере MgAl2O4: КЧ(Mg)=4 - тетраэдрическое окружение, КЧ(Al)=6 - октаэдрическое окружение, КЧ(O)=4 - тетраэдричское окружение, число формульных единиц = 8. Трёхслойная ПШУ атомов O, ½ октаэдрических пустот занята атомами В, 1/8 тетраэдрических - атомами A. Примеры соединений: Mn3O4.
