- •Часть 1
- •Алкены (этиленовые углеводороды, олефины)
- •Алкины (ацетиленовые углеводороды)
- •Экспериментальная часть Опыт 1. Свойства алканов
- •Опыт 2. Свойства алкенов
- •2.2 Получение этилена и качественные реакции на двойную связь.
- •Опыт 3. Свойства алкинов
- •Опыт 4. Свойства аренов
- •Контрольные вопросы (на них нужно устно или письменно ответить перед лабораторной работой)
-

МИСиС – ШКОЛЬНИКАМ:
ХИМИЧЕСКАЯ ЛАБОРАТОРИЯ
ЛАБОРАТОРНАЯ РАБОТА 1
КАЧЕСТВЕННЫЕ РЕАКЦИИ
ОРГАНИЧЕСКИХ ВЕЩЕСТВ
Часть 1
Качественные реакции углеводородов
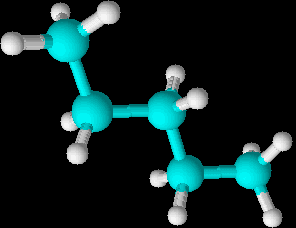
АЛКАНЫ (ПАРАФИНЫ)
Модель молекулы пентана |
Все связи С-С и С-Н в молекулах алканов простые (одинарные).
Все валентности атомов углерода, не занятые на образование связи С-С, направлены на связь с атомами водорода.
Чтобы вступить в химическую реакцию, алкан должен разорвать связь С-С или С-Н, а это сделать непросто (нужно затратить много энергии).
|
Вот поэтому алканы и не реагируют при обычных условиях с такими активными веществами, как серная и азотная кислоты, металлический натрий, перманганат калия.
За это алканы называют «химическими мертвецами», да и другое их название ― парафины ― происходит от латинского «parum affinis», что означает не терпящие сродства.
Алканы вступают в реакции только в жестких условиях, например, при ярком освещении, сильном нагревании, то есть тогда, когда подводится энергия, необходимая для разрыва связи С-С или С-Н, например:

В реакции с бромной водой и перманганатом калия алканы не вступают.
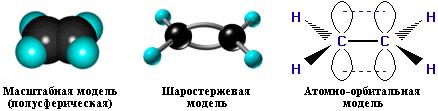
Алкены (этиленовые углеводороды, олефины)
Модель молекулы этилена. Показана двойная связь.
|
Зеленым цветом показано распределение электронной плотности в молекуле этилена.
|
Благодаря присутствию двойной связи алкены гораздо более химически активны, чем алканы. Основные типы химических реакций алканов - это присоединение, окисление и полимеризация.
Алкены легко присоединяют бром; например, пропилен превращается в 1,2-дибромпропан:

Для реакции можно использовать бромную воду – раствор брома в воде. Бромная вода в ходе реакции обесцвечивается.
Кроме того, алкены окисляются перманганатом калия KMnO4, причем
если реакцию проводят в присутствии серной кислоты, то раствор перманганата обесцвечивается. Если реакцию проводить в нейтральной среде, выпадает коричневый осадок MnO2:

Фиолетовая окраска KMnO4 в ходе реакции исчезает.
Органический продукт реакции – двухатомный спирт пропандиол-1,2.
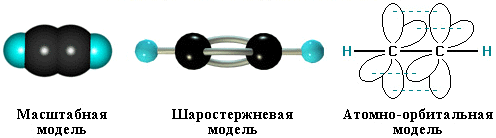
Алкины (ацетиленовые углеводороды)
Модель молекулы ацетилена. Показана тройная связь.
|
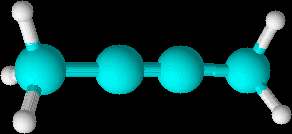
Модель молекулы бутина-2. Обратите внимание на линейную форму молекулы. |
Как и алкены, алкины склонны к реакциям присоединения, окисления и полимеризации. Следовательно, реакции с бромной водой и раствором перманганата калия являются качественными реакциями на алкины.
Отличить ацетиленовый углеводород от этиленового позволяет реакция с аммиачным раствором оксида серебра:

Образующийся ацетиленид серебра дает осадок бледно-желтого цвета.
Прочитайте вопросы, набранные курсивом в экспериментальной части лабораторной работы. Подумайте, на какие из них вы можете ответить до ее выполнения?
При подготовке ответов на вопросы пользуйтесь материалами школьного учебника и электронного учебника по органической химии WWW.CHEMISTRY.SSU.SAMARA.RU