
Органічні речовини
Органічні речовини— сполуки, молекули котрих утворені ланцюгами з ковалентно зв'язаних атомів Карбону.
Макромолекули— відносно великі молекули з високою молекулярною масою. Такі молекули складаються з подібних за структурою низькомолекулярних сполук, які повторюються й ковалентно зв'язані між собою. Утворена мономерами макромолекула називається полімером.
Близько 90 % сухої маси клітин припадає на чотири типи органічних молекул: білки, ліпіди, вуглеводи, нуклеїнові кислоти. Крім того, у менших кількостях у клітинах містяться інші органічні сполуки, що відіграють важливу роль у біохімічних процесах. До них належать органічні кислоти (піровиноградна, молочна, яблучна, лимонна, жирні кислоти — пальмітинова, стеаринова), пігменти (хлорофіл, білірубін) тощо.
Білки, нуклеїнові кислоти та полісахариди (крохмаль, целюлоза, хітин, глікоген) називають біополімерами, або макромолекулами, оскільки вони складаються з великої кількості одиниць — мономерів. Мономерами білків є амінокислоти, мономерами нуклеїнових кислот — нуклеотиди, мономерами полісахаридів — моносахариди. Часто нуклеїнові кислоти називають інформаційними полімерами, оскільки вони е універсальними біологічними носіями інформації.
Види полімерів
Регулярними біополімерами є, наприклад, крохмаль, глікоген, целюлоза. Нерегулярними — білки та нуклеїнові кислоти.
Вуглеводи
Молекули вуглеводів побудовані з трьох елементів — Карбону, Оксигену і Гідрогену. Вуглеводи — основне джерело енергії для живих організмів. Рослини синтезують вуглеводи в процесі фотосинтезу. Вміст вуглеводів у клітинах тварин рідко перевищує 5 %, але в клітинах рослин може досягати 90 %.
Функції вуглеводів.
1. Енергетична. Під час окиснення у процесі клітинного дихання вуглеводи вивільняють енергію, яка в них міститься, забезпечуючи значну частину енергетичних потреб організму.
2. Захисна. В'язкі секрети (слизи), багаті на вуглеводи, оберігають стінки органів (шлунок, кишечник, бронхи) від механічних і хімічних впливів.
3. Рецепторна. Більшість клітинних рецепторів є глікопротетами. Зв'язуючись з інтегральними мембранними білками, вуглеводи у складі рецепторів беруть участь у розпізнаванні сигнальних молекул (гормонів, нейромедіаторів).
4. Структурна. Вуглеводи є основними структурними компонентами клітин, які утворюють опорні тканини (целюлоза, хітин).
5. Запасаюча. Відкладаючись у тканинах, вуглеводи можуть забезпечити організм енергією уразі голодування (крохмаль, глікоген).
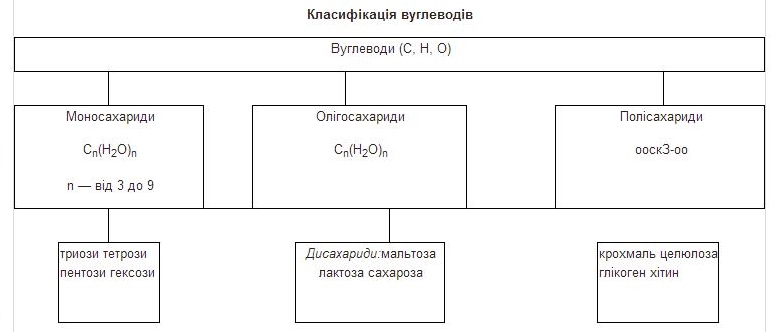
Моносахариди, або прості цукри, — сполуки з емпіричною формулою Cn(H2O)n, які не гідролізуються. Це тверді кристалічні речовини, розчинні у воді, мають солодкий смак. За кількістю атомів Карбону моносахариди поділяються:
на тріозиC3H6O3 — молочна та піровиноградні кислоти, проміжні продукти вуглеводного обміну;
тетрозиC4H8O4 — зустрічаються рідко, частіше в бактерій;
пентозиC5H10O5 — рибоза, входить до складу РНК;
C5H10O4 — дезоксирибоза, входить до складу ДНК;
гексозиC6H12O6 — глюкоза, фруктоза, галактоза.
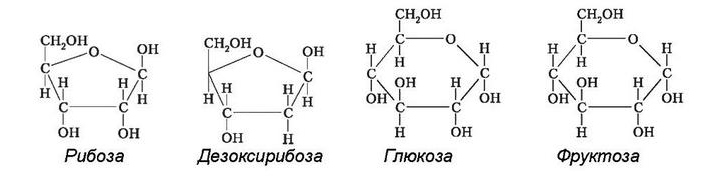
Глюкоза— первинне джерело енергії для клітин. Вона обов'язково міститься у складі майже всіх клітин, органів і тканин, регулює осмотичний тиск. Зниження рівня глюкози в крові спричинює порушення життєдіяльності нервових та м'язових клітин.
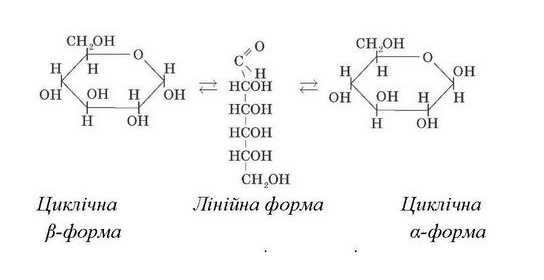
У розчинах глюкоза існує в циклічній та лінійній формах, між якими встановлюється хімічна рівновага.
Лінійна та циклічні форми глюкози
Олігосахариди— це вуглеводи,які мають від двох до десяти ланок моносахаридів. Зв'язок між двома моносахаридами здійснюється через атом Оксигену та називається глікозидним.
Олігосахариди, що складаються з двох моносахаридів, називаються дисахаридами. Вони широко поширені в тваринах і рослинних організмах і зустрічаються у вільному стані (як продукти біосинтезу або часткового гідролізу полісахаридів), а також як структурні компоненти глікозидів і ін. з'єднань.
До дисахаридів належать:
1) лактоза (молочний цукор), що міститься в молоці, утворена залишками глюкози та галактози;
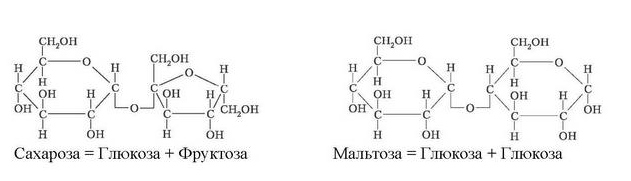
2) сахароза (тростинний цукор C12H22O11), складається з глюкози та фруктози;
3) продукт часткового гідролізу крохмалю в рослинах — мальтоза, що утворена двома залишками глюкози
4) трегалоза – грибний цукор, що так як і мальтоза утворена двома глюкозними залишками.
Полісахариди складаються з великої кількості моносахаридів. Відрізняються між собою складом мономерів, довжиною та ступенем розгалуженості. Полісахариди майже не розчиняються у воді й не мають солодкого смаку.
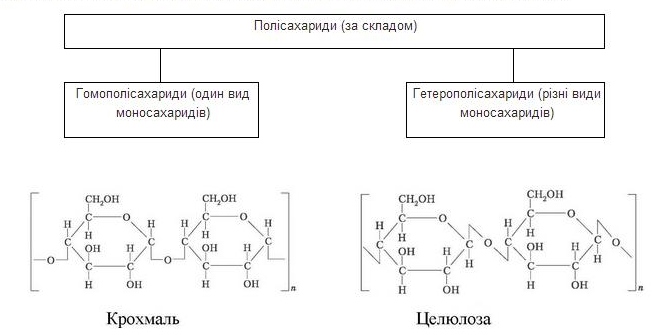
Крохмаль, полімер глюкози, має формулу (C6H10O5)n. Він є резервною поживною речовиною рослин і міститься в клітинах у вигляді різних за формою та розмірами крохмальних зерен. Крохмаль знаходить широке застосування в медицині та в багатьох галузях промисловості (харчовій, паперовій, фармацевтичній тощо). У промислових масштабах його отримують із бульб картоплі та зерен кукурудзи. Картопля містить 15—25 % крохмалю в перерахунку на сиру масу, насіння окремих зернових культур — 40-60 %.
Глікогенє полімером глюкози, але з більш розгалуженим, ніж у крохмалю, ланцюгом мономерів. Це головний енергетичний і вуглеводний резерв людини та тварин. Особливо великий вміст глікогену в печінці і м'язах Зустрічається він у грибів і мікроорганізмів.
Целюлоза— структурний полісахарид клітинної стінки рослин, полімер глюкози. На її частку припадає близько 50 % усього органічного вуглецю біосфери. Целюлоза має величезне значення для господарської діяльності людини, складаючи основну масу бавовняних тканин, паперу, штучного шовку, деяких пластмас і вибухових речовин.
ЛІПІДИ
Ліпіди — органічні сполуки, різні за структурою, хімічною будовою, функціями, але схожі за фізико-хімічними властивостями: нерозчинні у воді, добре розчинні в органічних розчинниках (ефірі, хлороформі, ацетоні).
Функції ліпідів
1. Енергетична. У разі повного окиснення 1 г тріацилгліцеролу виділяється 38,9 кДж енергії, що приблизно вдвічі більше, ніж під час окиснення 1 г білків або вуглеводів.
2. Структурна. Ліпіди є основними структурними компонентами біологічних мембран.
3. Регуляторна. Ліпіди регулюють текучість мембран, є важливими внутрішньоклітинними сигнальними молекулами, компонентами мієлінових оболонок нервових клітин, попередниками гормонів, вітамінами, беруть участь у регуляції генної активності.
4. Запасаюча. Завдяки високій енергетичній цінності жири є енергетичним депо й ендогенним джерелом води (у разі окиснення 100 г жиру виділяється 107 г води).
5. Захисна. Жири є основним компонентом підшкірної клітковини, вони запобігають тепловтратам і захищають від механічних впливів.
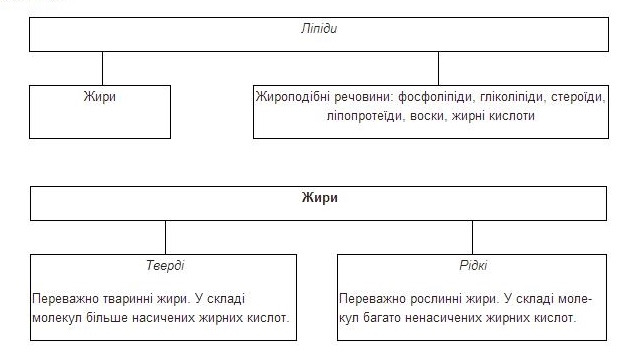
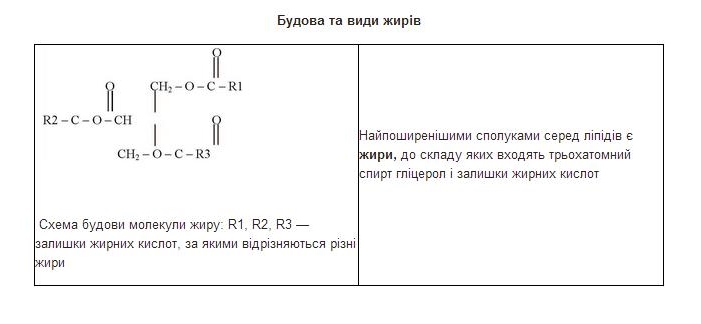
Будова та функції жироподібних речовин
Фосфоліпіди — містять залишок ортофосфатної кислоти, входять до складу клітинних мембран
Гліколіпіди – сполуки ліпідів з вуглеводами. Є складовою частиною тканин мозку та нервових волокон
Ліпопротеїди – комплексні сполуки різноманітних білків із жирами
Стероїди – важливі компоненти статевих гормонів, вітаміну D
Воски – виконують захисну функцію: у ссавців змащують шкіру і волосся, у птахів надають пір'ю водовідштовхувальних властивостей, у рослин запобігають надмірному випаровуванню води
Фосфоліпіди можна розглядати як похідні тріацилгліцеролів, у яких один із залишків жирної кислоти замінений фосфатною кислотою. Жирні кислоти є неполярними гідрофобними сполуками, а фосфатна кислота — полярною гідрофільною. Молекули, у складі яких є полярна та неполярна групи, називають амфіфільними. Амфіфільність дозволяє фосфоліпідам формувати у водному середовищі двошарові мембрани, в яких гідрофільні частини (полярні головки) орієнтовані назовні й контактують із водою, а гідрофобні (неполярні хвости жирних кислот) спрямовані всередину. Така структура служить матриксом усіх відомих біологічних мембран.
БІЛКИ
Білки — це біологічні полімери, мономерами яких є амінокислоти.
Функції білків
1. Ферментативна (біокаталіз) – Ферменти забезпечують перебіг хімічних реакцій у клітині за низьких температур, невисокого тиску і дуже малих концентрацій
2. Будівна (структурна) – Основний будівний матеріал клітини (мембран, органоїдів)
3. Захисна – Білки-антитіла здатні «розрізнювати» і знищувати хвороботворні мікроорганізми. Білки ядра – гістони захищають молекули ДНК від ушкоджень. Білкові фактори згортання крові захищають організм від крововтрат
4. Регуляторна (гуморальна, гормональна) – Поряд із нервовою системою гормони білкової природи керують роботою різних органів і всього організму через систему хімічних реакцій
5. Сигнальна – Окремі білки клітинних мембран здійснюють прийом сигналів і передачу їх всередину клітини
6. Скорочувальна (рухова) – Усі види рухів виробляються особливими видами скорочувальних білків
7. Транспортна –Транспортні білки крові переносять кисень та органічні речовини
8. Енергетична – При окисненні 1 г білка вивільняється 17,2 кДж
9. Рецепторна. Багато білків на поверхні плазматичної мембрани клітин здатні пізнавати молекули певної структури. Білкові рецептори на поверхні клітин імунної системи здатні пізнавати чужорідний антиген і запускати реакцію його знищення.
Структура білків.У звичайній еукаріотичній клітині налічується близько 10 тис. різних білків, а загальна кількість відомих білкових молекул наближається до 50 тис. Усі ці білки складаються не більше ніж з двадцяти видів амінокислот. Амінокислоти є органічними молекулами, що мають загальну схему будови: вони містять карбоксильну групу -COOH й аміногрупу -NН2, зв'язані з атомом Карбону. Індивідуальні властивості кожної амінокислоти визначаються радикалом R. Отже, амінокислоти — структурні мономери білків

Амінокислоти сполучаються між собою ковалентним зв'язком між карбоксильною групою однієї амінокислоти та аміногрупою іншої. Такий зв'язок називається пептидним. Амінокислоти об'єднуються за допомогою пептидних зв'язків у пептиди.
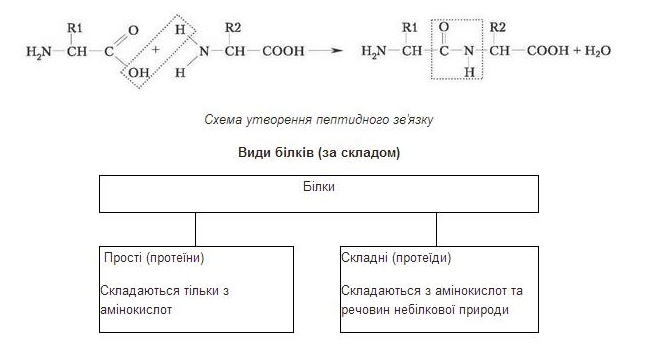
Функціональні властивості білків зумовлені послідовністю амінокислотних залишків і просторовою структурою поліпептидного ланцюга.
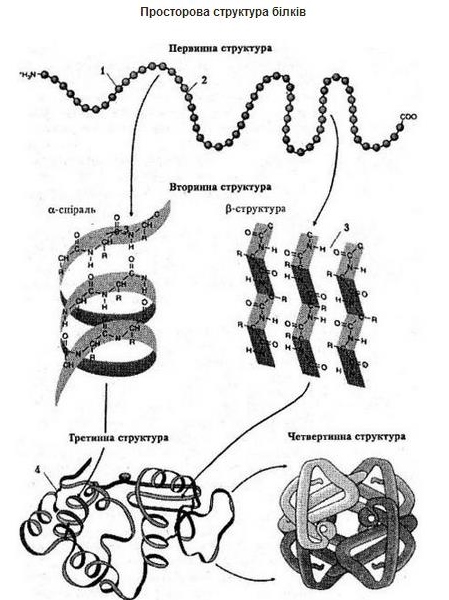
Первинна структура. Визначається порядком чергування амінокислот у пептидному ланцюзі. Амінокислоти з'єднуються міцним пептидним зв'язком.
Вторинна структура. Спірально закручений білковий ланцюжок. Витки спіралі утримуються водневими зв'язками між СО- і NH-групами, розташованими на сусідніх витках.
Третинна структура. Виникає внаслідок закручування вторинної структури в клубок (глобулу). Клубок утримується гідрофобними, йонними та водневими взаємодіями.
Четвертинна структура. Формується кількома глобулами білка. Стійку конфігурацію утворюють гідрофобні, електростатичні та водневі зв'язки.
Ферменти.
Усі ферменти є білками. Кожний фермент каталізує одну або декілька однотипних реакцій, тому зв'язування фермента із субстратом (речовиною, що піддається ферментативному перетворенню) високоспецифічне. Ділянка молекули білка, яка відповідає за зв'язування із субстратом, називається активним центром, а комплекс, що утворився при цьому,— фермент-субстратним комплексом. Суть каталізу полягає у зменшенні ферментом енергії активації (енергії, необхідної для вступу субстрату до реакції). Після завершення реакції комплекс розпадається. У процесі реакції фермент не піддається ані якісним, ані кількісним змінам.
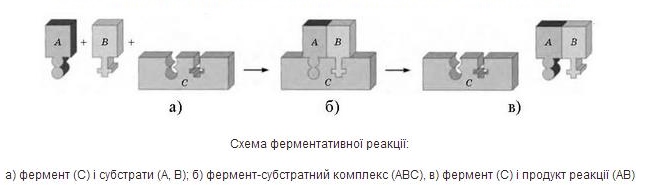
Ферменти мають дуже високу активність, вони здатні послідовно каталізувати тисячі й навіть мільйони реакцій за секунду. При цьому вони функціонують у дуже вузькому інтервалі умов середовища й у разі їхньої зміни інактивуються.
Назви ферментів утворюються віл назви субстрату з додаванням закінчення -аза, наприклад пероксидаза, лактаза
Ферменти широко використовуються в народному господарстві - харчовій, текстильній промисловості, у фармакології.
Ще ширше область використання ферментів в наукових дослідженнях і в медицині.
Порушення природної структури білків
Під впливом різних фізико-хімічних чинників (дія концентрованих кислот і лугів, важких металів, високої температури тощо) структура та властивості білків можуть змінюватися.
Процес порушення природної структури білка або розгортання поліпептидного ланцюга без руйнування пептидних зв'язків називається денатурацією.
Денатурація має необоротний характер. Однак на перших стадіях, за умов припинення дії негативних чинників, білок може відновлювати свій нормальний стан (ренатурація).
Процес руйнування первинної структури білків завжди необоротний, він називається деструкцією.
