
- •1.Белки,строение,биологическая роль
- •2.Аминокислоты,строение,классификация.Биологическая роль.
- •3.Белки,свойства белков(денатурация,нативность,эзоэлектрическая точка,белки-коллоиды).Доменная структура белков.Белки-шапероны.
- •4.Первичная,вторичная структура белков.Связи,участвующие в их образовании.Серповидно-клеточная анемия.
- •5.Третичная , четвертичная структура. Связи,участвующие в их образовании
- •6.Азотистый баланс.Полноценные и неполноценные белки.Биологическая ценность белка.
- •7.Матричный биосинтез белков.Репликация.
- •8.Матричный биосинтез белков.Трансляция.
- •9.Матричный биосинтез белков.Транскрипция.
- •10.Сложные белки.Классификация.Гемопротеины.Строение гемма
- •11. Нуклеиновые кислоты. Строение и биологическая роль
- •18. Гликоген. Синтез гликогена
- •19. Гликолиз,значение процесса для организма,1 этап
- •20 Гликолиз,значение процесса для организма,2этап
- •21. Цикл Кребса. Биологическое значение
- •22 Тканевое дыхание
- •23 Липиды и липоиды.Биологическая роль в организме.Классификация
- •26 Обмен липидов в жкт
- •28. Патологии липидного обмена
- •30.Липопротеины. Строение, классификация. Биологическая роль.
- •31.Биосинтез триглицеридов и фосфолипидов.
- •32. Ферменты. Химическая природа и биологическое значение. Классификация и номенклатура.
- •33.Применение ферментов в медицинской практике.
- •34. Механизм действия ферментов. Изоферменты, мультиферментные системы.
- •35. Переваривание белков в желудочно-кишечном тракте.
- •36. Превращение аминокислот в толстом кишечнике.
- •37. Всасывание продуктов распада белков. Судьба всосавшихся аминокислот.
- •38.Дезаминирование. Биологическое значение. Примеры.
- •39.Обезвреживание аммиака в организме. Орнитиновый цикл образования мочевины.
- •40.Декарбоксилирование. Биогенные амины. Биологическое значение. Примеры.
- •41. Трансаминирование.Биологическое значение.Примеры
- •42. Патологии азотистого обмена(триптофана)
- •44. Патологии азотистого обмена аминокислот с разветвлённой углеродной цепью
- •45. Клеточные мембраны, строение, биологическое значение
- •46.Химический состав клеточных мембран.
- •48. Гормоны,биологическая роль,классификация
- •49. Механизмы действия гормонов
- •50.Гормоны мозгового слоя надпочечников
- •51 Гормоны коркового слоя надпочечников
- •52. Инсулин,глюкагон,строение биологическое действие
- •53. Сахарный диабет.
- •54. Гормоны щитовидной железы
- •55. Гормоны паращитовидной железы
- •56. Гонадотропные гормоны
- •57. Гормоны гипофиза. Актг,ттг
- •58.Гормоны гипофиза. Пролактин,вазопрессин,окситоцин
- •59. Эйкозаноиды: простогландины,тромбоксаны.
- •60. Эйкозаноиды.Лейкотриены.Синтез.Биологическая роль
- •16. Витамины-коферменты.
30.Липопротеины. Строение, классификация. Биологическая роль.
Липопротеины - сложные белки. Их простетическая группа представлена разнообразными липидами. Существует несколько классов липидов. Каждый из них выполняет специфическую биологическую функцию.
Структурная классификация липидов. - Простые. Неполярные: 1.омыляемые; 2.жиры (триаглицерины); 3.воска (эфиры); 4.неомыляемые; 5.стероиды (холестерин). - Сложные. Полярные. Омыляемые: 1.глицерофосфолипиды; 2.сфингофосфолипиды; 3.гликолипиды.
Обязательным структурным компонентом всех классов липидов (кроме холестерина) являются жирные кислоты. Все жирные кислоты - это длинноцепочечные органические кислоты. Содержат одну карбоксильную группу СООН и длинный неполярный гидрофобный хвост. Поэтому липиды нерастворимы в воде. Они бывают насыщенными и ненасыщенными.
Функциональная классификация липидов:1.резервные; 2.структурные; 3.транспортные.
В плазме крови присутствуют свободные липопротеины. Они в отличие от остальных липидов растворимы в воде. Это объясняется строением их комплексов.
Различают 4 класса плазменных липопротеинов:1.хиломикроны; 2.липопротеины очень низкой плотности (ЛПОНП); 3.липопротеины низкой плотности (ЛПНП); 4.липопротеины высокой плотности (ЛПВП).
Классификация липопротеинов зависит от их плотности. Плотность - от содержания в них липидов. Чем больше липидов, тем ниже плотность.
Строение плазменных липопротеинов напоминает мицеллу. Ядро их состоит из неполярных гидрофобных липидов. Наружный слой - из полярных частей молекул фосфолипидов и белков. Такое строение обеспечивает растворимость липопротеинов в плазме.
Биологическая роль ЛП состоит в том, что они выполняют транспортную роль. Они переносят экзогенные, всосавшиеся из кишечника триаглицериды и холестерин к жировым депо и печени. От печени, где синтезируются эндогенные фосфолипиды и холестерин, они транспортируются ко всем внутренним органам, где используются. Поэтому липопротеины плазмы называют транспортными формами липидов. Каждый класс липопротеинов транспортирует ту фракцию липидов, которая в нем преобладает.
31.Биосинтез триглицеридов и фосфолипидов.
Синтез триглицеридов происходит из глицерина и жирных кислот (главным образом стеариновой, пальмитиновой и олеиновой). Путь биосинтеза триглицеридов в тканях протекает через образование глицерол-3-фосфата как промежуточного соединения. В почках, а также в стенке кишечника, где активность фермента глицеролкиназы высока, глицерин фосфорилируется за счет АТФ с образованием глицерол-3-фосфата:





Синтез триглицеридов (триацилглицеролов) в тканях происходит с учетом двух путей образования глицерол-3-фосфата и возможности синтеза триглицеридов в стенке тонкой кишки из β-моноглицеридов, поступающих из полости кишечника в больших количествах после расщепления пищевых жиров.
Синтез наиболее важных фосфоглицеридов локализован главным образом в эндоплазматической сети клетки.
Биосинтез фосфатидилэтаноламина. Первоначально этаноламин при участии соответствующей киназы фосфорилируется с образованием фосфо-этаноламина:

Затем фосфоэтаноламин взаимодействует с ЦТФ, в результате чего образуются цитидиндифосфатэтаноламин (ЦДФ-этаноламин) и пирофос-фат (PPi):
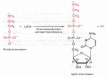
В следующей реакции ЦДФ-этаноламин, взаимодействуя с 1,2-дигли-церидом, образующимся при дефосфорилировании фосфатидной кислоты, превращается в фосфатидилэтаноламин. Реакция катализируется ферментом этаноламинфосфотрансферазой:
ЦДФ-этаноламин + 1,2-диглицерид –> Фосфатидилэтаноламин + ЦМФ.
Биосинтез фосфатидилхолина (лецитина). Фосфатидилэтаноламин является предшественником фосфатидилхолина. В результате последовательного переноса трех метальных групп от трех молекул S-аденозилметионина к аминогруппе остатка этаноламина образуется фосфатидилхолин:

Биосинтез фосфатидилсерина. У млекопитающих фосфатидилсерин образуется в реакции обмена этаноламина на серин следующим путем:
Фосфатидилэтаноламин
+ L-серин
 Фосфатидилсерин + Этанолмин.
Фосфатидилсерин + Этанолмин.
Существует и второй путь образования фосфатидилсерина, который связан с предварительным вовлечением фосфатидной кислоты в синтез фосфоглицеридов:

Затем происходит перенос серина на фосфатидильный остаток с образованием фосфатидилсерина:
ЦДФ-диглицерид + L-серин –> Фосфатидилсерин + ЦМФ.
Таким же путем образуется фосфатидилинозитол.
