
- •Лекция №11 Биотехнология бродильных производств – 6 ч.
- •1) Общая характеристика спиртового брожения. Физиолого-биохимические основы брожения.
- •2) Общая морфофизиологическая характеристика дрожжей, используемых в промышленности.
- •3) Получение этилового спирта.
- •4) Общая характеристика пропионовокислого брожения. Общая морфофизиологическая характеристика микроорганизмов, используемых в промышленности.
- •5) Применение пропионовокислых бактерий.
- •6) Ацетонобутиловое брожение: биохимизм процесса брожения.
- •7) Среды и культуры бактерий, используемых в производстве ацетона и бутанола. Общая технологическая схема ацетонобутилового брожения.
Лекция №11 Биотехнология бродильных производств – 6 ч.
План лекции:
Общая характеристика спиртового брожения. Физиолого-биохимические основы брожения.
Общая морфофизиологическая характеристика дрожжей, используемых в промышленности.
Получение этилового спирта.
Общая характеристика пропионовокислого брожения. Общая морфофизиологическая характеристика микроорганизмов, используемых в промышленности.
Применение пропионовокислых бактерий.
Ацетонобутиловое брожение: биохимизм процесса брожения.
Среды и культуры бактерий, используемых в производстве ацетона и бутанола. Общая технологическая схема ацетонобутилового брожения.
1) Общая характеристика спиртового брожения. Физиолого-биохимические основы брожения.
Спиртовое брожение играет большую роль в жизни человека. Дрожжи традиционно используют в хлебопечении, для получения спирта и многих других продуктов. По значимости для народного хозяйства с ними могут конкурировать только молочнокислые бактерии. Пожалуй, нет на земном шаре ни одного человека, который бы в своей повседневной жизни не пользовался “трудами” этих микроорганизмов.
На Востоке в качестве продуцента спиртового, брожения при производстве рисового пива (сакэ) применяется Aspergillus oryza. Спиртовое брожение могут вызывать также некоторые бактерии (Zymomonas mobilis, Z. anaerobica, Sarcina ventricula, Erwinia amylovora). Однако получение спирта с помощью этих микроорганизмов промышленного значения пока не имеет.
Термином “дрожжи” обозначают одноклеточные эукариотные микроорганизмы, которые в зависимости от наличия и типа полового процесса относят к трем классам грибов: Ascomycetes, Basidiomycetes и Deuteromycetes. Термин “дрожжи” в строгом смысле не имеет таксономического значения.
К классу Ascomycetes относят дрожжи, образующие при половом размножении сумки (аски) с эндогенными спорами. К нему принадлежат представители родов дрожжей, используемых в бродильных производствах, — Saccharomyces и Shizosaccharomyces.
В процессе эволюции дрожжи хорошо приспособились к обитанию в различных местах, содержащих чаще всего углеводы. Они растут на поверхности сладких плодов, в нектаре цветков, в сокотечениях деревьев, на поверхности листьев, в лесной подстилке и почве. Встречаются дрожжи и в водоемах. Содержатся они в пищеварительном тракте человека и животных. Большинство дрожжей сапрофиты, но среди видов, находящихся во внутренних органах и на кожных покровах человека, имеются патогенные или условно патогенные формы, например возбудитель кандидомикозов — Candida albicans. Некоторые дрожжи вызывают болезни растений.
Физиология дрожжей и биохимические основы спиртового брожения.
Из соединений углерода дрожжи, как правило, лучше всего используют гексозы. Некоторые виды хорошо растут на средах с пентозами. Из полисахаридов чаще всего утилизируют инулин и крахмал. Известны дрожжи, растущие на средах с углеводородами и некоторыми спиртами, в том числе метанолом и этанолом, а также органическими кислотами и другими углеродными субстратами.
В качестве источника азота дрожжи используют обычно соли аммония, аминокислоты, небольшие пептиды, реже нитраты и нитриты. Некоторые виды нуждаются в одном или более витаминах (чаще в биотине и тиамине), другие — способны все необходимые для роста витамины синтезировать сами.
Большинство дрожжей растет в границах рН от 3,0 до 8,0, оптимальные значения рН от 3,5 до 6,5. Общий диапазон температур для роста дрожжей довольно широк: от 0 (даже —7°С) до 480-50 0С. Оптимальная температура для роста большинства видов 28—30 °С, но некоторые расы дрожжей, например, используемые в пивоварении, имеют более низкий температурный оптимум. Известны также облигатно психрофильные дрожжи, не растущие при температуре выше 18—20 °С. Многие дрожжи — факультативные анаэробы. В условиях анаэробиоза они получают энергию в результате сбраживания углеводов, а в присутствии молекулярного кислорода — за счет аэробного дыхания.
Спиртовое брожение у дрожжей до образования пировиноградной кислоты отличается от гликолиза у высших организмов лишь последними этапами, на которых вместо молочной кислоты образуется этиловый спирт. Обусловлено это наличием у дрожжей пируватдекарбоксилазы, катализирующей превращение пирувата в ацетальдегид, который затем восстанавливается в этанол.
Гликолитическим путем (или путем Эмбдена — Мейергофа — Парнаса) его также называют фруктозобисфосфатным (ФБФ-путь), осуществляется разложение глюкозы, галактозы, фруктозы и маннозы. Олигосахариды вначале гидролизуются соответствующими ферментами до гексоз.
Существовало мнение, что дрожжи используют пентозы лишь в аэробных условиях. В последнее время установлено, что некоторые из них способны к росту в анаэробных условиях на средах, содержащих ксилозу или ксилулозу; последние подвергаются брожению с образованием этанола. Это имеет важное практическое значение для производств, перерабатывающих в спирт древесину и отходы сельскохозяйственных растений.
Разложение пентоз и высших спиртов осуществляется дрожжами через пентозофосфатный и ФБФ-пути. Спирты вначале дегидрируются до соответствующих гексоз и пентоз.
Брожение предполагает строгое равновесие процессов окисления и восстановления. Поэтому НАД, восстановленный на одном из этапов брожения, должен окисляться на другом этапе. Окисление НАДН происходит одновременно с восстановлением ацетальдегида в этанол. Такой процесс
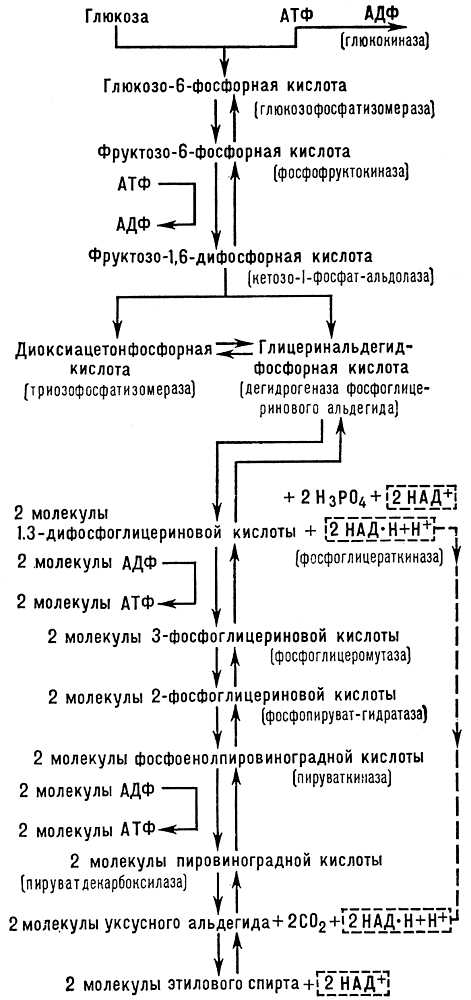
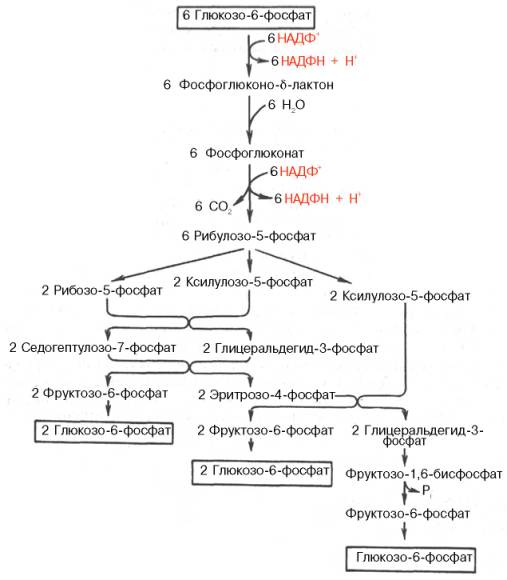
Схема спиртового брожения Пентозофосфатный путь
Нейберг назвал первой формой брожения. Суммарная реакция его:
Глюкоза2СО2 + 2 этанол
Ход брожения может заметно меняться в зависимости от конкретных условий. Если в культуру бродящих дрожжей добавить бисульфит натрия, который связывает ацетальдегид, он исключается из последующего процесса и блокируется:
Ацетальдегид+Na2S2O3 Ацетальдегид (связанный)
В таких условиях акцептором электронов (водорода) от НАДН становится дигидроксиацетонфосфат, превращающийся в глицерин-3-фосфат, а затем в глицерин (вторая форма брожения по Нейбергу). Суммарная реакция соответствует уравнению:
Глюкозаглицерин + ацетальдегид (связанный) + СО2
Суммарное количество синтезированной АТФ при такой форме брожения равно нулю и, следовательно, процесс не может обеспечить рост 'клеток, но его используют в промышленности для получения глицерина.
Сходный вариант спиртового брожения наблюдается при выращивании дрожжей в щелочной среде. В этих условиях ацетальдегид окисляется НАД- зависимой дегидрогеназой в уксусную кислоту. Образовавшийся на этой стадии НАДН используется для восстановления эквивалентного количества ацетальдегида в этанол. Одновременно НАДН, получающийся при окислении 3-фосфоглицеринового альдегида, используется для восстановления дигидроксиацетонфосфата в глицерин-3-фосфат, который затем превращается в глицерин (третья форма брожения по Нейбергу). Суммарная реакция выражается уравнением
2 глюкоза + Н2О 2 глицерин + этанол + уксусная кислота + 2С02
Такой химизм процесса благоприятен для клеток, поскольку образующаяся уксусная кислота снижает рН среды, после чего вновь возобновляется нормальное спиртовое брожение.
В начальной стадии спиртового брожения дигидроксиацетонфосфат также выполняет роль акцептора электронов до момента, пока не накопится ацетальдегид, необходимый для окисления НАДН. Этим объясняется наличие в начале брожения своеобразного периода индукции, во время которого появляется глицерин. Одновременно 3-фосфоглицериновый альдегид превращается, согласно реакциям ФБФ-пути, в пировиноградную кислоту, последняя затем декарбоксилируется в ацетальдегид. Но ацетальдегид не может восстанавливаться в спирт, так как НАДН использован для образования глицерина из дигидроксиацетонфосфата. Поэтому при образовании в процессе брожения одной молекулы глицерина накапливается одна молекула пировиноградной кислоты или ацетальдегида, которая не превращается в этиловый спирт. Спиртовое и глицеринпировиноградное брожение тесно связаны. Вначале преобладает глицеринопировиноградное брожение, но даже в период бурного брожения наряду со спиртом обнаруживаются другие продукты.
В присутствии молекулярного кислорода дрожжи быстро переключаются с брожения на аэробное дыхание. При этом пировиноградная кислота, образующаяся из глюкозы и других субстратов, окисляется через цикл трикарбоновых кислот (ЦТК) до СО2 и Н2О. Кроме того, ЦТК обеспечивает клетки рядом метаболитов, необходимых для дальнейших биосинтетических реакций. В энергетическом отношении дыхание более выгодно, чем брожение. Поэтому в аэробных условиях дрожжи растут лучше и образуют большую биомассу. При выращивании дрожжей в аэробных условиях на средах с этанолом или ацетатом помимо ЦТК важное значение имеет функционирование у них глиоксилатного шунта.
Подавление брожения в аэробных условиях носит название эффекта Пастера. Он связан, видимо, с различием энергетического заряда клеток в аэробных и анаэробных условиях. Дыхательная система и субстратное фосфорилирование конкурируют за АДФ. Кроме того, значение имеет аллостерическая регуляция фосфофруктокиназы. Фермент ингибируется АТФ и активируется АМФ. В анаэробных условиях содержание АТФ низкое, а активность фермента высока, в аэробных — отношение АТФ : АМФ повышается и активность фосфофруктокиназы снижается. Известно также, что аллостерическим ингибитором фосфофруктокиназы является цитрат — промежуточный продукт ЦТК.
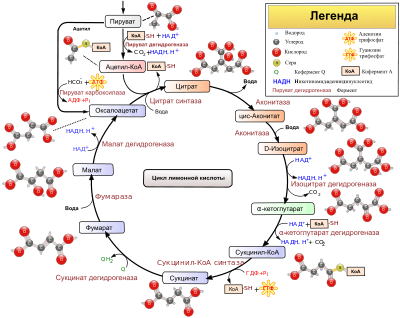
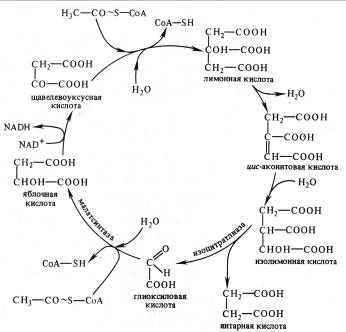
Цикл трикарбоновых кислот Глиоксилатный цикл
Спиртовое брожение может происходить в условиях значительной аэрации при высоком содержании глюкозы в среде (1,5—2,0%). Подавление аэробного дыхания при высокой концентрации глюкозы (высокой скорости ее усвоения) называется эффектом Крэбтри или катаболитной репрессией. Этот эффект не наблюдается при выращивании дрожжей на средах, содержащих менее усваиваемые сахара. Катаболитная репрессия аэробного дыхания не только снижает получение дрожжами энергии, но подавляет биосинтез промежуточных продуктов ЦТК и глиоксилатного цикла. В таких условиях необходимые для биосинтеза кислоты ЦТК образуются путем карбоксилирования пирувата:
Пируват + АТФ + С02 + Н2О пируваткарбоксилаза Оксалоацетат + АДФ + фн
Выше уже указывалось, что в начале спиртового брожения преобладает глицеринопировиноградное брожение, приводящее к образованию глицерина и пировиноградной кислоты. Однако пировиноградная кислота обнаруживается, как правило, в небольших количествах, поскольку основная ее часть идет на образование различных вторичных продуктов. К ним относятся уксусная, молочная, янтарная, пропионовая, муравьиная и некоторые другие кислоты, ацетон, диацетил, ацетоин, 2,3-бутандиол, различные альдегиды и сложные эфиры.
При сбраживании дрожжами сахаров обычно накапливается небольшое количество D(—)-молочной кислоты. Исключением является Sacch. veronae, синтезирующий L (+)-молочную кислоту. К продуктам брожения, образующимся из пировиноградной кислоты в небольшом количестве, относятся также лимонно-яблочная и диметилглицериновая кислота.
Кроме вторичных продуктов при спиртовом брожении образуются побочные продукты — высшие спирты, известные под названием сивушных масел. Почти половину общего количества высших спиртов составляют два изоамиловых спирта: 3-метил-бутанол-(1) и 2-метилбутанол-(1). Наряду с ними в сивушном масле содержатся изобутиленовый, н-бутиловый, н-пропиловый и ароматические спирты (р-фенилэтиловый, р-оксифенилэтиловый). Эти продукты синтезируются из соответствующих кетокислот, образующихся в результате метаболизма углеводов, или из аминокислот. Поэтому вторичные и побочные продукты нельзя строго разграничить. Они существенно влияют на вкус и аромат готового продукта; накопление их не коррелирует с образованием - этанола и сброженные растворы, содержащие одинаковое количество спирта, могут отличаться по вкусовым и ароматическим качествам.
Образование высших спиртов включает дезаминирование аминокислоты в кетокислоту, которая декарбоксилируется в альдегид; последний восстанавливается в спирт:
Однако не все высшие спирты синтезируются из аминокислот. Второй путь их образования можно рассматривать как биосинтез из продуктов метаболизма углеводов. Так, при конденсации пировиноградной кислоты с уксусным альдегидом или с ацетил-КоА образуется ацетомолочная кислота, которая превращается в 2-кетоизовалериановую кислоту. В результате декарбоксилирования этой кислоты получается изомасляный альдегид, восстанавливающийся в изобутанол.
Полагают, что некоторые высшие спирты могут синтезироваться обоими путями (из аминокислот и углеводов), другие— только из продуктов метаболизма углеводов.
При спиртовом брожении образуются также серусодержащие вещества — сероводород и сульфиты. Последние могут быть в форме ионов бисульфит HSO-3 или сернистой кислоты (H2SO3). Синтез этих веществ связан со способностью дрожжей восстанавливать SO42- в S2- через сульфит (SО2-3). Восстановление сульфатов в сульфиты зависит от свойств штамма дрожжей. На образование H2S влияет интенсивность брожения, а также присутствие ионов меди и цинка.
Из других серусодержащих веществ в незначительном количестве могут образовываться меркаптаны (этилмеркаптаны, метилмеркаптаны) —летучие вещества с неприятным запахом. Выделение СО2 при брожении способствует удалению этих веществ из среды.
