
- •Қан биохимиясы
- •Қаннның қызметі
- •Қан плазмасының химиялық құрамы және негізгі биохимиялық тұрақтылары. Қан плазмасының протеиндері.
- •Қан плазмасы протеиндерінің қызметі:
- •Альбуминдер
- •Глобулиндер
- •Қан плазмасының фермент-протеиндері
- •Қан плазмасының протеин емес органикалық заттары. Қанның азотсыз органикалық және бейорганикалық заттары.
- •Плазманың бейорганикалық компоненттері
- •Плазманың қышқылдық-сілтілік балансы
- •Плазманың буферлік жүйесі
- •Қанның негізгі протеолиттік жүйелері
- •Қанның ұю жүйесі және фибринолиз
- •Ұюдың сыртқы механизмінің бастапқы стадиялары
- •Ұюдың ішкі механизмдерінің бастапқы стадиялары
- •Ұюға қарсы жүйе немесе антикоагулянттар
- •Қаннның формалық элементтерінің биохимиясы
- •Гемоглобиннің қалыпты туындылары
- •Бор эффектісі
- •Гемоглобиннің патологиялық түрлері
- •Эритроциттердің тотығу стрессінен қорғалуы
- •Эритроциттердің гемолизі
- •Темір алмасуы
- •Медициналық маңызы
- •Иммуноглобулиндердің супержиыны. Қосымша 1.
- •Комплемент жүйесі, қызметі. Қосымша 2.
- •Калликреин – кинин жүйесі. Қосымша3.
- •Гемоглобиннің синтезі
Эритроциттердің тотығу стрессінен қорғалуы
Оттектің улы формалары және антиоксиданттық қорғаныс жүйесі.
О2 –ден тұрақты түрде, аз мөлшерде, оттектің активтелген формасы (ОАФ) деп аталатын улы заттар туындайды. Бұл қосылыстар күшті тотықтырғыш немесе өте реакцияласуға қабілетті бос радикал болып табылады. Олар жасуша құрылымын және қызметші молекулаларды бұзады.
Оттек молекуласы (О2) құрамында екі жұптаспаған электрон болады және осылай болғандықтан ол бирадикал болып табылады. Бірақ, О2 молекуласындағы жұптаспаған электрондар оның салыстырмалы түрде тұрақты болуына кедергі келтірмейді. Сонда да, егер молекула қосымша түрде электронды қосатын болса (стадия а), онда жоғары реакцияласуға қабілетті супероксид-радикал (•О2-) түзіледі. Келесі стадия, тотықсыздану, (стадия б) пероксид-анион (•О22-) түзілуіне әкеледі. Ол протонды оңай байланыстырады және соның нәтижесінде сутек асқын тотығы (Н2О2) түзілуіне әкеледі. Үшінші электронның байланысуы (стадия в) молекуланы О2- және О- иондарына ыдыратады. Бұл кезде О2- екі протонды байланыстыру жолымен су түзіуіне әкеледі. Төртінші электронның байланысуы және О- -тің протондалуы гидроксил-радикалдың (•ОН) түзілуімен аяқталады.
ОАФ-зақымдалуға негізінен эритроциттер түседі, олар оттекті тасымалдау қызметін атқаратын болғандықтан, өздерінде оттектің жоғары концентрациясы болуымен сипатталады. Эритроциттердегі оттектің активті формасының тұрақты шығу көзі гемоглобиннің ферментсіз тотығуы: Hb(Fe2+)+O2 MeтHЬ(Fe3+) + 02- .
ОАФ эритроциттердің гемолизін дамытуы мүмкін. Эритроциттер құрамында оттек радикалдарының улы әсерін болдырмайтын және эритроциттер мембранасын ыдыраудан сақтайтын ферменттік жүйе болады.
ОАФ әсерінен және басқа да радикалдардан қорғану үшін барлық жасушалардың құрамында тотғуға қарсы тұратын заттар - антиоксиданттар болады.
Антиоксиданттар - тотықсыздандырғыштар, олар тотықтырғыш заттармен оңай реакцияласады және соның нәтижесінде маңызды молекулаларды тотығудан сақтайды. Биологиялық антиоксидантқа С және Ε витаминдері, кофермент Q және кейбір каротиноидтар жатқызылады. Гемнің ыдырауы кезінде түзілетін билирубин де тотығудан қорғайтын қызметті атқарады.
Глутатион (трипептид Glu-Cys-Gly) аса маңызды, ол барлық жасушада жоғары концентрацияда болады. Оның тотықсыздандырғышы цистеин қалдығындағы тиолдық топ. Тотықсызданған формасының екі молекуласы (GSH) тотығу кезінде дисульфидті (GSSG) түзеді.
Эритроциттер де ОАФ-ті инактивтейтін және олардың зақымдалуын қалпына келтіретін жүйе (супероксиддисмутаза, каталаза, GSH) болады.
Ол үшін эритроциттерде қалыпты зат алмасуды қамтамассыз ететін заттар қажет. Сол себепті болуы мүмкін, эритроциттерде метаболизм тек гликолизбен және пентозофосфаттық жолмен шектелген болады.
Гликолиз кезінде түзілетін АТФ бәрінен бұрын Na+/ К+-АТФ-азаның субстраты қызметін атқарады, ол эритроциттердің мембраналық потенциалын ұстайды. Пентозофосфаттық жолда НАДФН+Н+ түзіледі, ол глутатионредуктаза әсерімен глутатиондисульфидтен (GSSG) глутатион (GSH)-тің регенерацияланып қалыптасуына қажетті Н+ -ті береді. Қалыптастырылған (тотықсызданған) глутатион — эритроциттердің ең маңызды антиоксиданты, ол метгемоглобинді қызметті активті гемоглобинге қалыптастыруда кофермент қызметін атқарады. Маңызды қорғаныстық ферментке селенқұрамды глутатионпероксидаза да жатқызылады. (Сур.3.)
Қалыптасқан (тотықсыздаған) глутатион көмегімен Н2О2 детоксикациясы да, сонымен бірге, эритроциттердің мембранасындағы қанықпаған май қышқылдарының АОФ-пен реакциясы кезінде пайда болатын гидропероксидтердің де детоксикациясы атқарылады.
Глюкозо-6-фосфатдегидрогеназа жұмысының генетикалық ақауында және кейбір күшті тотықтырғыш болатын дәрілік заттарды қабылдағанда глутатиондық қорғаныс потенциалы жеткіліксіз болуы мүмкін.
Бұл, жасушаларда гемоглобин молекуласындағы SH-тобының тотығуын жүргізетін оттектің активті формасы мөлшерінің жоғарлауына әкеледі. Гемоглобин мен метгемоглобин протомерлері арасында дисульфидтік байланыс түзілуі олардың агрегаттануына – Хайнц денешіктерінің түзілуіне әкеледі. Бұл денешіктер эритроциттерді ұсақ капиллярларға түскенде ыдырауын жүргізеді (Сурет 4).
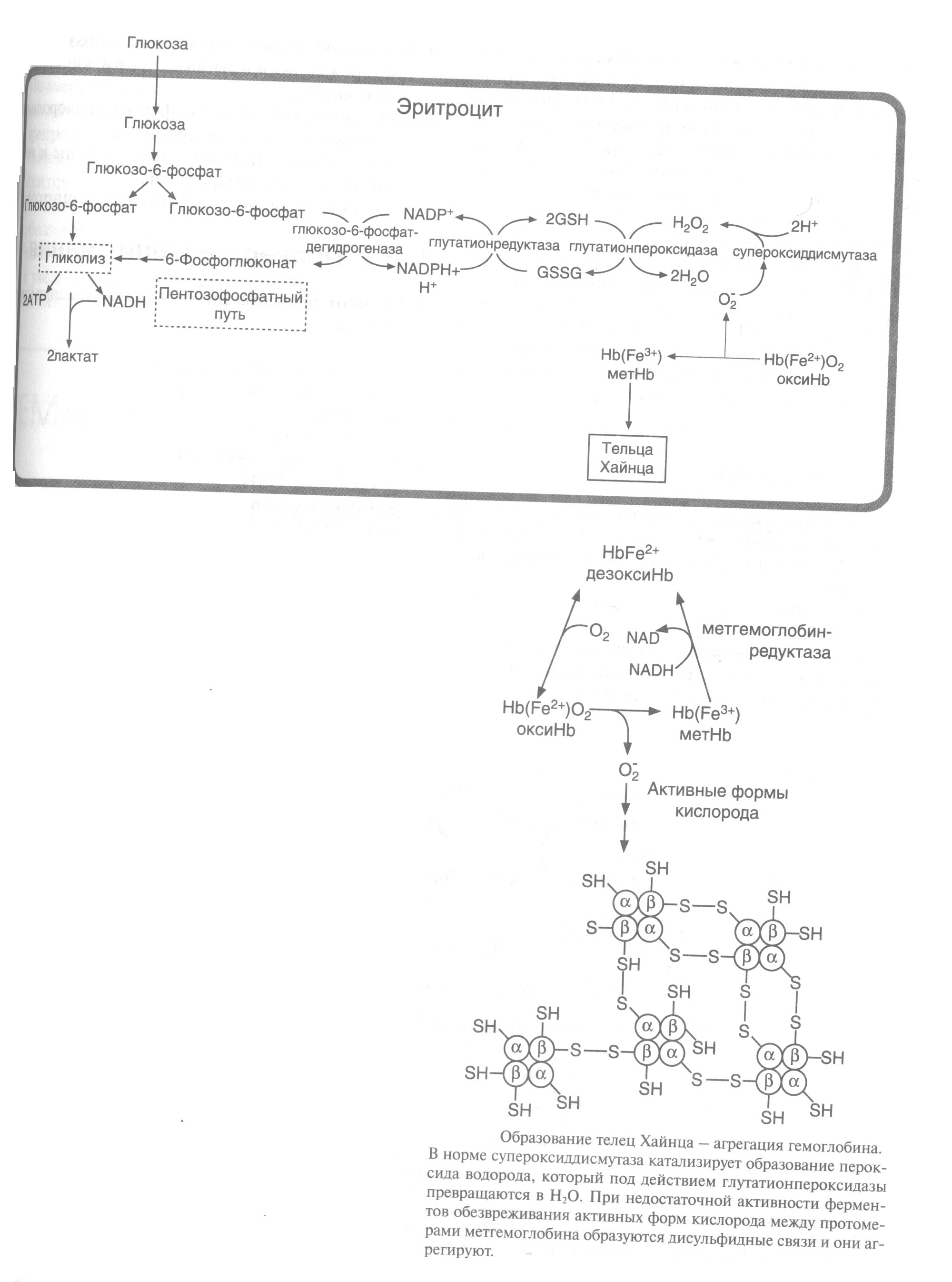
Сурет 2. Хайнц денешіктері түзілуінің механизмі
