
- •2 Экспериментальная часть
- •2.1 Исходные вещества, методики эксперимента, исследований и анализа
- •2.1.2 Методики анализа
- •2.2 Исследование экстракция кадмия нбэа-2 из сульфатных растворов
- •2.2.1 Изучение влияния времени контактирования фаз на экстракцию кадмия
- •2.2.2 Влияние рН водной фазы на экстракцию кадмия
- •2.3 Определение состава экстрагируемого комплекса
- •2.4 Изучение процесса реэкстракции кадмия
2.2 Исследование экстракция кадмия нбэа-2 из сульфатных растворов
2.2.1 Изучение влияния времени контактирования фаз на экстракцию кадмия
С целью установления условий равновесия экстракции кадмия была изучена зависимость распределения металла между фазами от продолжительности процесса.
Экстракцию проводили в течение 5 - 60 минут. В качестве экстрагента был использован 0,062 М НБЭА-2 в смешанном растворе керосина и 25 % октанола. Экстракцию проводили при комнатной температуре и соотношении объемов фаз Vo : Vв = 1 : 1. Полученные результаты представлены в табл. 6. и рис. 13
Таблица 6
Зависимость экстракции кадмия от времени контактирования фаз
№ |
τ, мин |
ХCd, г/л |
YCd, г/л |
DCd |
1 |
5 |
0,005 |
0,795 |
159 |
2 |
10 |
0,005 |
0,795 |
159 |
3 |
15 |
0,005 |
0,795 |
159 |
4 |
30 |
0,005 |
0,795 |
159 |
5 |
45 |
0,005 |
0,795 |
159 |
6 |
60 |
0,005 |
0,795 |
159 |
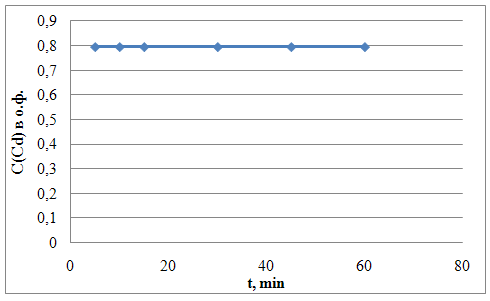
Рис.13 Зависимость экстракции кадмия от времени контактирования фаз
Из полученных данных видно, что равновесие устанавливается очень быстро, уже при 5 минутах достигается максимальное извлечение кадмия в органическую фазу. Дальнейшее увеличение времени контактирования фаз на извлечение кадмия в органическую фазу не влияет.
2.2.2 Влияние рН водной фазы на экстракцию кадмия
Известно, что экстракция азотсодержащими реагентами существенно зависит от рН раствора [ ], поэтому нами была изучена зависимость экстракции кадмия от рН раствора. Экстракцию кадмия проводили 0,062 М раствором НБЭА–2 в диапазоне рН от 4 до 13. Исходная концентрация кадмия – 1 г/л, время контакта фаз 5 мин, соотношение Vo : Vв = 1 : 1. Полученные данные представлены в табл. 5 и на рис.12.
Таблица 5
Зависимость экстракции кадмия от рН раствора
№ |
рН |
ХCd, г/л |
YCd, г/л |
D |
1 |
4,01 |
0,98 |
0,02 |
0,02 |
2 |
4,97 |
1 |
0 |
0 |
3 |
6,80 |
0,97 |
0,03 |
0,031 |
4 |
8,30 |
0,005 |
0,995 |
199 |
5 |
8,99 |
0,005 |
0,995 |
199 |
6 |
10,40 |
0,005 |
0,995 |
199 |
7 |
11,22 |
0,005 |
0,995 |
199 |
8 |
11,98 |
0,005 |
0,995 |
199 |
9 |
12,91 |
0,005 |
0,995 |
199 |
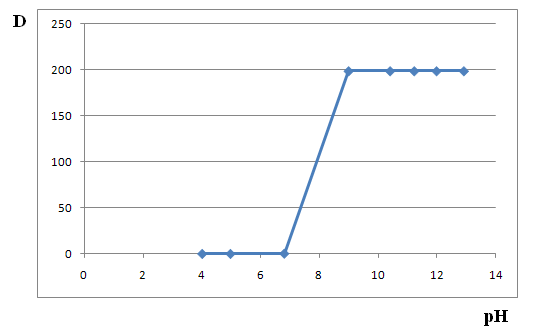
Рис.12. Зависимость коэффициента распределения кадмия от рН раствора
Полученные данные показали, что в диапазоне рН от 4 до 7 кадмий практически не экстрагируется, однако с увеличением рН коэффициент распределения кадмия резко возрастает и достигает максимума (DCd = 200) в диапазоне рН 8,30-13,00. Таким образом, в интервале рН 8,3-13 наблюдается наиболее полное извлечение кадмия в органическую фазу.
Для выявления экстрагируемой формы кадмия в изученной системе было проведено сопоставление зависимости экстракции кадмия от рН раствора с формами его существования в данных растворах (рис. 13). Проведенное сопоставление показывает, что по мере роста в растворе катиона Cd(OH)+ растет и экстракция кадмия, максимальная же его экстракция наблюдается при максимальном содержании в водных растворах Cd (OH)+ по всей видимости, именно этот катион и взаимодействует с НБЭА-2.
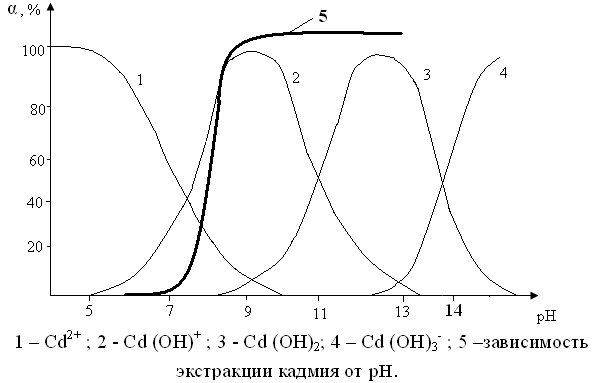
Рис. 13. Сопоставление зависимости распределения гидроксокомплексов кадмия в растворах от pH [Енов Б.Б., Камнев А.А. Определение состава гидроксокомплексов кадмия и кобальта в щелочных растворах. – Координац., химия, 1983, т.9, №9, с 1207-1211.] с экстракцией кадмия НБЭА-2.
