
10. Элементтердің d-және f- топтамалары.
d-элементтер сырттан санағанда 2-ші деңгейдің d-орбитальдары электронға тола басталады. Периодтық жүйеде қазір барлығы 35- d элемент бар. Топ бойынша 3-ші В мен 2-ші В топшаны құрайды.
Әдетте көпшілік d-элементтердің сыртқы деңгейінде 2 (ns2) электрон болады. Алайда кейбір элементтердің (Cr,Mo,Ru,Rh,Pt, Pd және т.б. ) сыртқы деңгейіндк бір не ноль электрон болады. Барлық d-элементтер таза металдар. Олардың валенттілігіне сыртқы s-және одан кейінгі d-электрондар қатысады, ең жоғарғы валенттілігі топ нөміріне сәйкес.
f-периодтық жүйеде 28- f элемент бар. Олар период жүйесінде 6-7-ші периодта орналасқан. Барлық f-элементтер таза металдар, жақсы тотықсыздандырғыштар.
11. Менделеевтің пз-нің ескі анықтамасы.
Элементтер қасиеттерінде байқалатын осындай заңдылықтар негізінде 1869 Менделеев периодтық заңды ашты:
Жай заттардың қасиеттері, сондай-ақ олардың қосылыстарының формаларымен қаситтері элементтердің атомдық массаларының мөлшеріне периодты түрде тәуелді болады.
12. Менделеевтің Пз-нің жаңа анықтамасы.
Енді Мозли заңына сәйккес Менделеевтің периодтық заңының жаңа анықтамасы былай айтылады:
Элементтердің қасиеттері, сондай ақ олардың қосылыстарының формалары мен қасиеттері элементтердің ядро зарядтарының өсуі не периодты түрде тәуелді болады.
13. Период дегеніміз ядро зарядының біртіндеп өсуі және қасиеттерінің белгілі бір тәртіппен өзгеру бағытымен орналасқан элементтердің жиынтығы. Периодта элементтер саны белгілі заңдылыққа бағынып орналасады. Бірінші периодта екі элмемент, 3-4 сегіз элемент, 4-5-те 18 элемент, 6-7-де 32 элемент болады. Әр периодтың басы жаңа электрон қабатымен басталуымен сай келеді. Сондықтан периодтың нөмірі ондағы элементтердің атомдарында болатын квант қабатының ең шеткі санын көрсетеді мысалы, 5-ші период элементтерінің атомдарының саны 5 квант қабаты бар. Период сілтілік метал s-элементтен басталып инертті газбен, яғни p-элементпен аяқталады. Периодтың соңындағы инертті элементтің ақырғы квант қабаты сегіз электронды симметриялы болып келеді, оның конфигурациясы ns2,np6. Период қазіргі кезде қысқа периодты және ұзын перидты болып бөлінеді. Екі түрының де құрылысы кесте 7 период 8-топтан тұрады. Сонымен бірге, перид кіші және үлкен период болып бөлінеді. Кіші период 8-элементтен ал үлкен период 18-және одан да көп элементтен тұрады.
Период ішіндегі элемент қасиеті бойынша өзгереді: Әрбір период күшті сілтілік металмен басталып бірте-бірте металдық қасиет кеміп амфотерлі қасиеті бар элементтер шығып одан бейметелдарға ең күштілері галогендерге яғни асыл газбен бітеді.
14. Үлкен периодтардың сипаттамасы. Химиялық элементтердің периодтық жүйесінде 7 период бар. Кіші периодтар бір ғана қатардан, ал 2-периодтан 7-периодқа дейін 2 қатардан тұрады, олар үлкен периодтар деп аталады.
Үлкен периодтар сілтілік және жер металдарынан кейін электрондық қабаттың толуы басқаша жүреді.
Әр периодтың ішінде элементтің металдық қасиеті солдан оңға әлсрей бастайтындықтан үлкен периодтар жоғары жұп санды қатардағы элементтердің металдық қасиеттері, төменгі тақ қатардағы элементтердің қасиеттерінен басым болады.
Үлкен периодтар элементтері.
Rb +37
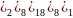 рубидий
рубидий
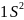 ,
,
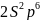 ,
,
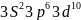 ,
,
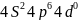 ,
,
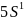
![]() S –
элемент
S –
элемент
І +53
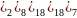 йод
йод
![]()
15. Химиялық элементтердің периодтық жүйесінде 7 период бар. Кіші периодтар бір ғана қатардан (1-3), ал 4-периодттан бастап 7-периодқа дейін екіқатардан тұратын период, үлкен периодтар деп аталады.
Кіші периодтарда ядро зарядының мәні артқан сайын сыртқы қабаттағы электрондар саны өседі. Бұл жоғары валенттіктің өсуіне, металдық қасиеттің бәсеңдеуіне, бейметалдық қасиеттің артуына әкеледі.
Сол сияқты сәйкес жоғарғы оксидтері мен гидроксидтерінің негіздік қасиеттері де екідайлылыққа, одан әрі қышқылдаққа ауысады. Кіші периодтарда тек S- және p-элементтері болады.
Кіші период элементтері:
![]()
І
период Н
+1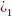
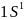
II
период
Li
+3
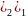
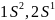
ІІІ
период
Р +15
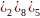 ,
,
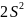 ,
,
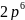 ,
,
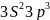
16. Әрбір периодта солдан оңға қарай элементтердің реттік нөмірі өсуіне байланыста олардың металдық қасиеттері кеміп, бейметалдық қасиеттері артады. Оның себебі атом құрылысы тұрғысынан қарағанда бір периодтағы элементтердің электрондық қабаттарының саны өзгермейді, ал ядро зарядтарының саны біртіндеп арта береді де ыртқы валенттілік электрондардың ядроға тартылуы күшееді. Осының нәтижесінде элементтердің радиустары кішірейіп электрон беру қабілеті азаяды, яғни металдық қасиеттері кемиді де, бейметалдық қасиеттер артады. Мыс 3-ші перидтың элементтері натрий атомының радиусы 0,110 нм, ал Хлор атомының радуисы 0,073 нм. Сондықтан атомның радиусы үлкен натрий күшті металл. Ал радиусы, кіші хлор күшті бейметалл.
17. Үқсас қасиеттеріне сай орналасқан элементтердің вертикаль қатарын топ деп атайды.
Топ негізгі және қосмша блып бөлінеді. Әр топшаның нөмірі сол топшада орналасқан элементтің валенттілігін көрсетеді. Негізгі топшада металдар (Li,Na,K,Rb,Cs,Fr.) Бұлар S элементтер атомдардың сыртқы энергетикалық деңгейінде бір-бірден электрон бар. Химиялық әрекеттескенде олар валеттілік электрондарын оңай беріп тұрақты +1 тотығу дәрежесі көрсетеді.
18. Негізгі топшалар сипаттамасы. Негізгі топшалар ұзын болады үйткені оларға барлық дерлік периодтардың элементтері кіреді. Негізгі топша элементтерінің атомдарының соңғы электрондары ең сыртқы қабаты ns не болмаса np қатпарына орналасады. Осыған орай оларды s және p элементтері деп атйды. Бұл екі s жәнер қатбарында 8-электрон болғандықтан негізгі топшаның жалпы саны 8 болады.Бұл элементтер әрекеттескенде реакцияға олардың сыртқы қабатындағы электрондардың барлығыда қатыса алады.
19. Қосымша топшалар қысқарақ себебі олардың элементі 4 периодтан басталады. Олар алғашқы екі Sэлементтен соң келетін болғандықтан металдық қасиетін төмендеу бағытында тұр. Бірақ мұнда жоғарыдағы периодтармен салыстырғанда металдық қасиет өте бояу әлсірейді үйткені олардың ішкері d қатпары біртіндеп электрондаға тола бастайды. Бұлардан соң метал еестік қасиеті бар р-элементтері келеді.
20. Негізгі топшадағы элементтердің реттік нөмірі жоғарылап жіне иондану энергиясы төмендеген сайын элементтердің металдық қасиеті заңды артады, электрондарын оңай береді.
21. Атом құрылысының s-элементтерде сыртқы деңгейдің s-орбиталіне электрон тола бастайды. S-Орбиталіне тек электрон сиятындықтан, s-элементтердің де сыртқы деңгеінде не 1, не 2-электрон болады. Сонымен s-элементтер период жүйесінің 1А және 2А
Топшасынан орын алады. Оларға сутегі мен гелий де кіреді жалпы период жүйесінде қазір 14- s элемент бар. 1-ші А топшадаға элементтердің сыртқы деңгейінде 1- s электрон бар, ал 2А топшадағы элементтердің сыртқы деңгейінде 2- s электрон болады. Олар сыртқы электрондарын әр-қашан беріп, күшті тотықсыздандырғыш қасиет көрсетеді. Химиялық байланыс түзген кезде олардың тотығу дәрежесі әрқашан ОҢ болады. (+1, -1)
Атом құрылысынан р-элементтердің р-орбиталі тола басталып, р-орбитальдің сиымдылығы 6-электрон демек, әр периодта 6- элемент бар. Периодты жүйеде 30-р элемент бар ол элементтердің сыртқы деңгейінде электрон саны 3-тен 8-ге дейін өседі. Период бойынша р-элементтің метал еместік қасиеті артады. Себебі сыртқы электрон саны өскен сайын олардың ядроға тартылуы күшееді. Сөйтіп р-элементтердің электрон беруден гөрі қосып алу қасиеті күшееді. Яғни тотықтырғыш қасиеті басым. Р-элемент қосылыс түзген кезде сыртқы р-электрондар мен қатар s-электрондар байланыс түзуге қатысады. Олардың валенттілігі топың нөміріне сәйкес келеді.
22. d-элементтер сырттан санағанда 2-ші деңгейдің d-орбитальдары электронға тола басталады. Периодтық жүйеде қазір барлығы 35- d элемент бар. Топ бойынша 3-ші В мен 2-ші В топшаны құрайды.
Әдетте көпшілік d-элементтердің сыртқы деңгейінде 2 (ns2) электрон болады. Алайда кейбір элементтердің (Cr,Mo,Ru,Rh,Pt, Pd және т.б. ) сыртқы деңгейіндк бір не ноль электрон болады. Барлық d-элементтер таза металдар. Олардың валенттілігіне сыртқы s-және одан кейінгі d-электрондар қатысады, ең жоғарғы валенттілігі топ нөміріне сәйкес.
f-периодтық жүйеде 28- f элемент бар. Олар период жүйесінде 6-7-ші периодта орналасқан. Барлық f-элементтер таза металдар, жақсы тотықсыздандырғыштар.
23) Ковалентті полюссіз байланыс дегеніміз теріс элетірлігі бірдей бейметал атомдар арасында жүретін байланыс. М: Н•+Н•- H(:)Н
Екі сутек атомының да электртерістілігі бірдей, сондықтан олар байланыстырушы электрон бұлтына бірдей күшпен әсер етеді. Байланыстырушы электрон бұлты ешқандай атомға қарай ығыспайды, екі атом ешқайсысында да артық заряд жоқ.
24) Ковалетті полюсті байланыс дегеніміз теріс электрлігі әр түрлі бейметал атомдары арасында жүретін байланыс. М:HCl-H•+Cl
Мүнда байланыстырушы электрон бұлты хлорға қарай ығысқан, электртерістілігі теріс жаққа қарай барады, әр түрлі атомдар арасында болады, сондықтан ковалетті полюсті .
25) 1. Ковалетті байланыстың ұзындығы-өзара байланысқан атомдардығ ядроларының арасын байланыстыратын қашықтық.
2. Химиялық байланысты түзу үшін немесе оны бұзу үшін байланыстың энергиясы деп атайды.
3. Қанығу ковалеттік байланыстың белгілі бір шекті мөлшерде түзілуі қанығу деп аталады.
26.Ковалетті байланыстың электрон бұлттарының белгілі бағыты болады, осының салдарының молекулалар белгілі бір құрылысқа ие болады. Ковалентті байланыстың бағытын білу үшін атомның байланыс түзуге жұмсайтын орбитальдарының пішінін білу керек. Атомдардың орбитальдары кез келген бағытта емес, тек өздерінің пішіндеріне сай бағытта ғана бүркеседі.
27.Зарядталған бөлшектердің арасында электрстатикалық тартылыс күштерінің арқасында пайда болатын байланыс иондық байланыс деп аталады. Иондық байланыстың бағыты болмайды және қанықпайды.
NaCl Na 1s22s2 2 p6 3s1 –le ->
Na + 1 s22s 2 2 p 6 3s0
Cl 1S22S2 2P63S23p5 + le ->
Cl – 1s2 2s2 2p6 3s2 3p6
28.Сутектік байланыс құрамында сутегі және электртерістілігі жоғары элемент атомы бар молекулаларда кездеседі. Сутегіндік байланысты нүктемен белгілейді, ол ковалетті байланысқа қаоағанда әлсіз. Дегенмен молекулаларды бірі-біріне біріктіріп ұстай алады. Сутектік байланыс молекулааралық және молекулаішілік болып бөлінеді.
29. Металдық байланыс – металдарда кездеседі. Метал атомдарының сыртқы энергетикалық деңгейдегі валенттік электрондардың саны аз болады. 1,2,3 немесе 4 сирек кездеседі.
30. Валенттік электрондардың гибриттенуі деп атомның пішіндері және энергиялары әр түрлі орбитальдарының һзара араласып, бір пішіндес және тең энергиялы орбитальдарға айналуын айтады. Гибреттенуге 1s және 3p-орбитальдары қатысатындықтан, түзілген орбитальдар sp3-гибритті орбитальдар деп аталады. Мұндағы s-тің пішіні шар тәрізді, ал p-нің пішіні гантель. Екеуі қосылып sp3-жаңа пішінді орбиталь түзеді. Бастапқыда p мен s-тің энергиялары әр түрлі еді, кейіннен екеуінін қосылғанна кейінгі энергиясы тең болды.
31.Термодинамика- энергиялардың арасындағы байланыст орнататын, өз бетінше жүретін процесстердің мүмкіншілігін, бағытын және шегін зерттейтін ғылымның саласы.
Химиялық термодинамика-химиялық реакцияларды фазалық өзгерістерді адцорбциялардың, энергияның бір түрден екінші түрге айналуын зерттейді.
32. Термодинамикалық параметрлер-жүйенің күйін сипаттайтын физикалық шамалар (температура, көлем,қыым)
Термодинамикалық процесс-жүйенің күйін сипаттайтын термодинамикалық параметрлердің кез келген біреуінің өзгерісі.
33. Жүйе-сыртқы ортада белгілі бір бөліну шекаралармен шектелегн заттардың жиынтығы.
Ашық жүйе-қоршаған ортамен затта, энергияда алмасады. Жабық жүйе қоршаған ортамнһен энергия ғана алмасады. Тұйық жүйе- қоршаған ортамен затта энергия алмаспайды. Гомогенді жүйе- бір фазадан тұрады. Гетерогенді жүе бірнеше фазадан тұрады.
Фаза- жүйенің нақты және белгілі беткейлерімен бөлінген, құрамы мен физикалық химиялық қасиеттері бойынша біртеті бөліктерінің жиынтығы.
