
- •3. Ферментативный катализ_______________
- •3. Ферментативный катализ.
- •3.1 .Строение ферментов.
- •3.2. Механизм действия ферментов.
- •3.3. Специфичность ферментов.
- •3.4. Изоферменты.
- •3.5. Кинетика ферментативного катализа.
- •3.5.1. Зависимость скорости ферментативной реакции
- •3.5.2. Зависимость скорости ферментативной реакции
- •3.5.3. Зависимость скорости ферментативной реакции
- •3.5.4. Зависимость скорости ферментативной реакции от рН.
- •3.6. Ингибиторы ферментов.
- •3.7. Активаторы ферментов.
- •3.8. Регуляция скорости ферментативных реакций.
- •3.9. Классификация и индексация ферментов.
- •IV класс - лиазы – ферменты, катализирующие расщепление химических связей без присоединения воды:
- •V класс - изомеразы - ферменты, катализирующие изомерные превращения, т.Е. Перенос отдельных химических групп в пределах одной молекулы:
- •3.10. Номенклатура ферментов.
3.9. Классификация и индексация ферментов.
Современная классификация ферментов основывается на характере химической реакции, катализируемой ферментом. Все ферменты делятся на шесть классов в зависимости от типа катализируемой реакции:
I класс – оксидоредуктазы - ферменты, катализирующие окислительно-восстановительные реакции.
Схематично действие ферментов I класса можно записать:
 A
+ B C + D
A
+ B C + D
II класс – трансферазы – ферменты, катализирующие перенос химических группировок с молекулы одного вещества на молекулу другого:
AB + C A + BC
III класс – гидролазы – ферменты, расщепляющие химические связи путем присоединения воды, т.е. путем гидролиза:
AB + H2O A-H + B-OH
IV класс - лиазы – ферменты, катализирующие расщепление химических связей без присоединения воды:
 AB
A + B
AB
A + B
V класс - изомеразы - ферменты, катализирующие изомерные превращения, т.Е. Перенос отдельных химических групп в пределах одной молекулы:
A B
VI класс - синтетазы - ферменты, катализирующие реакции синтеза, протекающие за счет энергии гидролиза АТФ:
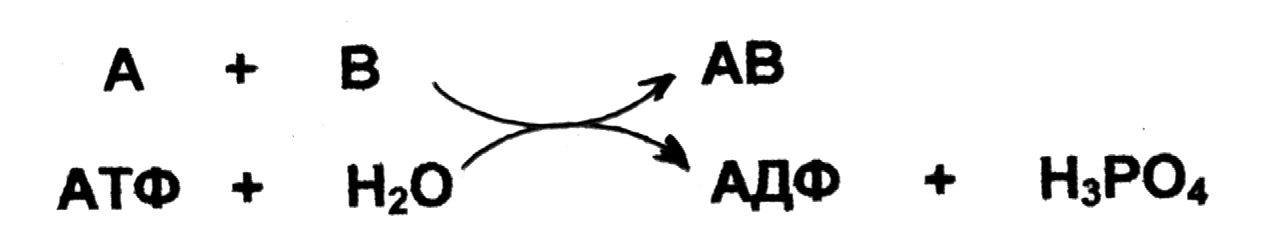
Каждый класс, в свою очередь, делится на подклассы, внутри подклассов выделены подподклассы. Каждый подподкласс содержит список индивидуальных ферментов в строго определенной последовательности, которая не изменяется, а лишь продлевается по мере открытия новых ферментов.
В основе подразделения ферментов на подклассы и на подподклассы лежит тип химической связи или химическое строение группировки субстрата, на которую действует фермент.
С классификацией ферментов тесно связана их индексация (нумерация). Индекс (шифр) каждого фермента состоит из четырех чисел, разделенных точками, и составляется по следующему принципу:
Первая цифра индекса указывает к какому из шести классов принадлежит данный фермент. Второе и третье числа индекса обозначают соответственно порядковые номера подклассов и подподклассов. Четвертое число индекса – порядковый номер индивидуального фермента внутри своего подподкласса.
Например, фермент слюны – амилаза, расщепляющий крахмал, имеет индекс 3.2.1.1., что свидетельствует о принадлежности этого фермента к классу гидролаз.
3.10. Номенклатура ферментов.
Название фермента, как правило, состоит из двух частей. Первая часть является названием субстрата, превращения которого катализируется данным ферментом. Вторая часть названия, имеющая окончание -аза, указывает природу реакции. Например, фермент, отщепляющий от лактата (молочная кислота) атомы водорода, называется лактатдегидрогеназа; фермент, катализирующий изомеризацию глюкозо-6-фосфата в фруктозо-6-фосфат, имеет название глюкозофосфат-изомераза; а фермент, участвующий в синтезе гликогена, - гликогенсинтетаза.

Полезная информация
Энергия активации – избыток энергии (выше среднего), которым должны обладать молекулы, чтобы их столкновение оказалось продуктивным, т.е. привело бы к химической реакции. Изменение величины энергии активации в большой мере влияет на скорость реакции: незначительное уменьшение энергии активации приводит к резкому повышению скорости реакции, и, наоборот, самое небольшое ее возрастание сопровождается весьма значительным снижением скорости
