
- •Введение.
- •1. Основная часть
- •1.1. Из истории кристаллографии
- •1.2.Технологии выращивания кристаллов.
- •1.3. Форма кристаллов.
- •2. Экспериментальная часть.
- •2.1. Выращивание кристаллов из горячего насыщенного раствора солей.
- •2.2. Влияние различных добавок на процесс формирования кристаллов.
- •2.3. Влияние различных факторов на кристаллизацию сульфата железа (II).
- •2.4. Получение кристаллов лимонной кислоты.
- •2.5. Определение размеров кристаллов
- •Заключение
2.2. Влияние различных добавок на процесс формирования кристаллов.
1

 .
Добавление в насыщенный раствор сульфата
меди (II)
серной кислоты привело к ускорению
процесса выпадения кристаллов, но их
цвет стал менее насыщенным и прозрачным,
а более матовым (рисунок 6).
.
Добавление в насыщенный раствор сульфата
меди (II)
серной кислоты привело к ускорению
процесса выпадения кристаллов, но их
цвет стал менее насыщенным и прозрачным,
а более матовым (рисунок 6).
Рисунок 6.
2. Добавление в раствор немного этилового спирта или сульфата калия, приводит к искажению формы кристаллов, причём небольшое количество сульфата калия скругляет грани кристаллов, но с увеличением его количества кристаллы всё сильнее меняют форму – становятся более похожими на наклонённые призмы (рисунок 7).

Рисунок 7.
2.3. Влияние различных факторов на кристаллизацию сульфата железа (II).
 1.
При растворении в воде сульфата железа
(FeSO4·7H2O)
или железного купороса. раствор вначале
становится молочно-белым, а потом зелёным
и прозрачным. Из такого раствора растут
очень красивые слоистые кристаллы
интересной формы нежно-зелёного цвета.
Но с этими кристаллами у меня возникли
проблемы их хранения: поваренная соль
и медный купорос – более стойкие соли,
а вот кристаллы железного купороса,
несмотря на то, что были покрыты бесцветным
лаком, начали терять содержавшуюся в
них воду и покрываться невзрачным белым
порошком (рисунок 8).
1.
При растворении в воде сульфата железа
(FeSO4·7H2O)
или железного купороса. раствор вначале
становится молочно-белым, а потом зелёным
и прозрачным. Из такого раствора растут
очень красивые слоистые кристаллы
интересной формы нежно-зелёного цвета.
Но с этими кристаллами у меня возникли
проблемы их хранения: поваренная соль
и медный купорос – более стойкие соли,
а вот кристаллы железного купороса,
несмотря на то, что были покрыты бесцветным
лаком, начали терять содержавшуюся в
них воду и покрываться невзрачным белым
порошком (рисунок 8).
Р
Рисунок 8.
Чтобы повысить устойчивость кристаллов сульфата железа, я добавила в раствор серную кислоту. В результате кристаллы изменили свою форму – кристаллы сульфата железа-аммония более вытянутые, и слоистые в другом направлении (рисунок 9).


Рисунок 9.
2.4. Получение кристаллов лимонной кислоты.
Хрупкие, но невероятно красивые, чистые и прозрачные кристаллы выросли из лимонной кислоты. Да, вы не ослышались, кристаллы можно вырастить не только из соли, но и кислоты, явление это невероятное, но твёрдых кислот довольно большое количество, так что удивляться здесь нечему. Кристаллы имеют форму ромбоэдра или ромбододекаэдра – многогранника, у которого все грани имеют форму ромбов. Растворимость лимонной кислоты достаточно большая, если растворять в горячей воде, получится что-то вроде сиропа. Кристаллы сохраняются плохо, если не покрыть сразу же бесцветным лаком, то через 2-3 недели образуются белые крапинки, но даже лак не защитит кристалл от постепенного выветривания – через полгода белый налёт всё равно образуется.
2.5. Определение размеров кристаллов
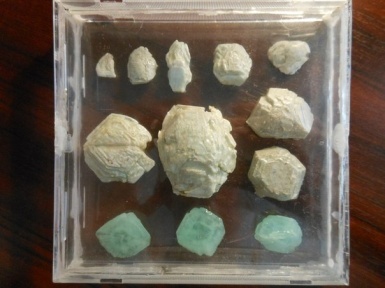
В процессе выращивания кристаллов, я обратила внимание на различные размеры образующихся кристаллов. На рисунке 10 представлены размеры кристаллов.
Рисунок 10. 1.Сульфат никеля 2. Лимонная кислота 3. Сульфат железа (II) 4. Хлорид натрия 5. Медный купорос

Как видно из данных представленных на рисунке 9 наибольший размер имеют монокристаллы медного купороса.
Заключение
В ходе экспериментальной части работы я узнала, что кристаллы в домашних условиях можно вырастить из более, чем из двадцати разных веществ. Не все они, к сожалению, доступны и легко-получаемы. Мне удалось вырастить самые разнообразные кристаллы, которые отличаются друг от друга и по форме, и по цвету, по размеру и по степени устойчивости. Так что основная цель моей работы достигнута.
Кроме того я выяснила условия формирования кристаллов и изучила ряд факторов влияющие на рост кристаллов их форму и размер. Все это позволило мне получить кристаллы для оформления своей работы на конкурсе и существенно расширило мои знания в области кристаллографии.
На основании изученной литературы и выполненного эксперимента можно сделать следующие выводы:
Мною выращены кристаллы из 12 химических соединений, включая соли и лимонную кислоту.
Наиболее быстро образуются следующие кристаллы: сульфат меди (II), сульфат меди-аммония, сульфат железа (II), сульфат железа-аммония.
Полученные кристаллы имеют следующие формы: правильная кубическая, прямоугольная призма, шестигранная призма, а также слоистые кристаллы.
Наиболее устойчивые кристаллы – это кристаллы медного купороса и поваренной соли (хлорида натрия).
Полученные кристаллы имеют различную цветовую окраску, которая может изменять свою интенсивность в зависимости от условий эксперимента.
Добавление некоторых веществ в раствор для кристаллизации может ускорить процесс образования кристаллов, изменять из цветовую окраску и изменять форму образующихся кристаллов.
Наиболее крупные монокристаллы образуют медный купорос (кристаллогидрат сульфата меди II) и хлорид натрия.
Список использованной литературы:
«Биофайл» научно-информационный журнал – Предмет история кристаллографии (http://biofile.ru/geo/3283.html)
«Мир кристаллов» - Применение кристаллов в науке и технике, автор: Батенева О.М., учитель физики МАОУ «СОШ №2» г. Урай 2009г. (http://course-crystal.narod.ru/p31aa1.html)
Информационно образовательный портал «Veni, VIdi, Vici» - Разнообразие кристаллических форм, составители: Логинов В.Н., Корженко О.И., рецензент доктор г.-м.н. И.Н. Бушляков (http://www.vevivi.ru/best/Raznoobrazie-kristallograficheskikh-form-ref212085.html)
«О кристаллах» авторы: Логвинова С., Чопорова Ж.В., Усович О. (http://www.pandia.ru/text/77/146/67.php)
«Выращивания кристаллов в результате взаимодействия растворов различных солей», авторы: Цвиленева Ю, Оробец В. (http://nsportal.ru/ap/ap/nauchno-tekhnicheskoe-tvorchestvo/vyrashchivanie-kristallov-v-rezultate-vzaimodeystviya)
Опыты в домашней лаборатории.- М.: Наука. Главная редакция физико- математической литературы,1980г,144с.
«Горные породы и минералы» Научно - поп. издание. Москва, Мир, 1986
«Драгоценные камни», Смит Г, Мир, 1980
«Практическое руководство по минералогии», Смольянинов Н. А, геологическая литература, 1948
Toplivo2 – сайт для химиков, автор: Максим Мартынов (http://toplivo2.ru/?p=1072 и http://toplivo2.ru/?p=351
