
- •1 Теоретическая часть
- •1.1 Устройство и принцип действия насадочного абсорбера
- •1.2 Равновесие при абсорбции
- •1.3 Материальный баланс процесса
- •1.4 Гидравлические условия работы насадочных колонн
- •1.5 Расчет высоты абсорбера
- •2 Расчет насадочного абсорбера
- •2.1 Определение массы поглощаемого вещества и расхода поглотителя
- •2.2 Расчет движущей силы
- •2.3 Расчет скорости газа и диаметра абсорбера
- •2.4 Определение плотности орошения и активной поверхности насадки
- •2.5 Расчет коэффициента массопередачи
- •2.6 Определение поверхности массопередачи и высоты абсорберов
- •2.7 Гидравлическое сопротивление
- •3 Эскиз насадочного абсорбера
- •4 Контрольные вопросы
- •5 Рекомендуемая литература
Практическая работа №4.
Расчет насадочного абсорбера
1 Теоретическая часть
1.1 Устройство и принцип действия насадочного абсорбера
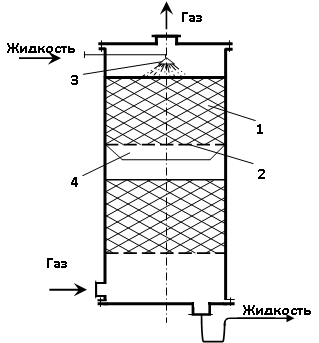
1 — насадка; 2 — опорная решетка; 3 — распределитель жидкости; 4 — перераспределитель жидкости
Рисунок 1 . Насадочная колонна
В насадочной колонне (рисунок 1) насадка 1 укладывается на опорные решетки 2, имеющие отверстия или щели для прохождения газа и стока жидкости. Жидкость с помощью распределителя 3 равномерно орошает насадочные тела и стекает вниз.
По всей высоте слоя насадки равномерное распределение жидкости по сечению колонны обычно не достигается, что объясняется пристеночным эффектом — большей плотностью укладки насадки в центральной части колонны, чем у ее стенок. Вследствие этого жидкость имеет тенденцию растекаться от центральной части колонны к ее стенкам. Поэтому для улучшения смачивания насадки в колоннах большого диаметра насадку иногда укладывают слоями (секциями) высотой (35)D и под каждой секцией, кроме нижней, устанавливают перераспределители жидкости 4.
В насадочной колонне жидкость течет по элементу насадки главным образом в виде тонкой пленки, поэтому поверхностью контакта фаз является в основном смоченная поверхность насадки, и насадочные аппараты можно рассматривать как разновидность пленочных. Однако в последних пленочное течение жидкости происходит по всей высоте аппарата, а в насадочных колоннах — только по высоте элемента насадки. При перетекании жидкости с одного элемента насадки на другой пленка жидкости разрушается и на нижележащем элементе образуется новая пленка. При этом часть жидкости проходит через расположенные ниже слои насадки в виде струек, капель и брызг. Часть поверхности насадки бывает смочена неподвижной (застойной) жидкостью.
Основными конструктивными характеристиками насадки являются ее удельная поверхность и свободный объем.
Удельная поверхность насадки а — это суммарная поверхность насадочных тел в единице занимаемого насадкой объема аппарата. Удельную поверхность обычно измеряют в м2/м3. Чем больше удельная поверхность насадки, тем выше эффективность колонны, но ниже пропускная способность и больше гидравлическое сопротивление.
Под свободным объемом насадки ε понимают суммарный объем пустот между насадочными телами в единице объема, занимаемого насадкой. Свободный объем измеряют в м3/м3 . Чем больше свободный объем насадки, тем выше ее пропускная способность и меньше гидравлическое сопротивление, однако при этом снижается эффективность работы насадки.
Конструкции насадок, применяемых в промышленных аппаратах можно разделить на две группы — нерегулярные (насыпные) и регулярные насадки.
В зависимости от используемого для изготовления насадки материала они разделяются на металлические, керамические, пластмассовые, стеклянные, стеклопластиковые и др. В таблице П2 даны характеристики некоторых нерегулярных насадок, загружаемых в навал.
1.2 Равновесие при абсорбции
При абсорбции содержание газа в растворе зависит от свойств газа и жидкости, давления, температуры и состава газовой фазы (парциального давления растворяющегося газа в газовой смеси).
В случае растворения в жидкости (С) бинарной газовой смеси (распределяемый компонент А, носитель В) взаимодействуют две фазы (Ф=2), число компонентов равно трем (К = 3) и, согласно правилу фаз, число степеней свободы системы равно трем.
Для данной системы газ-жидкость переменными являются температура, давление и концентрации в обеих фазах. Следовательно, в состоянии равновесия при постоянных температуре и общем давлении зависимость между парциальным давлением газа А (или его концентрацией) и составом жидкой фазы однозначна. Эта зависимость выражается законом Генри парциальное давление р*А растворенного газа пропорционально его мольной доле хА в растворе:
 (1)
(1)
Или растворимость газа (поглощаемого компонента А) в жидкости при данной температуре пропорциональна его парциальному давлению над жидкостью:
 , (2)
, (2)
где
 – парциальное
давление поглощаемого газа, находящегося
в равновесии с раствором, имеющим
концентрацию хА
(в
мол. долях);
– парциальное
давление поглощаемого газа, находящегося
в равновесии с раствором, имеющим
концентрацию хА
(в
мол. долях);
 –
концентрация
газа в растворе (в мол. долях), равновесном
с газовой фазой, в которой парциальное
давление поглощаемого компонента равно
рА;
Е
–
коэффициент пропорциональности,
называемый коэффициентом, или константой
Генри.
–
концентрация
газа в растворе (в мол. долях), равновесном
с газовой фазой, в которой парциальное
давление поглощаемого компонента равно
рА;
Е
–
коэффициент пропорциональности,
называемый коэффициентом, или константой
Генри.
Числовые значения коэффициента Генри для данного газа зависят от природы поглотителя и газа и от температуры, но не зависят от общего давления в системе.

Рисунок 2 – Растворимость газа в жидкости при различных температурах (t1>t2>t3 и соответственно E1>E2>E3)
Зависимость Е от температуры выражается уравнением:
 (3)
(3)
где q – дифференциальная теплота растворения газа;
R – газовая постоянная;
С – постоянная, зависящая от природы газа и поглотителя.
Для идеальных растворов на диаграмме р–х (рисунок 2) зависимость равновесных концентраций от давления изображается прямой, имеющей наклон, равный Е – коэффициенту Генри. Из рисунка 2 и уравнения (3) следует, что с повышением температуры (при прочих равных условиях) увеличивается значение Е и соответственно уменьшается, согласно уравнению (2), растворимость газа в жидкости.
Если уА – мольная доля извлекаемого компонента А в газовой смеси и Р – общее давление в системе, то парциальное давление , по закону Дальтона, можно выразить зависимостью:
 . (4)
. (4)
Подставив значение в уравнение (1), получим:
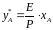 . (5)
. (5)
или закон Генри может быть представлен в форме:
 . (6)
. (6)
где т = E / P – коэффициент распределения, или константа фазового равновесия.
Уравнение (6) показывает, что зависимость между концентрациями данного компонента в газовой смеси и в равновесной с ней жидкости выражается прямой линией, проходящей через начало координат и имеющей угол наклона, тангенс которого равен т. Числовые значения величины т зависят от температуры и давления в системе: уменьшаются с увеличением давления и снижением температуры. Таким образом, растворимость газа в жидкости увеличивается с повышением давления и снижением температуры.
Когда в равновесии с жидкостью находится смесь газов, закону Генри может следовать каждый из компонентов смеси в отдельности.
Закон Генри справедлив только для идеальных растворов. Поэтому он с достаточной точностью применим лишь к сильно разбавленным реальным растворам, приближающимся по свойствам к идеальным, т. е. соблюдается при малых концентрациях растворенного газа или при его малой растворимости. Для хорошо растворимых газов, при больших концентрациях их в растворе, растворимость меньше, чем следует из закона Генри. Для систем, не подчиняющихся этому закону, коэффициент т в уравнении (6) является величиной переменной, и линия равновесия представляет собой кривую, которую строят обычно по опытным данным.
Для описания равновесия между газом и жидкостью уравнение (6) применимо только при умеренных давлениях, невысоких температурах и отсутствии химического взаимодействия между газом и поглотителем.
