- •Лекція . Токсичні речовини в харчових продуктах. Харчування і безпека життєдіяльності План лекції
- •1. Токсичні речовини харчових продуктів: природні компоненти продуктів, що проявляють шкідливу дію та шкідливі речовини, які потрапляють у їжу ззовні класифікація чужорідних речовин
- •Забруднення речовинами, які застосовуються в рослинництві
- •Природні токсиканти
- •Антиаліментарні фактори харчування
- •Шляхи надходження чужорідних речовин в продукти харчування
- •2. Міри токсичності. Міжнародний і Державний контроль безпеки харчових продуктів.
- •Міжнародний і Державний контроль безпеки харчових продуктів
- •Заходи щодо зменшення небезпечних речовин в харчових продуктах.
- •4. Ідентифікація небезпечних речовин.
- •Контрольні питання
4. Ідентифікація небезпечних речовин.
Методи визначення мікотоксинів. Сучасні методи виявлення й визначення змісту мікотоксинів у харчових продуктах: Скринінг-методи Це мініколоночний метод визначення афлатоксинів, охратоксину А й зеараленону; методи тонкошарової хроматографії (ТШХ-методи) для одночасного визначення до 30 різних мікотоксинів, флуоресцентний метод визначення і деякі інші. Кількісні аналітичні методи визначення мікотоксинів представлені хімічними, радіоімунологічними й імуноферментними методами. Високочутливі й високоспецифічні радиоімуно-хімічні й імуноферментні методи виявлення, ідентифікації й кількісного визначення мікотоксинів засновані на одержанні антисироваток до конъюгатів мікотоксинів з бичачим сироватковим альбуміном. Біологічні методи застосовуються у тих випадках, коли відсутні хімічні методи виявлення мікотоксинів або на додаток до них як підтверджувальні тести. Як тест-об'єкти використовують різні мікроорганізми, курячі ембріони, різні лабораторні тварини, культури кліток і тканин.
Пример. Ранним августовским утром 1961 г. сотни обезумевших птиц (ранее безобидные буревестники) атаковали приморский город Капитола в американском штате Калифорния. Четверть века спустя, зимой 1987 года, на острове Принца Эдуарда у североатлантического побережья Канады случилась другая загадочная история: более сотни человек стали жертвами сильнейшего пищевого отравления. Оказалось, что все пострадавшие употребляли в пищу голубые мидии. Практически у всех наблюдались симптомы расстройства психики, пациенты проявляли бесконтрольную агрессивность. Более чем у четверти других жертв оказалась нарушена кратковременная память. Позже выяснилось, что оба случая — результат воздействия одного и того же токсического агента.
Д ля
выяснения всех обстоятельств произошедшего,
а также для предотвращения подобных
случаев Канадский департамент рыболовства
поручил группе морских биологов и
химиков выделить и идентифицировать
токсический агент.
ля
выяснения всех обстоятельств произошедшего,
а также для предотвращения подобных
случаев Канадский департамент рыболовства
поручил группе морских биологов и
химиков выделить и идентифицировать
токсический агент.
Первоначальное исследование мидий на наличие известных бактериальных и вирусных патогенов не привело никчему. Тесты на тяжёлые металлы и пестициды также оказались отрицательными. В состав образцов, взятых для анализа, входили тысячи различных химических соединений. Как можно из такой сложной смеси изолировать один компонент, при этом не зная ничего о нем? В качестве теста были выбраны мыши. После введения небольших количеств исследуемого образца в случае присутствия в нём токсина у подопытных животных наблюдалась неврологическая реакция.
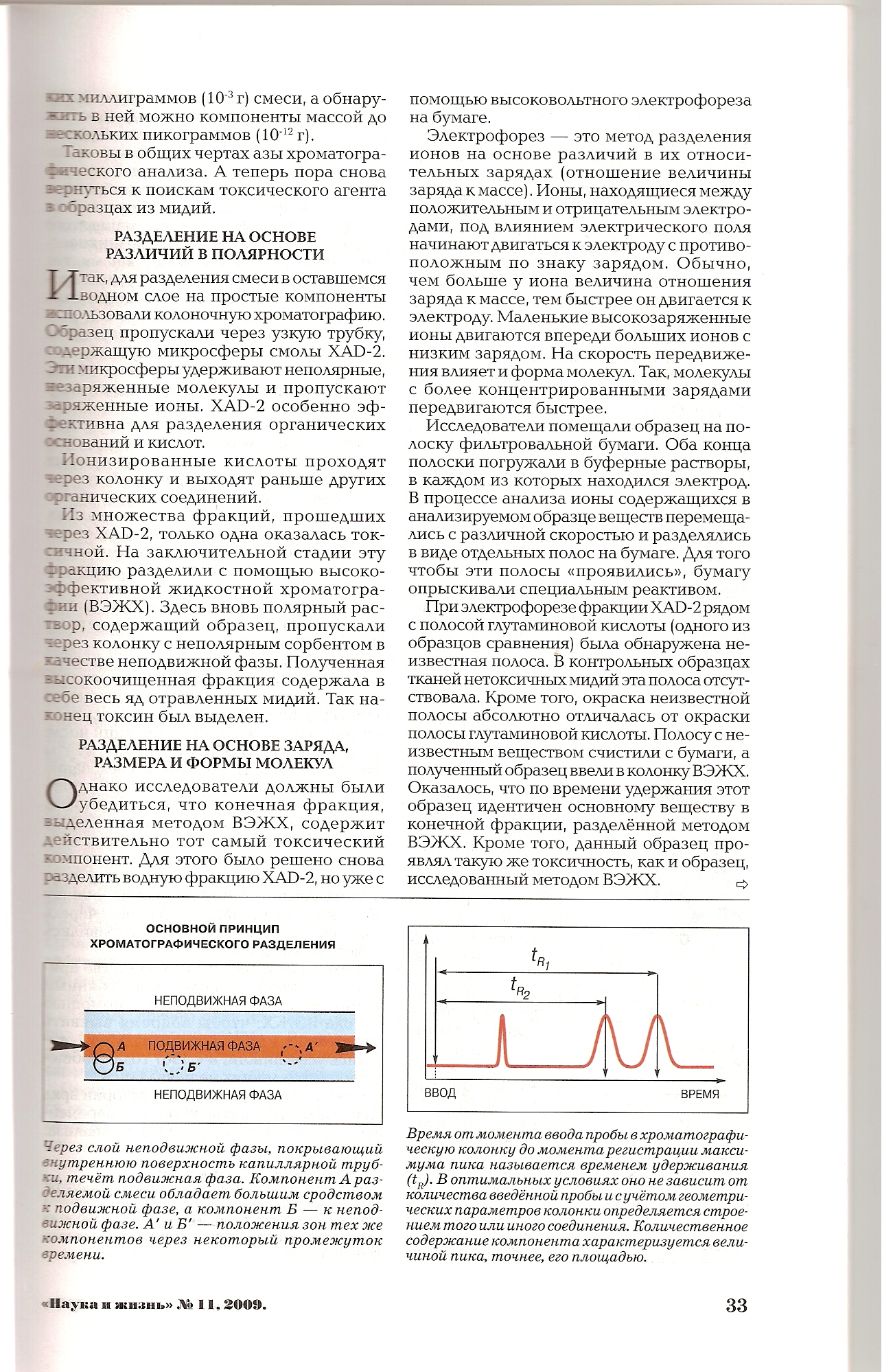
Для разделения сложных компонентов в отравленных образцах тканей мидий учёные использовали стандартные физико-химические методы. Обработке подвергались как токсичные, так и нетоксичные образцы мидий (для последующего сравнительного анализа). Проследим за всеми шагами процесса, изображённого на схеме, и исследования проходили по схеме:
РАЗДЕЛЕНИЕ НА ОСНОВЕ РАСТВОРИМОСТИ И ЛЕТУЧЕСТИ
На первых трёх стадиях согласно общей исследователи использовали экстракцию и упаривание. Чтобы предотвратить возможное разрушение искомого соединения экстракцию проводили при комнатной температуре водным раствором метанола. Мыши проявляли на метанольньй экстракт ту же неврологическую реакцию, что и на исходные образцы устриц. Затем экстракт концентрировали упариванием. Сконденсированный пар был нетоксичен, а вот полученный остаток давал необходимую реакцию у мышей. Стало ясно, что яд — вещество нелетучее.
Была проведена вторая экстракция. Концентрированный экстракт встряхивали со смесью дихлорметана и воды. Эти растворители не смешиваются и образуют два раздельных слоя. В дихлорметановой фракции обнаружили окрашенные вещества — пигменты водорослей. Пигменты не ядовиты и дихлорметановая фракция дала отрицательный результат на подопытных мышах. А вот в водном слое токсин присутствовал.
Для разделения смеси в оставшемся водном слое на простые компоненты использовали колоночную хроматографию. Образец пропускали через трубку, содержащую сорбент, который удерживает неполярные (незаряженные молекулы) и пропускает заряженные ионы. Сорбент (Смола ХАЭ-2) эффективен для разделения органических оснований и кислот. Ионизированные кислоты проходят через колонку и выходят раньше других органических соединений. Из множества фракций, прошедших через колонку, только одна оказалась токсичной. На заключительной стадии эту фракцию разделили с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ). Здесь вновь полярный раствор, содержащий образец, пропускали через колонку с неполярным сорбентом в качестве неподвижной фазы. Полученная высокоочищенная фракция содержала в ебе весь яд отравленных мидий. Так наконец токсин был выделен.
РАЗДЕЛЕНИЕ НА ОСНОВЕ ЗАРЯДА, РАЗМЕРА И ФОРМЫ МОЛЕКУЛ
Исследователи должны были убедиться, что конечная фракция содержит тот самый токсин. Для этого разделяли водную фракцию с помощью электрофореза на бумаге. В процессе анализа образовавшиеся ионы веществ анализируемого бразца перемещались с различной скоростью и разделялись в виде отдельных полос на бумаге. Для того чтобы эти полосы «проявились», бумагу опрыскивали специальным реактивом. Рядом с полосой глутаминовой кислоты (одного из образцов сравнения) была обнаружена неизвестная полоса. В контрольных образцах тканей нетоксичных мидий эта полоса отсутствовала. Полосу с неизвестным веществом счистили с бумаги, а полученный образец ввели в колонку ВЭЖХ. По времени удержания этот образец идентичен основному веществу в конечной водной фракции и проявлял токсический эффект.
идентификация токсина по заряду и массе
На заключительном этапе предстояло определить химическую формулу и молекулярную массу выделенного токсина. С помощью масс-спектрометрии учёные нашли молекулярный вес (312 г/моль) и молекулярную формулу (С15Н21гТО6) выделенного токсина. Спектроскопический анализ выявил присутствие двойных связей и спектров, характерных для аминогруппы. А при сравнении спектров вещества со спектрами в международной базе данных соединение было идентифицировано как домоевая кислота.
Некоторые учёные настаивали на том, что домоевую кислоту красных водорослей используют как средство народной медицины от кишечных паразитов. По всей вероятности, безобидное в небольших концентрациях вещество в больших дозах-проявляло выраженную токсичность. Домоевая кислота—своеобразный «троянский конь» в мире молекул. Нервные клетки ошибочно принимают её за молекулы глутаминовой кислоты, и эта ошибка становится для них смертельной.
|
|
|
|
|