
- •Промышленный органический синтез
- •1. Сырье промышленности органического синтеза
- •2. Процессы органического синтеза
- •3. Синтез метилового спирта
- •4. Производство этилового спирта
- •5. Производство ацетилена и его переработка
- •6. Производство капролактама
- •6.1. Структурная схема производства капролактама из бензола
- •6.2. Физико-химические основы и технологическая схема
- •7. Производство стирола
- •Производство формальдегида окислительным дегидрированием метанола
- •Производство формальдегида окислением метанола
6. Производство капролактама
Капролактам (лактам -аминокапроновой кислоты, 2-оксо-гексаметиленимин) представляет бесцветное кристаллическое вещество с
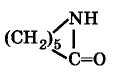
Температура вспышки капролактама составляет 135 оС, температура самовоспламенения 400°С. Капролактам раздражает кожу, ПДК равна 10 мг/м3. Транспортируется и хранится в твердом состоянии в мешках, или в виде расплава в цистернах с обогревом в атмосфере азота.
Капролактам получают различными методами из ароматического (бензол, толуол, фенол) и неароматического (циклогексан, фурфурол, ацетилен, окись этилена) сырья. Во всех методах промежуточным продуктом является циклогексаноноксим, изомеризацией которого получается капролактам. Промышленное значение имеют следующие методы производства циклогексаноноксима.
1. Из фенола через циклогексанол с последующим его дегидрированием до циклогексанона (фенольный метод):
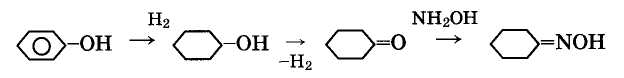
2. Из толуола через бензойную кислоту с последующим гидрированием ее до циклогексанкарбоновой кислоты и обработкой последней нитрозилсерной кислотой (толуольный метод):
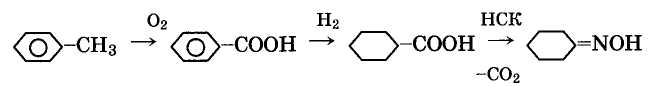
3. Из анилина через циклогексиламин с последующим отщеплением аммиака при действии воды (анилиновый метод):
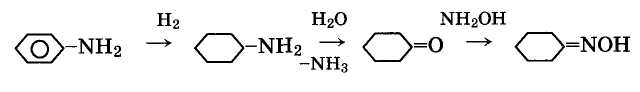
4. Из циклогексана, выделенного из нефтяного сырья, или полученного гидрированием бензола, следующими методами:
— окислением воздухом через циклогексанол и циклогексанон:
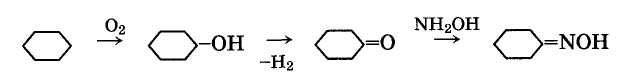
— фотонитрозированием хлористым нитрозилом:
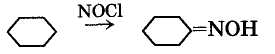
— нитрованием через нитроциклогексан с последующим восстановлением до нитрозоциклогексана (нитроциклогексановый метод):
 HNO3
H2
H2
HNO3
H2
H2
 –NO2
–NO2
=NOH
–NO2
–NO2
=NOH
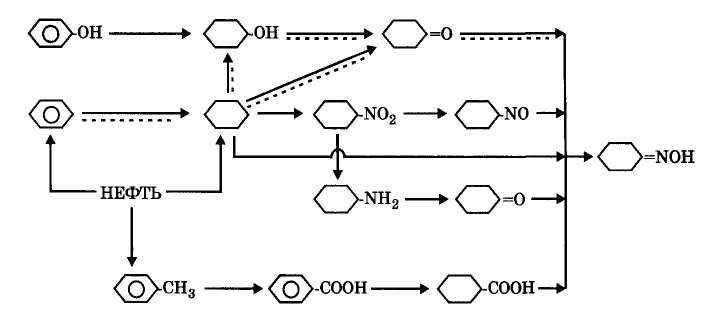
Рис. 14.10. Взаимосвязь промышленных методов производства циклогексаноноксима из различного сырья
Из этих методов наиболее распространенным является бензольный (в схеме на рис. 14.10 показан пунктиром). По данным 1985 года из всего мирового производства капролактама в 2,7 млн. т из бензола было получено 83,5%, из фенола 12,0% и из толуола 4,5% . По сравнению с фенольным методом бензольный метод отличается более низкой стоимостью сырья, меньшим числом стадий и меньшим расходом неорганических реагентов. Поэтому себестоимость капролактама, полученного бензольным методом, составляет 85% от себестоимости продукта, производимого из фенола.
Капролактам используют главным образом в качестве мономера для производства поликапролактама, перерабатываемого в капроновое волокно и полиамидные пластические массы. Незначительное количество капролактама применяется в качестве полупродукта для получения незаменимой аминокислоты L-лизина (а,е-диаминокапроновая кислота).
История. Капроновая кислота СН3(CH2)4СООН была выделена в 1817— 23 гг. М. Шеврелем в процессе систематического изучения жиров. Синтез и полимеризация -капролактама были впервые осуществлены в конце XIX столетия. Промышленное производство -капролактама как мономера для получения капронового волокна было организовано на основе исследований В. Карозерса (1930 г.) и Шлака (1940 г.) в конце 40-х годов по фенольному методу. В последующие годы были внедрены в промышленность методы производства капролактама фотонитрозированием (1951 г.), из циклогексанона через капролактон (1966 г.) и другие.
На основе работ З.А. Роговина, И.Л. Кнунянца, А.А. Стрепихеева, Э.В. Хаита и др. в 1949 г. на Дзержинском химическом комбинате создается первое в стране производство капролактама из фенола. В 1961—65 гг. подобные производства строятся на химических заводах в Чернигове, Рустави, Курске, Кемерово и Барнауле. В 1963 г. на Лисичанском химическом комбинате организуется производство капролактама из бензола через циклогексан. В период 1967—77 гг. создаются новые производства капролактама более экономичным методом прямого окисления циклогексана до циклогексанона, который к 1977 г. становится преобладающим.
