- •Промышленный органический синтез
- •1. Сырье промышленности органического синтеза
- •2. Процессы органического синтеза
- •3. Синтез метилового спирта
- •4. Производство этилового спирта
- •5. Производство ацетилена и его переработка
- •6. Производство капролактама
- •6.1. Структурная схема производства капролактама из бензола
- •6.2. Физико-химические основы и технологическая схема
- •7. Производство стирола
- •Производство формальдегида окислительным дегидрированием метанола
- •Производство формальдегида окислением метанола
3. Синтез метилового спирта
Метиловый спирт (метанол) — важное соединение для получения, главным образом, формальдегида а также - диметилсульфата, диметилтерефталата метилацетата, диметилформамида, аитидетонационных смесей (тетраметилсвинец), ингибиторов, антифризов, метиламина, метилового эфира акриловой кислоты, лаков, красителей и других продуктов. В чистом виде применяется в качестве растворителя и может быть использован как высокооктановая добавка к моторному топливу.
Синтез метилового спирта по физикохимическим условиям его проведения и по технологическому оформлению аналогичен процессу синтеза аммиака. Синтез-газ, как и азотоводородную смесь, можно получать конверсией генераторных газов или природного газа. При синтезе метанола, как и при синтезе аммиака, взаимодействие смеси тщательно очищенных газов происходит при высоких давлении и температуре в присутствии катализаторов. И, наконец, из-за малого выхода конечных продуктов и тот и другой процессы являются циклическими, причем реакцию никогда не вёдут до полного превращения. Поэтому оба синтеза ведут на аналогичных установках, которые монтируют в составе одного завода. Для синтеза берут смесь газов при соотношении СО и Н2 от 1:4 до 1:8. Процесс ведут при 350 - 400 оС и 2∙107 - 3∙107 Н/м2 в присутствии смешанного цинко-хромового катализатора ZnO+Сr2О3. Основная реакция процесса
СО + 2Н2 = СН3ОН + 111 кДж
Одновременно, особенно при уменьшении давления или увеличении температуры сверх оптимальной могут протекать и следующие побочные реакции
СО + 3Н2 = СН4 + Н2О + 209 кДж (а)
2СО + 2Н2 = СН4 + СО2 + 252 кДж (б)
2СО = СО2 + С (в)
СО + Н2 = СН2О + 8,4 кДж (г)
2СН3-ОН = СН3-О-СН3 + Н2О (д) (диметиловый эфир)
СН3-ОН + nСО + 2nН2 = СН2(СН2)nОН + nН2О (е)
высшие спирты
СН3-ОН + Н2 = СН4 + Н2О (ж)
Количество тех или иных побочных соединений в продукциоиной смеси зависит не только от температуры и давления, но и состава исходной газовой смеси, селективности и состояния катализатора. Наиболее существенной примесью как правило является метан. По сравнению со всеми побочными процессами (а)—(ж) получение метилового спирта идет с максимальным уменьшением объема, поэтому в соответствии с принципом Ле-Шателье повышение давления двигает равновесие в сторону образования метилового спирта. Так как процесс экзотермичен, то при повышении температуры равновесие сдвигается влево и равновесная степень превращения синтез-газа в метиловый спирт уменьшается. В то же время при недостаточно высоких температурах скорость процесса чрезвычайно мала. Поэтому в промышленности процесс ведут в узком интервале температур с колебаниями в 20-30 °С.
Фактические выходы всегда ниже равновесных вследствие недостаточной избирательности применяемых катализаторов. Каталитическую способность для реакции синтеза метанола проявляют многие металлы. В промышленности используется цинк-хромовый катализатор, который получается осаждением оксидов цинка и хрома при соотношении ZnO:Сr2О3 ≈ 2:1. Катализатор восстанавливают в токе того же газа. Длительность работы такого катализатора без регенерации колеблется от 4 до 6 месяцев. Общая скорость реакции синтеза определяется адсорбцией водорода.
Температурная зависимость константы скорости прямой реакции описывается уравнением Аррениуса и соответствует энергии активации Е = 100 кДж/моль.
Интервал оптимальных температур соответствующих наибольшему выходу продукта определяется активностью катализатора, объемной скоростью газовой смеси и давлением. Для цинк-хромового катализатора при давлениях около 5∙106—25∙106 Н/м2 и объемных скоростях 20 000—40 000 ч-1 оптимальные температуры колеблются в пределах 360-380 0С. На низкотемпературных катализаторах, например на медь-цинк-алкалюминиевых катализаторах, используемых при 220-280 °С, процесс осуществляется при более низких давлениях 4∙106—10∙106 Н/м2.
В производстве процесс синтеза осуществляется при объемных скоростях 20 000— 40 000 ч-1 и выход метанола составляет около 4% за один проход. При увеличении объемной скорости до 100 000 ч-1 степень превращения исходной смеси за один проход уменьшается, но при циклической схеме с рециркуляцией газов количество полученного метилового спирта возрастает, так как степень превращения снижается медленнее, чем увеличивается объемная скорость.
Технологическая схема производства метилового спирта представлена на рис 14.2. Исходная смесь газов после предварительной очистки от примесей сжимается пятиступенчатым компрессором до 25106 Н/м2. После каждой ступени сжатия установлены холодильник (не показанные на схеме), которые отбирают тепло сжатия. Затем газовая смесь смешивается в смесителе с циркуляциовным газом и, пройдя фильтр для очистки от масла, поступает в трубное пространство теплообменника, где нагревается примерно до 220 °С за счет тепла реакционных газов и далее направляется в колонну синтеза (высота 12-18 м, внутренний диаметр 0,8-1,2 м, толщина стенок 0,09-0,1 м).
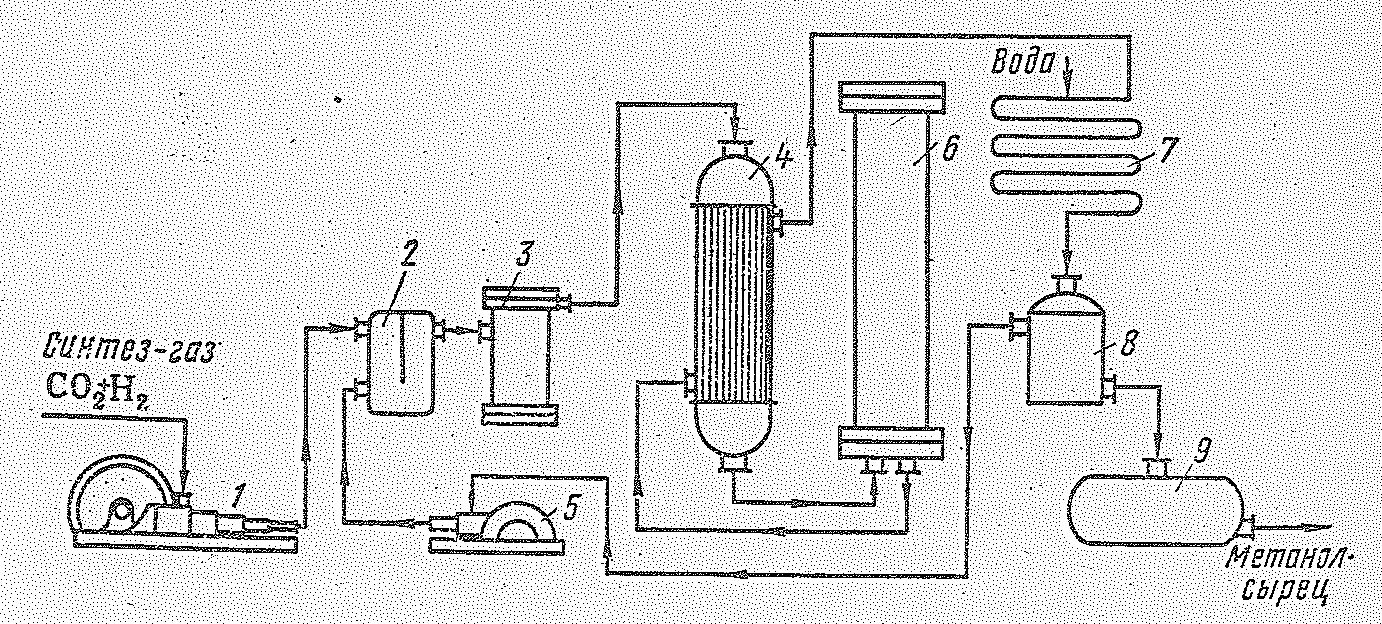
Рис. 14.2. Схема установки для синтеза метилового спирта из оксида углерода и водорода: 1 - компрессор; 2 - смеситель; 3 - фильтр; 4 - трубчатий теплообменник; 5 - циркуляционный компрессор; 6 колонна синтеза; 7 - холодильник-конденсатор; 8 – сепаратор; 9 - сборник спирта-сырца.
|
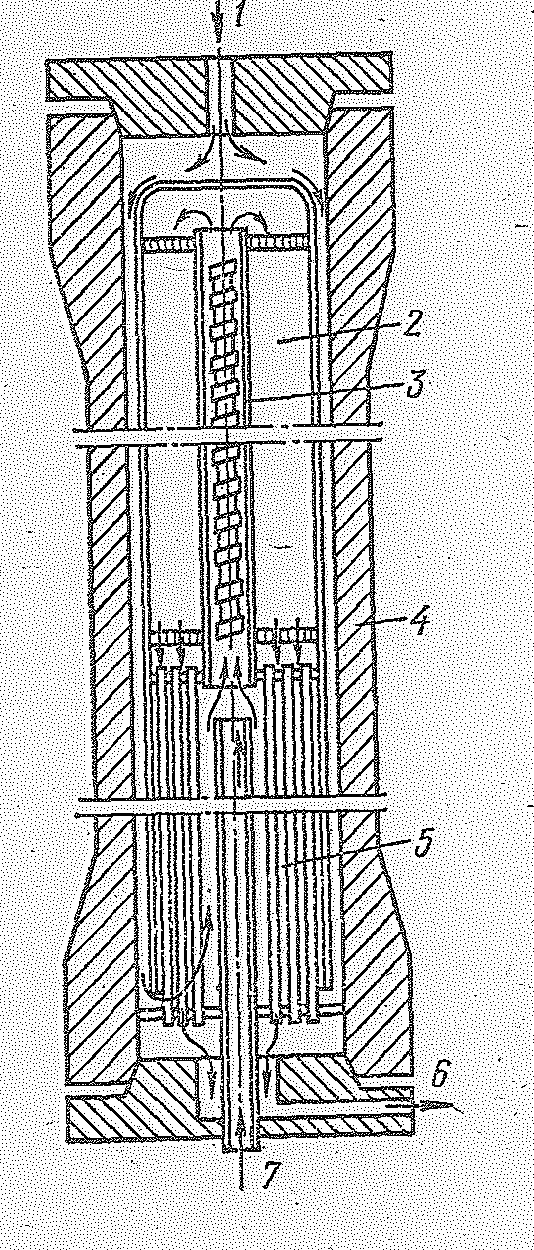
Рис. 14.3. Схема колонны синтеза метанола: 1 - вход основного газа; 2 - катализаторная коробка; 3 - электроподогреватель; 4 - корпус колонны; 5 - теплообменник; 6 - выход газа; 7 - вход байпасного газа. |
Требуемая температура в колонне поддерживается за счет тепла реакции, часть которого отбирает идущая по теплообменным трубкам исходная газовая смесь, поступающая затем в катализаторную массу. При необходимости регулирования температуры в колонну вводят холодную смесь тазов.
Колонны синтеза различаются по типу насадки. В полочной колонне катализатор расположен на нескольких полках и газ последовательно проходит один слой за другим. На рис. 14.3 приведена схема колонны синтеза, в которой в одном корпусе совмещены катализаторная коробка, электроподогреватель и теплообменник. Синтез-газ вводится сверху и проходит по кольцевому пространству между корпусом колонны и коробкой. Затем газ поступает в межтрубное пространство теплообменника, где подогревается за счет тепла контактных газов, проходящих по трубкам теплообменника. В колонне такого типа лучше осуществляется теплообмен и тем самым обеспечивается приближение к оптимальной температуре. Колонна работает в режиме, близком к идеальному вытеснению. Контактные газы выходят из нижней части колонны и, отдав свое тепло исходной газовой смеси в теплообменнике, направляются через водяной ходильник-конденсатор в сепаратор. Здесь полученный спирт-сырец (концентрация 96%) отделяется от непрореагировавшего газа, который циркуляционным компрессором дожимается до давления исходного газа и направляется в смеситель, а метиловый спирт поступает в сборник спирта-сырца.
В связи с тем, что в циркулирующей газовой смеси скапливаются различные примеси и продукты побочных реакций (метан, азот, двуокись углерода к др.), ее периодически обновляют, сжигая часть возвращаемого газа. Для получения 1 т метилового спирта расходуется примерно 700 м3 СО и 1400-2000 м3 Н2 (из 1 м3 синтез-газа газа образуется около 400 г спирта т. е. выход составляет от 84 до 87% от теоретического).
Окись углерода реагирует с углеродистой сталью, образуя пектакарбокил железа Fе(СО)5, который разлагаясь на катализаторе, быстро покрывает его слоем дисперсного железа, усиливающего побочные реакции образования метана, что, в свою очередь нарушает оптимальный температурный режим. Для предотвращения карбонильной коррозии стенки колонны и некоторые другие детали футеруются медью или выполняются из высоколегированной стали. Полученный метанол-сырец очищают от сложных эфиров, высших спиртов, пентакарбонила железа, что в сочетании с последующей ректификацией позволяет получить чистый метиловый спирт.
Для разогрева газовой смеси в пусковой период внутри колонны синтеза вмонтирован электроподогреватель. Изменяя условия синтеза: температуру, давление, соотношение СО и Н2 в исходной смеси, состав катализатора - можно получить не только метиловый, но и высшие спирты, альдегиды, кетоны, эфиры, органические кислоты, предельные и непредельные углеводороды любой длины цепи, вплоть до твердых парафинов, но преимущественно неразветвленной структуры. Исходная смесь газов должна быть тщательно очищена от вредных примесей: сернистых соединений, смол и пыли.