
- •Введение
- •Теоретическая часть
- •1. Диаграммысостояния и физико-химический анализ
- •2. Природа и возможное число конденсированных фаз.
- •1. Чистые компоненты, образующие систему.
- •3. Твердые растворы (фазы переменного состава).
- •3. Применение правила фаз и принцип соответствия
- •4. Линии ликвидуса и солидуса и принцип непрерывности
- •5. Химические соединения и характер их плавления
- •6. Поля гетерогенности и правило отрезков
- •7. Линии безвариантных равновесий и изотермические превращения с участием трех фаз
- •8. Изменение фазового состояния сплава
- •Формулировка задания
- •Данные к задаче 1
- •Данные к задаче 2
- •Данные к задаче 2
- •Данные к задаче 3
- •Данные задаче 3
- •Расчет ветвей ликвидуса в простейшей системе с эвтектическим преврашением и определение теплоты плавления растворителя Пример расчета задачи №2
- •Требования к оформлению задания
- •Расчетно-графическое задание №2
- •Библиографический список
Министерство образования и науки Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования Магнитогорский государственный технический университет им. Г.И. Носова
КАФЕДРА ХИМИЧЕСКОЙ ТЕХНОЛОГИИ НЕМЕТАЛЛИЧЕСКИХ МАТЕРИАЛОВ И ФИЗИЧЕСКОЙ ХИМИИ

ФАЗОВЫЕ РАВНОВЕСИЯ В ДВУХКОМПОНЕНТНЫХ МЕТАЛЛИЧЕСКИХ СИСТЕМАХ
Методические указания к выполнению расчетно-графического задания №2 по дисциплине “Физическая химия” для студентов специальностей 110100, 110400, 110600
Магнитогорск
2007
![]()
Составитель Э.В.Дюльдина
Диаграммы состояния двухкомпонентных систем: Методические указания к выполнению расчетно-графического задания №2 по дисциплине “Физическая химия” для студентов специальностей 110600, 110400, 110100. Магнитогорск: МГТУ 2006.29 с.
Введение
Инженеру, специализирующемуся в области металловедения и ВВЕДЕНИЕ
Инженеру, специализирующемуся в области металловедения и термической обработки металлов, необходимо ориентироваться в громадном количестве сплавов, используемых в настоящее время в технике. Он должен знать, как связаны свойства сплавов с их структурой и как методами термической обработки обеспечить необходимую структуру, а значит и свойства металлических изделий.
Первый этап на пути приобретения этих знаний — знакомство с Диаграммами состояния металлических систем и методом их анализа.
Диаграммы состояния смешанных систем строят в координатах температура - состав. В ряде случаев, а именно: для металлов, ограниченно растворимых друг в друге, обладающих полиморфизмом и дающих несколько химических соединений, диаграммы состояния сложны. Однако все они (и простые, и сложные) содержат одни и те же геометрические элементы, чередующиеся в определенной последовательности. Это облегчает анализ любой диаграммы состояния.
Настоящие методические указания помогут студентам научиться "читать " диаграммы состояния систем из двух компонентов и познакомят их с расчетом ветвей ликвидуса в простейшей системе с эвтектическим превращением.
Теоретическая часть
1. Диаграммысостояния и физико-химический анализ
Фазовое равновесие в многокомпонентных системах изучают при помощи физико-химического анализа. В основе этого метода лежит исследование физических зависимостей различных физических свойств смешанных систем от состава.
Частным случаем диаграмм состав - свойство являются диаграммы состояния или фазовые диаграммы. Они выражают зависимость температур равновесных фазовых переходов от состава системы.
По диаграммам состояния можно судить о числе и природе фаз образующихся в системе, и условиях их существования, о температурах начала и конца различных фазовых переходов, совершающихся при изменении температуры, о составах равновесных фаз и количественном соотношении между ними при различных температурах, а также о возможности пластической деформации и термической обработки металлических сплавов.
2. Природа и возможное число конденсированных фаз.
В двухкомпонентных металлических системах конденсированные фазы могут быть жидкими и твердыми.
Жидкие фазы — это расплавы или ненасыщенные растворы одного вещества в другом, т. е. фазы переменного состава. Им на диаграммах состояния удовлетворяют поля. В различных системах общее число жидких фаз может быть разным (рис. 1).
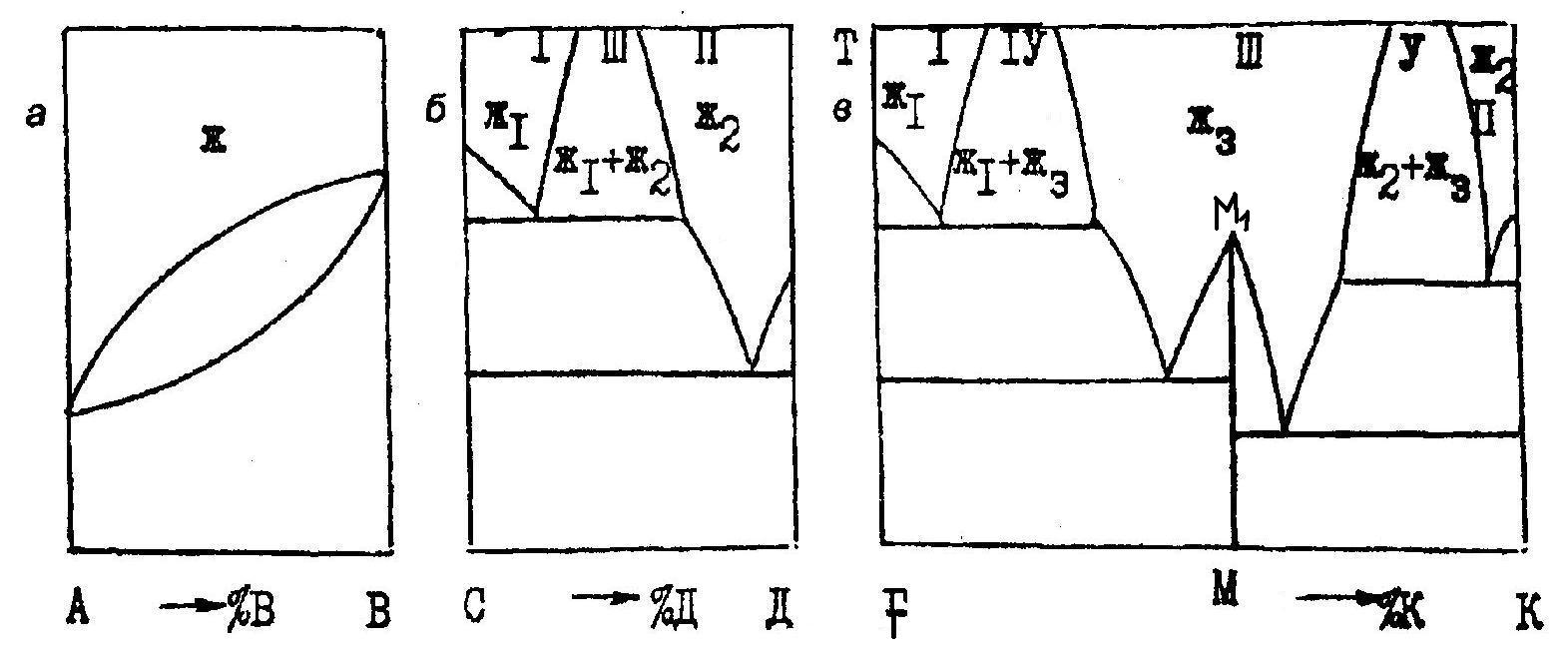
Рис. 1 . Диаграммы состояния систем с различным числом жидких фаз
В системе А-В (рис.1,а) компоненты неограниченно растворимы друг в друге и дают одну жидкую фазу — ненасыщенный раствор из вещества А и В, устойчивый в верхнем поле диаграммы.
В системе С-Д (рис. 1,б) с
ограниченной растворимостью компонентов
две жидкие фазы (Ж1
и Ж2).
Поля их устойчивости I
и II
примыкают к граничным вертикалям и
разделяются областью расслоения III,
где в равновесии присутствуют две
несмешивающиеся жидкости. Каждый из
растворов Ж1
и Ж2
обогащен одним из компонентов,
он и выступает в роли растворителя. В
расплаве
![]() растворитель
— вещество С, а в расплаве Ж2
— вещество Д.
растворитель
— вещество С, а в расплаве Ж2
— вещество Д.
В системе F-К (рис. 1,в) с химическим соединением М жидких фаз три (Ж1, Ж2, Ж3), поля их существования I, II и III разделены двумя областями расслоения IV и V. В расплаве Ж3 преобладает химическое соединение М, оно и является растворителем.
Твердые фазы. Они могут быть трех типов:
