
- •Индивидуальное задание: «Электрохимическое производство щелочи,хлора и водорода»
- •Содержание
- •3.3Структурная схема 24
- •Введение
- •Продукты электролиза раствора NaCl
- •Методы электролиза растворов хлористых солей.
- •2.2 Метод электролиза с ртутным катодом
- •3.1Структурная схема
- •3.2Операторная схема
- •3.3Структурная схема
- •3.5 Функциональная схема
- •Литература
3.1Структурная схема
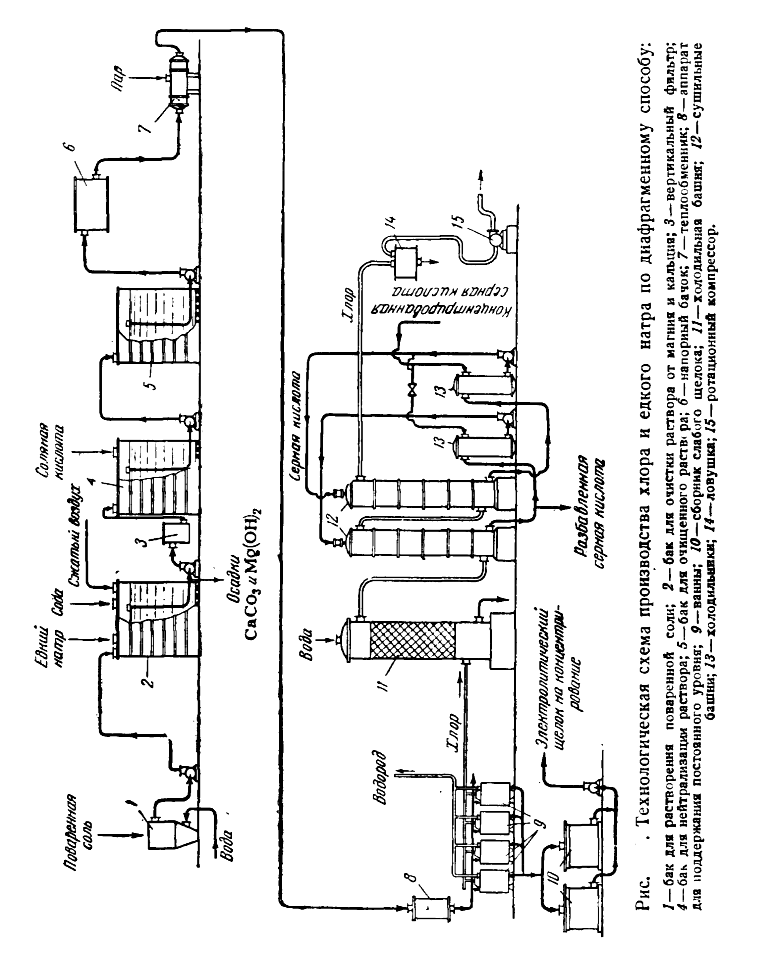
3.2Операторная схема

Растворение NaCl в H2O;
Химическая очистка от Са2+ и Mg2+ путем добавки в него необходимых количеств растворов соды и едкого натра;
Образование нерастворимых осадков CaC03, Mg(OH)2;
Фильтрация;
Нейтрализация остаточной щелочи;
Подогрев глухим паром до 70—80°;
Электролиз очищенного раствора поваренной соли;
Разделение продуктов реакции;
Охлаждение;
10) Сжижение водорода;
11) Охлаждение хлора водой;
12) Осушение хлора;
13) Сжижение хлора;
14) Упаривание слабого щелока;
15) Очистка концентрированного щелока от поваренной соли;
16) Возврат непрориагировавшей поваренной соли в цикл.
3.3Структурная схема
Материальные потоки |
Элементы системы |
L1 – Вода; L2–Концентрированный раствор поваренной соли (305—310 г/л NaCl); L3 –Раствор NaOH; L4 – Раствор Na2CO3; L5–Концентрированный раствор поваренной соли, содержщий нерастворимые осадки CaC03, Mg(OH)2; L6–Концентрированный раствор поваренной соли, отфильтрованный от нерастворимых осадков CaC03, Mg(OH)2; L7 – Раствор HCl; L8–Концентрированный нейтрализованный раствор поваренной соли, L9 – Слабый раствор NaOH; L10 – H2SO4 (95-96%); L11 – H2SO4 (около 78%); L12 – Сжиженный чистый хлор; G1 – Водород; G2 – Хлор; G3 – Охлажденный хлор с содержанием влаги; G4–Очищенный от влаги хлор, с небольшим содержанием серной кислоты. G5 – Полностью очищенный хлор; S1 – Поваренная соль; S2 – Осадок CaC03; S3 – Осадок Mg(OH)2. |
|

3.5 Функциональная схема

Растворение NaCl в H2O;
Химическая очистка от Са2+ и Mg2+ путем добавки в него необходимых количеств растворов соды и едкого натра;
Образование нерастворимых осадков CaC03, Mg(OH)2 и их фильтрация;
Нейтрализация остаточной щелочи;
Подогрев глухим паром до 70—80°;
Электролиз очищенного раствора поваренной соли;
Разделение продуктов реакции;
Охлаждение водорода;
9) Сжижение водорода;
10) Упаривание щелока;
11) Раздиление концентрированного щелока и осадка NaCl (фильтрованием);
12) Охлаждение хлора;
13) Очистка хлора от воды;
14) Сжижение хлора.
Вывод
Сравнение методов электролиза: ванны с ртутным катодом по сравнению с ваннами с диафрагмой имеют как преимущества, так и недостатки. К преимуществам ртутных ванн относится возможность получения едких щелочей в четыре-шесть раз большей концентрации, чем в ваннах с диафрагмой; щелока почти не содержат хлористых солей, не требуют упарки и могут быть применены непосредственно в ряде производств (например, в производстве искусственного шелка, в мыловарении и т. п.). Газообразный хлор получается высококонцентрированный (до 98% С12).
Недостатками метода с ртутным катодом являются: повышенный расход электроэнергии (по сравнению с методом с диафрагмой), обусловленный более высоким потенциалом выделения натрия на ртути, чем водорода на железе; значительные капитальные затраты на приобретение дорогостоящей ртути для первоначальной заливки ее в ванны; небольшие, но неизбежные потери ртути в процессе производства (1 —1,5% от всего количества в год); сложность и дороговизна конструкции ванн; вредные условия труда из-за проникновения ртути в атмосферу и др.
Перечисленными недостатками объясняется значительно меньшее распространение ртутного метода по сравнению с диафрагменным. Ртутный метод значительно менее распространен также вследствие достигнутых в настоящее время успехов по очистке от примесей (главным образом от хлористого натрия) щелоков, получаемых в ваннах с диафрагмой
