
- •«Циклогексан»
- •Химия и технология процессов гидрирования
- •Гидрирование ароматических углеводородов
- •Технология жидкофазного гидрирования
- •Процессы жидкофазного гидрирования классифицируют по нескольким основным признакам.
- •Технологическая схема жидкофазного гидрирования
- •Технологическая схема
- •Структурная схема
- •Функциональная схема
- •Операторная схема
Министерство образования и науки
Донецкий национальный университет
Химический факультет
Реферат
на тему:
«Циклогексан»
Г. Донецк
2010 год
Химия и технология процессов гидрирования
В промышленности основного органического и нефтехимического синтеза широко используют процессы гидрирования углеводородов, кислородсодержащих и азотистых соединений с целью получения главным образом насыщенных углеводородов, кетонов, карбоновых кислот, спиртов и аминов.
Гидрирование ароматических углеводородов
Катализаторами гидрирования ароматических систем могут быть все металлы восьмой группы, но в промышленности применяют главным образом никель на носителях, особенно на Cr2O3. С таким контактом достаточная скорость процесса достигается при 120-2000 С. При этом в отличие от олефинов, необходимо повышенное давление (1-5 МПа) – не только для ускорения реакции, но и для увеличения равновесной степени конверсии, так как термодинамические отношения в этом случае менее благоприятны для гидрирования. Ароматические углеводороды нужно предварительно очищать от соединений серы, являющихся контактными ядрами.
Сравнительная стабильность ароматической системы обуславливает ее меньшую реакционную способность при гидрировании по сравнению с олефинами. Так, относительные скорости гидрирования бензола в ядро, циклоолефина и двойных связей в боковой цепи арилолефина таковы (в условных единицах) :

1 |
150 |
900 |
По этой причине и даже не смотря на последовательно-параллельный тип реакции со ступенчатым насыщением связей
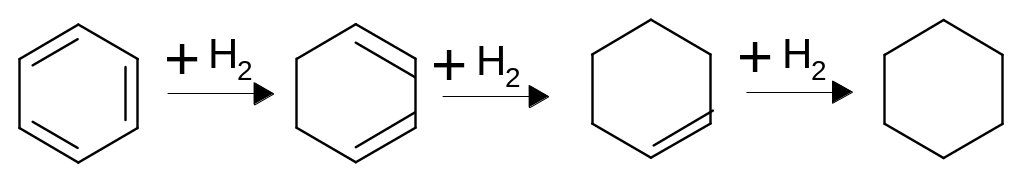
В реакционной массе не обнаруживается циклических олефинов. Однако в специальных условиях из бензола можно получить циклогексен (нагомогенных катализаторах) или циклогексилбензол ( на гетерогенных бифункциональных катализаторах):
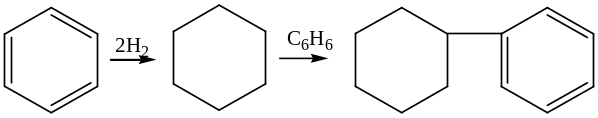
Гомологи бензола гидрируются с меньшей скоротью, чем сам бензол, что является еще одним проявлением дезактивирующего влияния заместителей при гидрируемых связях. При наличии в ароматическом углеводороде ненасыщенной боковой цепи она гидрируется в первую очередь. В присутствии медного катализатора, не катализирующего гидрирование ароматических систем, насыщаются только боковые цепи, а на никелевом при избытке водорода происходит полное гидрирование, например, стирола:
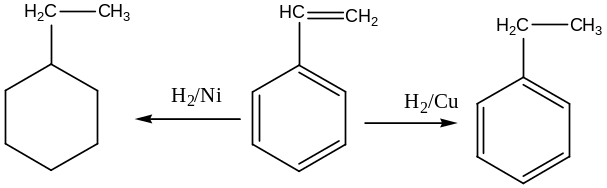
Условия гидрирования ароматических углеродов во многом определяются побочными реакциями гидрогенолиза с расщеплением боковых цепей и циклов. Так, из бензола на никелевом катализаторе при 2900 С образуются метан (до 71 %) и свободный углерод :
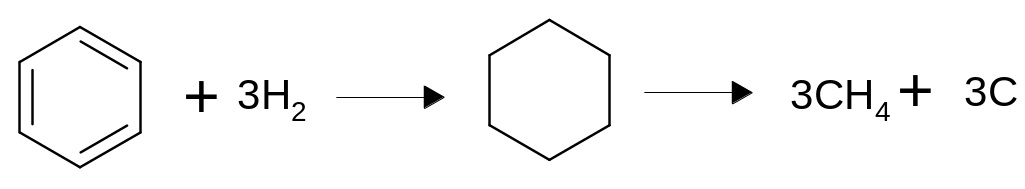
Еще легче расщепляются боковые цепи, особенно более длинные. Например, из н-пропилбензола при гидрировании можно получить не только пропилциклогексан, но также этил- и метилзамещенные, циклогексан и низшие парафиновые углеводороды. Эти побочные реакции определяют верхний предел температуры при гидрировании ароматических углеводородов.
В промышленности процессы гидрирования ароматических углеродов применяют для синтеза нескольких практически важных продуктов, в особенности циклогексана.
Циклогексан С6Н12 (жидкость; т.кип 80,70 С) содержится в небольшом количестве в бензиновых фракциях нефти, и его можно извлекать из легких нефтяных фракций экстрактивной перегонкой, фракционной кристаллизацией. На практике эти методы используют редко. Это объясняется трудностями, связанными с выделением чистого циклогексана из нефтяного сырья. Главным методом получения циклогексана в промышленности является гидрирование бензола:
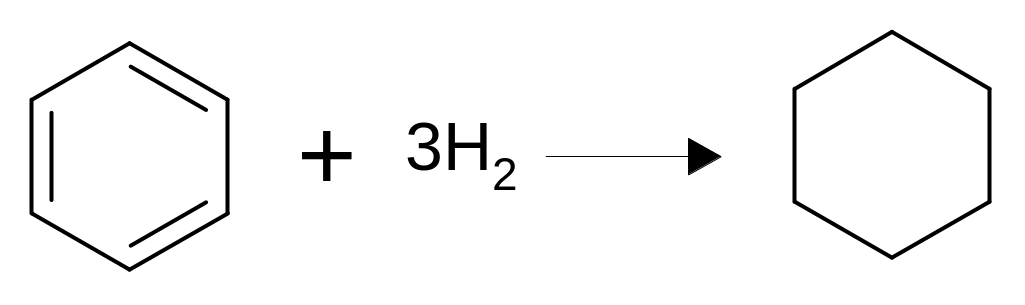
Гидрирование бензола протекает с выделением тепла (ΔН= -49 ккал). Гидрирование бензола проводят при атмосферном давлении, так и при среднем и высоком давлении. Наиболее выгодно в техноэкономическом отношении является, по-видимому, проведение процесса при высоком давлении: при 200-300 атм и 260 – 3600 С. При более низких температурах равновесие обратимой реакции сдвигается вправо, но значительно уменьшается скорость реакции, и поэтому снижается производительность катализатора. Повышение температуры приводит, наряду с ускорением основной реакции, и к ускорению побочной- изомеризации циклогексана в метилциклопентан:

Если исходный бензол не содержит сернистых соединений, синтез циклогексана проводят при 100 атм и 2700 С в присутствии никелевого катализатора (окись никеля, нанесенная на окись алюминия). Через 1л такого катализатора можно пропустить в час 2,7 л бензола и 20 л водорода, сжатого до 200 атм.
Если в исходном бензоле содержатся сернистые соединения, то используют комбинированный катализатор, состоящий из сульфида никеля и сульфида вольфрама. Сульфиды наносят на носитель – активную окись алюминия; однако возможно применение сульфидов без носителя – в этом случае съем продуктов с единицы объема катализатора выше. Сульфидные катализатор, обладая высокой активностью и селективностью, не отравляется сернистыми соединениями. Наоборот, для его нормальной работы необходимо избегать обессеривания, поэтому вместе с исходными реагентами в контактный слой непрерывно вводят в небольших количествах сероуглерод или сероводород.
В последнее время циклогексан приобрел важное значение для производства циклогексанона, капролактама и адипиновой кислоты.
