
- •Дм. 01 Основные химические понятия и законы Руководство по модулю «Основные химические понятия и законы»
- •Ме 1.1 (Занятие № 2)
- •Руководство по ме «Основные химические понятия и законы»
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство по освоению действия ме 1.1 «Составить формулы химических соединений. Применить основные законы химии для составления уравнений химических реакций»
- •Самостоятельная работа
- •Ме 1.2 (Занятие № 3)
- •Руководство по ме «Решение задач»
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство по освоению действия ме 1.2 «Решать задачи»
- •Самостоятельная работа
- •Ме 1.3 (Занятие № 4)
- •Руководство по ме «Зачет № 1»
- •Руководство по оценке действия «Продемонстрировать освоенные действия по дм 01Основные химические понятия и законы»
- •Зачетная работа
- •Ме 2.1 (Занятие № 5)
- •Руководство по ме «Периодический закон и Периодическая система химических элементов д.И. Менделеева»
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство по освоению действия ме 2.1 «Понять структуру Периодической таблицы химических элементов. Сделать лабораторную работу «Моделирование построения Периодической таблицы химических элементов»
- •Инструкция
- •Самостоятельная работа
- •Ме 2.2 (Занятие № 6)
- •Руководство по ме «Строение атома»
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Самостоятельная работа
- •Дм. 03 Строение вещества Руководство по модулю «Строение вещества»
- •Ме 3.1 (Занятие № 7)
- •Руководство по ме «Виды химической связи»
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Самостоятельная работа
- •Ме 3.2 (Занятие № 8)
- •Руководство по ме «Виды химической связи»
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Самостоятельная работа
- •Ме 3.3 (Занятие № 9)
- •6. Заполняется личный дневник студента. Руководство по ме «Металлическая связь. Дисперсные системы»
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Самостоятельная работа
- •Дм. 04 Вода. Растворы. Электролитическая диссоциация Руководство по модулю «Вода. Растворы. Электролитическая диссоциация»
- •Ме 4.1 (Занятие № 10)
- •Руководство по ме «Растворение как физико - химический процесс»
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •3.1 Массовая доля
- •3.2 Молярность раствора
- •Самостоятельная работа
- •Ме 4.2 (Занятие № 11)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Плотность и процентное содержание растворов хлорида натрия.
- •100 Г раствора - 1 г NaCl
- •201,315 Г раствора - х г NaCl
- •Самостоятельная работа
- •Ме 4.3 (Занятие № 12)
- •Руководство по ме «Классифицировать основные классы неорганических веществ с точки зрения теории электролитической диссоциации. Определять сильные и слабые электролиты»
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •1) Молекулярное уравнение:
- •3) Сокращенное ионно-молекулярное уравнение:
- •Самостоятельная работа
- •Дм. 05 Классификация неорганических соединений и их свойства Руководство по модулю «Классификация неорганических соединений и их свойства»
- •Ме 5.1 (Занятие № 13)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Самостоятельная работа
- •Ме 5.2 (Занятие № 14)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Самостоятельная работа
- •Ме 5.3 (Занятие № 15)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Алгоритм написания уравнений реакций гидролиза солей
- •Самостоятельная работа
- •Ме 5.4 (Занятие № 16)
- •Руководство по ме «Контрольная работа»
- •Руководство по оценке действия «Продемонстрировать освоенные действия за I семестр»
- •Контрольная работа
- •Дм. 06 Химические реакции Руководство по модулю « Химические реакции»
- •Ме 6.1 (Занятие № 17)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Самостоятельная работа
- •Ме 6.2 (Занятие № 18)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Ме 6.3 (Занятие № 19)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Ме 6.4 (Занятие № 20)
- •Руководство по ме «Зачет № 2»
- •Руководство по оценке действия «Продемонстрировать освоенные действия по дм 06 Химические реакции»
- •Зачетная работа
- •Дм. 07 Металлы и неметаллы Руководство по модулю «Металлы и неметаллы»
- •Ме 7.1 (Занятие № 21)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Ме 7.2 (Занятие № 22)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Ме 7.3 (Занятие № 23)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •1. Пример:
- •Некоторые качественные реакции на анионы и катионы
- •Дм. 08 Основные понятия органической химии и теория строения органических соединений Руководство по модулю «Основные понятия органической химии и теория строения органических соединений»
- •Ме 8.1 (Занятие № 24)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Ме 8.2 (Занятие № 25)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Основные положения теории химического строения а.М. Бутлерова
- •1. Атомы в молекулах соединяются в определенном порядке в соответствии в соответствии с их валентностью. (Углерод четырехвалентен).
- •2. Свойства веществ зависят не только от их качественного и количественного состава, но и от строения их молекул.
- •3. Свойства веществ зависят от взаимного влияния атомов в молекулах.
- •Дм. 09 Углеводороды и их природные источники Руководство по модулю «Углеводороды и их природные источники»
- •Ме 9.1 (Занятие № 26)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •2. Реакции отщепления (дегидрирование)
- •4. Реакции разложения
- •Ме 9.2 (Занятие № 27)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Задание 3: н аписать уравнения реакций в соответствии со схемой: сн4 с2н4 (- сн2 – сн2)n
- •Ме 9.3 (Занятие № 28)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •1.1 Решив задачу, определим молекулярную формулу первого представителя гомологического ряда алкинов – ацетилена. Решение задач на определение молекулярной формулы веществ
- •Ме 9.4 (Занятие № 29)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Дм. 10 Кислородосодержащие органические соединения Руководство по модулю «Кислородосодержащие органические соединения»
- •Ме 10.1 (Занятие № 30)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Одноатомные спирты.
- •Многоатомные спирты
- •Ме 10.2 (Занятие № 31)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Ме 10.3 (Занятие № 32)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Ме 10.4 (Занятие № 33)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •1. Реагирует с оксидом серебра (I) в аммиачном растворе (реакция “серебряного зеркала”):
- •4. Специфические свойства.
- •Ме 10.5 (Занятие № 34)
- •Руководство по ме «Зачет № 3»
- •Зачетная работа
- •1)Алканов 2)алкинов
- •3)Алкенов 4)аренов
- •1) Бутан 2) бутен 3) бутин 4) бутанол
- •1)Бензина 2) углеводов
- •3) Бутадиена 4) фенола
- •Дм. 11 Азотсодержащие органические соединения. Полимеры Руководство по модулю «Азотсодержащие органические соединения»
- •Ме 11.1 (Занятие № 35)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Номенклатура аминов.
- •2) Взаимодействие с азотистой кислотой:
- •Важнейшие - аминокислоты общей формулы (таблицу переписать в тетрадь)
- •Задание 3: Составить структурные формулы
- •3. Изучим свойства и способы получения аминокислот Свойства аминокислот:
- •Способы получения аминокислот (все уравнения реакций перенести в тетрадь)
- •Химические свойства
- •Ме 11.2 (Занятие № 36)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •2. Изучим конфигурации белков Структура белков
- •1. В образовании какой структуры принимают участие дисульфидные мостики: а) вторичной, б) первичной, в) третичной.
- •Ме 11.3 (Занятие № 37)
- •Контрольная ведомость обучающегося гр. ____________
- •Руководство
- •Качественные реакции органических соединений
- •Ме 11.4 (Занятие № 38)
- •Руководство по ме «Итоговый зачет»
- •Руководство по оценке действия «Продемонстрировать освоенные действия курсу «Химия»»
- •Зачетная работа
Контрольная ведомость обучающегося гр. ____________
Дисциплина: Химия (на базе основного общего образования).
Задача урока:
ФИО студента __________________________________________
Критерий оценки – студент может самостоятельно выполнить следующие действия |
Да/нет |
Если нет, то что студент должен сделать дополнительно |
Дать определение белкам |
|
|
Объяснить конфигурацию белков |
|
|
Составлять химические реакции, доказывающие способы получения белков |
|
|
Назвать химические реакции, доказывающие свойства белков |
|
|
Сделать лабораторную работу «Химические свойства белков» |
|
|
Достижение цели – изучить строение, свойства и биологические функции белков (индивидуальное задание) |
|
|
Результат оценки:
|
||
Подписи оценщиков:
|
Дата проведения оценки: |
|
Руководство
по освоению действия МЕ 11.2 «Изучить строение, свойства и биологические функции белков»
Освоим действие – Изучить строение, свойства и биологические функции белков
Порядок освоения действия: Все определения и уравнения записываем в тетрадь!
1. Дадим определение белкам
Белки - природные полимеры, мономерами которых являются аминокислоты
Вещества белковой природы известны с давних времен. Начало их изучению положено в середине XVIII в. итальянцем Я.Б.Беккари, который предложил углеродную теорию. Через 100 лет ученые пришли к выводу, что белки – главный компонент живых организмов. Затем из белковых гидролизатов были получены продукты расщепления, и возникла гипотеза о том, что белки состоят из остатков аминокислот (А.Я.Данилевский). Над проблемой строения белков долгое время работал Э.Г.Фишер. На основе его работ была создана полипептидная теория строения белков. Было доказано, что в состав белков входят атомы углерода, водорода, кислорода, азота, серы, фосфора и другие.
Элементный состав белков
Элемент |
Содержание, % |
C |
50–55 |
H |
6,5–7,3 |
O |
19–24 |
N |
15–19 |
S |
0,2–2,4 |
Характерной особенностью белков является их многообразие, связанное с количеством, свойствами и способах соединения входящих в их молекулу аминокислот.
2. Изучим конфигурации белков Структура белков
П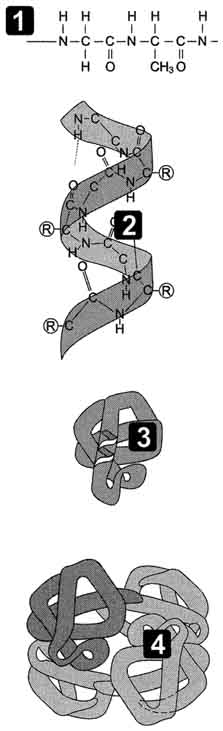 ервичная
структура
ервичная
структура
Первичная структура белка - специфическая аминокислотная последовательность, т.е. порядок чередования - аминокислотных остатков в полипептидной цепи
Вторичная стуктура
Конфигурация полипептидной цепи, т.е. способ скручивания цепи в пространстве за счет водородных связей между группами NH и CO. Одна из моделей вторичной структуры – - спираль
Третичная структура
Трехмерная конфигурация закрученной спирали в пространстве, образованная за счет дисульфидных мостиков –S–S– между цистеиновыми остатками и ионных взаимодействий
Четвертичная структура
Структура, образующаяся за счет взаимодействия между разными полипептидными цепями
3.Изучим способы получения белков
- аминокислоты вступают друг с другом в реакцию поликонденсации, приводя к амидам кислот. Продукты такой конденсации называются пептидами или белками.
При взаимодействии двух аминокислот образуется дипептид:
H2N– |
H I CH– |
O II C–OH + H–NH– |
CH3 I CH– |
O II C–OH |
|
глицин |
аланин |
||
H2N– |
H I CH– |
O II C–NH– |
CH3 I CH– |
O II C–OH + H2O |
|
глицилаланин |
|
||
Связь – O II C–NH – называется пептидной связью.
Задание 1: Напишите уравнение реакции получения дипептида, используя формулы глицина и аланина
4. Изучим химические свойства белков:
Денатурация — разрушение вторичной и третичной структуры белка, обусловленное воздействием кислот, щелочей, нагревания, радиации и т.д. Первичная структура белка при денатурации сохраняется. Денатурация может быть обратимой (так называемая, ренатурация) и необратимой.
Качественные реакции на белок:
биуретовая реакция: фиолетовое окрашивание при обработке солями меди в щелочной среде (дают все белки),
ксантопротеиновая реакция: желтое окрашивание при действии концентрированной азотной кислоты, переходящее в оранжевое под действием аммиака (дают не все белки),
выпадение черного осадка (содержащего серу) при добавлении ацетата свинца (II), гидроксида натрия и нагревании.
Гидролиз белков — при нагревании в щелочном или кислом растворе с образованием аминокислот.
5. Лабораторная работа «Химические свойства белков»
Цель работы: Изучить химические свойства белков. Провести качественные реакции на обнаружение белка в пшеничной муке и шерстяной нити.
Задание:
Провести реакцию денатурации белка.
Провести качественные реакции на белки
Результаты работы оформить в таблице
№ п/п |
Исходные вещества (формулы) |
Наблюдения |
Выводы |
Оборудование:
Штатив с пробирками, химический стакан, держатель, спиртовка
Вещества:
Растворы куриного белка (альбумина), сульфата меди, гидроксида натрия, азотная кислота (концентр.)
Ход работы:
Опыт 1. Свертывание белков.
Налейте в пробирку 1 мл водного раствора белка и нагрейте в пламени спиртовки до кипения. Опишите ваши наблюдения и сделайте вывод о процессе, который произошел с белком.
Опыт 2. Биуретовая реакция.
а) Внесите в пробирку 1 мл раствора белка, 1 мл раствора щелочи и 3-4 капли раствора сульфата меди. Обратите внимание на цвет раствора, опишите свои наблюдения и сделайте вывод.
Опыт 3. Ксантопротеиновая реакция.
а) Внесите в пробирку 1 мл раствора белка и 3-4 капли НNO3(конц.). Отметьте цвет образовавшегося осадка.
6. Проверим достижение цели - изучить строение, свойства и биологические функции белков
Самостоятельная работа:
Вариант 1
1.Что является мономерами белков?
2.Назовите качественные реакции на белки
Вариант 2
1. Перечислите биологические функции белков
2. Составьте уравнение взаимодействия глицина и фенилаланина
Вариант 3
1. При каких условиях происходит денатурация белков?
2. Дайте краткую характеристику белков:
1) органическими или неорганическими веществами являются белки;
2) какую структуру — моно- или полимерную — имеют молекулы белков;
3) что выступает мономером в молекуле белка;
4) какие функции в организме выполняют белки;
5) в чем заключается ферментативная функция белков.
Вариант 4
