
- •Содержание
- •Глоссарий 7
- •Конспект лекционных занятий
- •3. Практические занятия
- •4. Лабораторные занятия
- •5. Самостоятельная работа студентов
- •7 Экзаменационные вопросы 181
- •8 Технические средства обучения 182
- •Список рекомендуемой литературы 182
- •1. Глоссарий
- •2 Конспект лекционных занятий модуль 1 Лекция № 1. Перспективы развития технологии органических веществ (2 часа)
- •0,5 О2 носн2-сн2он
- •О носн2-сн2nh2
- •Лекция № 2. Физико-химические основы термического крекинга
- •Лекция № 3. Физико-химические основы каталитического крекинга
- •Лекция № 4. Физико-химические основы каталитического риформинга
- •Лекция № 5. Физико-химические основы гидрогенизационных процессов
- •Лекция № 7. Химизм и механизм технологических процессов переработки нефтяных газов
- •Лекция № 8 Технологическое оборудование и технологическое оформление основных аппаратов процессов переработки органических веществ
- •Лекция № 10 Теоретические основы очистки нефтяных фракций
- •Лекция № 11 Адсорбционные и каталитические методы очистки
- •Лекция № 12 Очистка с применением избирательных растворителей
- •Лекция № 13 Депарафинизация масел и дизельных фракций
- •3. Практические занятия
- •Практическое занятие №1
- •Тема: Расчетные методы определения физико-химических свойств
- •И состава нефти и нефтепродуктов
- •Задачи для решения
- •Практическое занятие №2 Тема: Расчетные методы вычисления материального баланса процесса термического крекинга
- •Составление материального баланса
- •Задачи для решения
- •Практическое занятие №3 Тема: Составление материального баланса процесса каталитического крекинга
- •Задачи для решения
- •Практическое занятие №4 Тема: Составление материального баланса процесса каталитического риформинга
- •Задачи для решения
- •Практическое занятие №5 Тема: Расчетные методы вычисления материального баланса гидрогенизационных процессов
- •Задачи для решения
- •Практическое занятие №6 Тема: Расчетные методы вычисления материального баланса процесса полимеризационных процессов
- •Задачи для решения
- •Практическое занятие №7 Тема: Задачи и упражнения по составлению уравнений химических реакций, протекающих при алкилировании и изомеризации с указанием механизма ее протекания
- •Задачи для решения
- •Практическое занятие №8 Тема: Технологический расчет основных аппаратов установок переработки органических веществ
- •Число тарелок
- •Практическое занятие №9 Тема: Приближенные методы построения линии однократного испарения (ои)
- •Задачи для решения
- •Практическое занятие №10 Тема: Решение задач по теоретическим основам процесса очистки нефтяных фракций
- •Задачи для решения
- •Практическое занятие №11 Тема: Решение задач по депарафинизации нефтяных фракций
- •Задачи для решения
- •Практическое занятие №12 Тема: Решение задач по закономерностям получения гомогенных растворов
- •Задачи для решения
- •4. Лабораторные занятия лабораторная работа №1 Тема: Термический крекинг (пиролиз) углеводородов и составление материального баланса опыта
- •Описание установки и методика проведения работы
- •Лабораторная работа №2 Тема: Каталитический крекинг углеводородов и составление материального баланса опыта
- •Проведение работы
- •Оформление результатов работы
- •Методика проведения эксперимента
- •Приготовление алюмохромового оксидного катализатора
- •Методика выполнения работы
- •Лабораторная работа №5 Тема: Полукоксование
- •Описание установки и методика проведения работы
- •Лабораторная работа №6 Аппараты установок термических и каталитических процессов. Тема: Методы разделения и анализа продуктов реакций
- •Методика проведения работы
- •Методика проведения работы
- •Лабораторная работа №7 Тема: Разгонка нефти на ректификационном аппарате
- •Лабораторная работа №8 Тема: Очистка сырой нефти от влаги и механических примесей
- •Определение сухого остатка
- •Методика определения
- •Прокаленный остаток
- •Методика определения
- •Лабораторная работа №9 Тема: Депарафинизация бензиновой фракции карбамидным методом
- •Методика определения
- •Лабораторная работа №10 Тема: Адсорбционная очистка масляных дистиллятов
- •Порядок выполнения работ
- •5. Самостоятельная работа студентов под руководством преподавателей (срсп) срсп №1. Реакционная способность органических соединений. Электронные эффекты
- •Срсп № 2. Классификация органических реакций
- •Срсп № 3. Характеристика основных механизмов реакций органических соединений
- •Срсп № 4. Образование пироуглерода и сажи
- •Срсп №5. Термические превращения углеводородов в жидкой фазе
- •Срсп №6. Процесс коксования нефтяного сырья
- •Срсп №7. Кислотный катализ
- •Реакции карбкатионов
- •Срсп №8. Классификация каталитических реакций и катализаторов
- •Энергия активации каталитической реакции
- •Срсп №9. Кинетика газофазных реакций в присутствии твердых катализаторов
- •Срсп №10. Теоретические основы подготовки и переработки газообразного сырья
- •6. Самостоятельная работа студентов срс
- •7 Экзаменационные вопросы
- •8 Технические средства обучения
- •Список рекомендуемой литературы
- •9.1 Основная литература
- •9.2 Дополнительная литература
Срсп №7. Кислотный катализ
Катализ кислотами широко применяется в нефтеперерабатывающей промышленности. Каталитическое действие кислот обусловлено образованием при их взаимодействии с углеводородами катионов углеводородов, называемых карбоний-ионами или карбкатионами. Обычно карбкатионы образуются при передаче протона от кислоты к молекуле ненасыщенного углеводорода:

Кислоты Льюиса являются энергичными акцепторами электронной пары и также могут инициировать реакцию с участием карбоний иона:
![]()
Карбкатионы – чрезвычайно реакционноспособные соединения. Константы скорости ионных реакций на несколько порядков выше аналогичных радикальных реакций. Об относительной устойчивости карбкатионов можно судить по теплоте их образования (Табл. 8).
Таблица 2 - Значения теплоты образования карбкатионов, кДж/моль:
СН3+ |
1097 |
СН3СН2СН2СН2+ |
883 |
СН3СН2+ |
955 |
СН3СН2С+НСН3 |
812 |
СН3СН2СН2+ |
917 |
(СН3)3С+ |
737 |
СН3С+НСН3 |
833 |
(СН3)3ССН2+ |
812 |
Как следует из этих данных, стабильность карбкатионов возрастает в ряду: первичный вторичный третичный.
Основными реакциями карбкатионов, как и радикалов, являются мономолекулярный распад по -правилу и бимолекулярные реакции замещения и присоединения. Существенное отличие карбкатионов от радикалов – их способность к изомеризации.
Реакции карбкатионов
Изомеризация. Изомеризация карбкатионов может происходить в результате переноса как гидрид-иона, так и метиланиона:
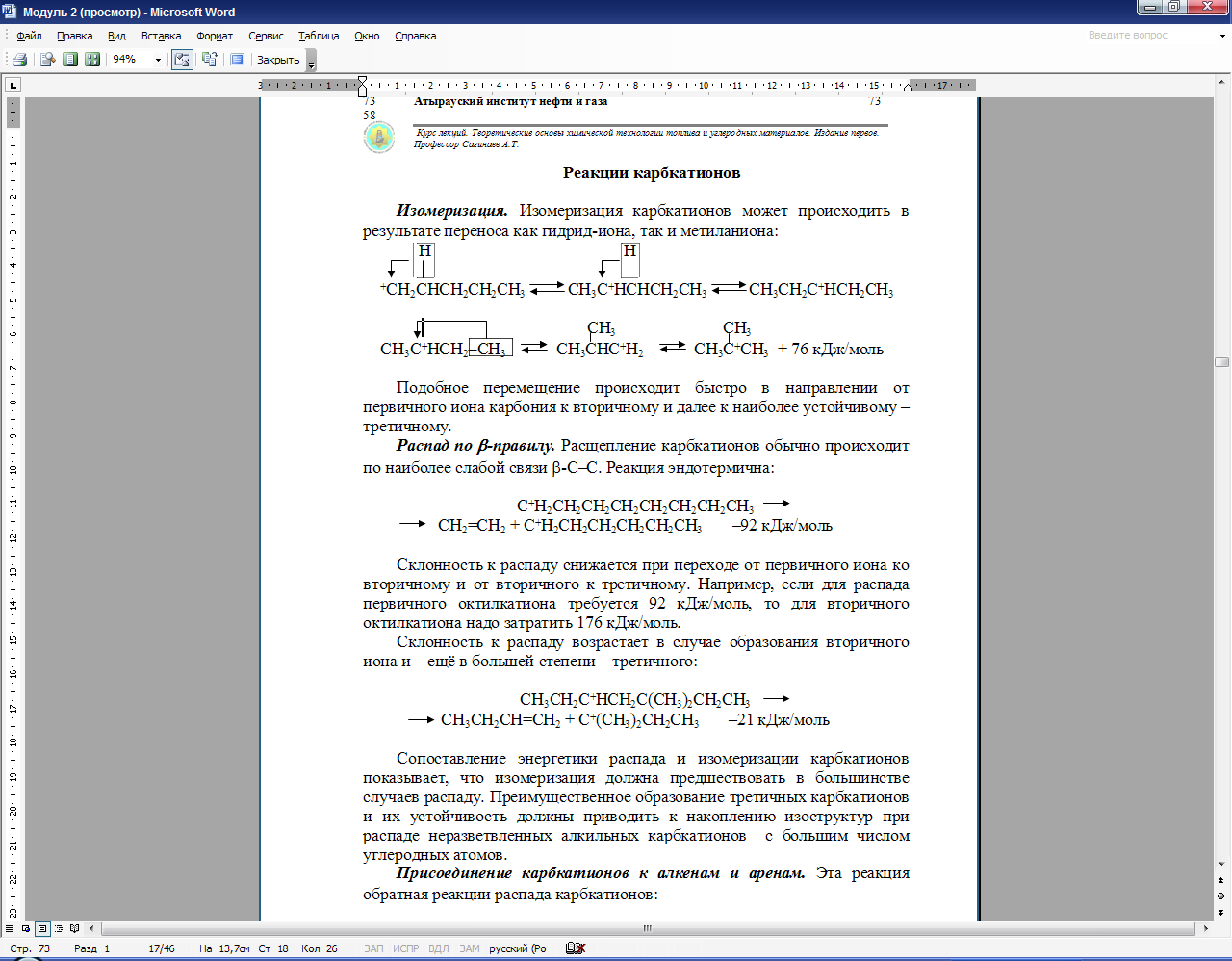
Подобное перемещение происходит быстро в направлении от первичного иона карбония к вторичному и далее к наиболее устойчивому – третичному.
Распад по -правилу. Расщепление карбкатионов обычно происходит по наиболее слабой связи -С–С. Реакция эндотермична:
+Н2СН2СН2СН2СН2СН2СН2СН3
С Н2=СН2 + С+Н2СН2СН2СН2СН2СН3 –92 кДж/моль
Склонность к распаду снижается при переходе от первичного иона ко вторичному и от вторичного к третичному. Например, если для распада первичного октилкатиона требуется 92 кДж/моль, то для вторичного октилкатиона надо затратить 176 кДж/моль.
Склонность к распаду возрастает в случае образования вторичного иона и – ещё в большей степени – третичного:
СН3СН2С+НСН2С(СН3)2СН2СН3
С Н3СН2СН=СН2 + С+(СН3)2СН2СН3 –21 кДж/моль
Сопоставление энергетики распада и изомеризации карбкатионов показывает, что изомеризация должна предшествовать в большинстве случаев распаду. Преимущественное образование третичных карбкатионов и их устойчивость должны приводить к накоплению изоструктур при распаде неразветвленных алкильных карбкатионов с большим числом углеродных атомов.
Присоединение карбкатионов к алкенам и аренам. Эта реакция обратная реакции распада карбкатионов:
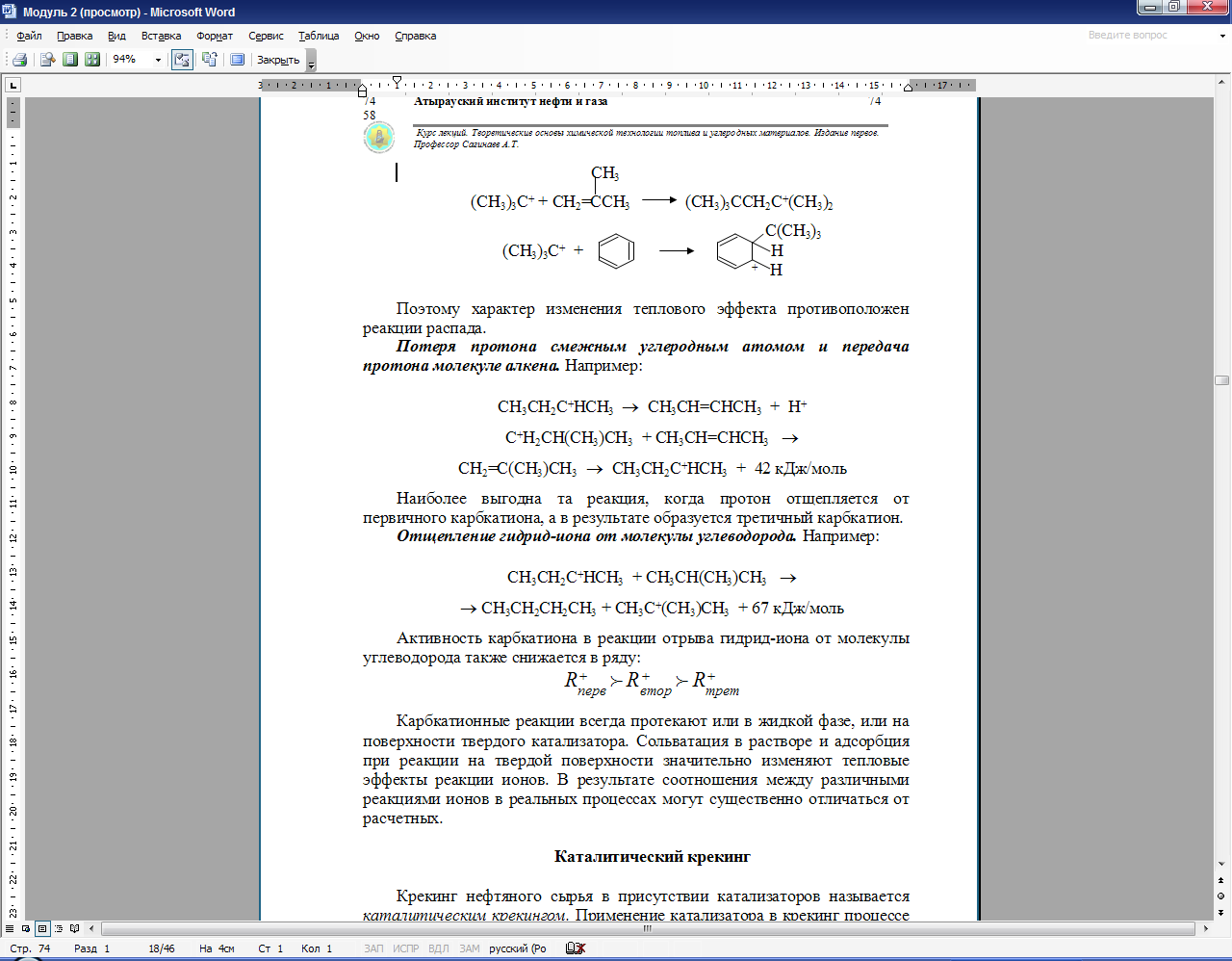
Поэтому характер изменения теплового эффекта противоположен реакции распада.
Потеря протона смежным углеродным атомом и передача протона молекуле алкена. Например:
СН3СН2С+НСН3 СН3СН=СНСН3 + Н+
С+Н2СН(СН3)СН3 + СН3СН=СНСН3
СН2=С(СН3)СН3 СН3СН2С+НСН3 + 42 кДж/моль
Наиболее выгодна та реакция, когда протон отщепляется от первичного карбкатиона, а в результате образуется третичный карбкатион.
Отщепление гидрид-иона от молекулы углеводорода. Например:
СН3СН2С+НСН3 + СН3СН(СН3)СН3
СН3СН2СН2СН3 + СН3С+(СН3)СН3 + 67 кДж/моль
Активность карбкатиона в реакции отрыва гидрид-иона от молекулы углеводорода также снижается в ряду:
![]()
Карбкатионные реакции всегда протекают или в жидкой фазе, или на поверхности твердого катализатора. Сольватация в растворе и адсорбция при реакции на твердой поверхности значительно изменяют тепловые эффекты реакции ионов. В результате соотношения между различными реакциями ионов в реальных процессах могут существенно отличаться от расчетных.
Контрольные вопросы
Роль каталитических процессов в промышленной технологии.
Что такое катализатор и каталитические реакции?
Гомогенный и гетерогенный катализ?
Литература
1. Р.З.Магарил. Теоретические основы химических процессов переработки нефти. 1985.
2. В.Н.Эрих, М.Г.Расина, М.Г.Рудин. Химия и технология нефти и газа. 1977.
