
- •Содержание
- •Глоссарий 7
- •Конспект лекционных занятий
- •3. Практические занятия
- •4. Лабораторные занятия
- •5. Самостоятельная работа студентов
- •7 Экзаменационные вопросы 181
- •8 Технические средства обучения 182
- •Список рекомендуемой литературы 182
- •1. Глоссарий
- •2 Конспект лекционных занятий модуль 1 Лекция № 1. Перспективы развития технологии органических веществ (2 часа)
- •0,5 О2 носн2-сн2он
- •О носн2-сн2nh2
- •Лекция № 2. Физико-химические основы термического крекинга
- •Лекция № 3. Физико-химические основы каталитического крекинга
- •Лекция № 4. Физико-химические основы каталитического риформинга
- •Лекция № 5. Физико-химические основы гидрогенизационных процессов
- •Лекция № 7. Химизм и механизм технологических процессов переработки нефтяных газов
- •Лекция № 8 Технологическое оборудование и технологическое оформление основных аппаратов процессов переработки органических веществ
- •Лекция № 10 Теоретические основы очистки нефтяных фракций
- •Лекция № 11 Адсорбционные и каталитические методы очистки
- •Лекция № 12 Очистка с применением избирательных растворителей
- •Лекция № 13 Депарафинизация масел и дизельных фракций
- •3. Практические занятия
- •Практическое занятие №1
- •Тема: Расчетные методы определения физико-химических свойств
- •И состава нефти и нефтепродуктов
- •Задачи для решения
- •Практическое занятие №2 Тема: Расчетные методы вычисления материального баланса процесса термического крекинга
- •Составление материального баланса
- •Задачи для решения
- •Практическое занятие №3 Тема: Составление материального баланса процесса каталитического крекинга
- •Задачи для решения
- •Практическое занятие №4 Тема: Составление материального баланса процесса каталитического риформинга
- •Задачи для решения
- •Практическое занятие №5 Тема: Расчетные методы вычисления материального баланса гидрогенизационных процессов
- •Задачи для решения
- •Практическое занятие №6 Тема: Расчетные методы вычисления материального баланса процесса полимеризационных процессов
- •Задачи для решения
- •Практическое занятие №7 Тема: Задачи и упражнения по составлению уравнений химических реакций, протекающих при алкилировании и изомеризации с указанием механизма ее протекания
- •Задачи для решения
- •Практическое занятие №8 Тема: Технологический расчет основных аппаратов установок переработки органических веществ
- •Число тарелок
- •Практическое занятие №9 Тема: Приближенные методы построения линии однократного испарения (ои)
- •Задачи для решения
- •Практическое занятие №10 Тема: Решение задач по теоретическим основам процесса очистки нефтяных фракций
- •Задачи для решения
- •Практическое занятие №11 Тема: Решение задач по депарафинизации нефтяных фракций
- •Задачи для решения
- •Практическое занятие №12 Тема: Решение задач по закономерностям получения гомогенных растворов
- •Задачи для решения
- •4. Лабораторные занятия лабораторная работа №1 Тема: Термический крекинг (пиролиз) углеводородов и составление материального баланса опыта
- •Описание установки и методика проведения работы
- •Лабораторная работа №2 Тема: Каталитический крекинг углеводородов и составление материального баланса опыта
- •Проведение работы
- •Оформление результатов работы
- •Методика проведения эксперимента
- •Приготовление алюмохромового оксидного катализатора
- •Методика выполнения работы
- •Лабораторная работа №5 Тема: Полукоксование
- •Описание установки и методика проведения работы
- •Лабораторная работа №6 Аппараты установок термических и каталитических процессов. Тема: Методы разделения и анализа продуктов реакций
- •Методика проведения работы
- •Методика проведения работы
- •Лабораторная работа №7 Тема: Разгонка нефти на ректификационном аппарате
- •Лабораторная работа №8 Тема: Очистка сырой нефти от влаги и механических примесей
- •Определение сухого остатка
- •Методика определения
- •Прокаленный остаток
- •Методика определения
- •Лабораторная работа №9 Тема: Депарафинизация бензиновой фракции карбамидным методом
- •Методика определения
- •Лабораторная работа №10 Тема: Адсорбционная очистка масляных дистиллятов
- •Порядок выполнения работ
- •5. Самостоятельная работа студентов под руководством преподавателей (срсп) срсп №1. Реакционная способность органических соединений. Электронные эффекты
- •Срсп № 2. Классификация органических реакций
- •Срсп № 3. Характеристика основных механизмов реакций органических соединений
- •Срсп № 4. Образование пироуглерода и сажи
- •Срсп №5. Термические превращения углеводородов в жидкой фазе
- •Срсп №6. Процесс коксования нефтяного сырья
- •Срсп №7. Кислотный катализ
- •Реакции карбкатионов
- •Срсп №8. Классификация каталитических реакций и катализаторов
- •Энергия активации каталитической реакции
- •Срсп №9. Кинетика газофазных реакций в присутствии твердых катализаторов
- •Срсп №10. Теоретические основы подготовки и переработки газообразного сырья
- •6. Самостоятельная работа студентов срс
- •7 Экзаменационные вопросы
- •8 Технические средства обучения
- •Список рекомендуемой литературы
- •9.1 Основная литература
- •9.2 Дополнительная литература
Срсп № 4. Образование пироуглерода и сажи
При газофазном термическом разложении углеводородов наряду с гомогенными реакциями в некоторой степени протекает реакция с образованием твердого вещества, содержащего 99% углерода – пироуглерода. Отложение пироуглерода на стенках реакционных труб печей пиролиза сильно снижает общий коэффициент теплопередачи к реагирующей смеси. Образование дисперсного пироуглерода в газовом объеме – сажи – сильно затрудняет разделение продуктов процесса. В зависимости от температуры средний диаметр частиц сажи составляет 40-3000 нм. Образование сажи начинает происходить всегда при более высокой температуре, чем выделение углерода на поверхности. Различные углеводороды в разной степени склонны к образованию сажи. С ростом числа С : Н в молекуле углеводорода выход сажи при заданных условиях повышается. Водород тормозит образование сажи.
Образование сажи происходит, как и пироуглерода, за счет прямого разложения углеводородных молекул до элементов.
Для неароматических углеводородов образованию сажи всегда предшествует образование ацетилена; предполагают, что в этом случае сажевые частицы из него и образуются. В случае ароматических углеводородов зародыши сажевых частиц образуются с большей скоростью, чем из ацетилена. С увеличением числа конденсированных аренов скорость образования сажевых частиц повышается.
Сажа и пироуглерод ‑ продукты высокотемпературного пиролиза углеводородных газов, протекающего как радикально-цепной процесс. Конечные продукты этого процесса термодинамически наиболее устойчивые при температурах порядка 1000 оС ‑ молекулярный водород и свободный углерод. Рассмотрим, например, возможный механизм образования сажи из метана ‑ углеводорода с наибольшим содержанием водорода:
СН4 С + 2Н2 (+Н293)=74,75 кДж/моль СН4
Наиболее простым путем термического разложения метана может быть ряд последовательных стадий дегидрирования:
-
‑Н
‑Н
‑Н
‑Н
СН4
СН3
СН2
СН
С
Однако расчеты показывают, что затраты энергии на образование атомов водорода, углеводородных радикалов и газообразного углерода очень велики, например:
СН4 СН3 + Н (+Н293)=431,54 кДж/моль СН4.
Очевидно, что эндотермические процессы дегидрирования должны параллельно сопровождаться какими-то экзотермическими реакциями, по-видимому, ассоциацией атомов водорода и углеводородных радикалов.
Затраты энергии на образование углеводородных радикалов непрерывно снижаются с укрупнением последних. Исходя из энергетических затрат вполне убедительной выглядит, например, следующая схема:
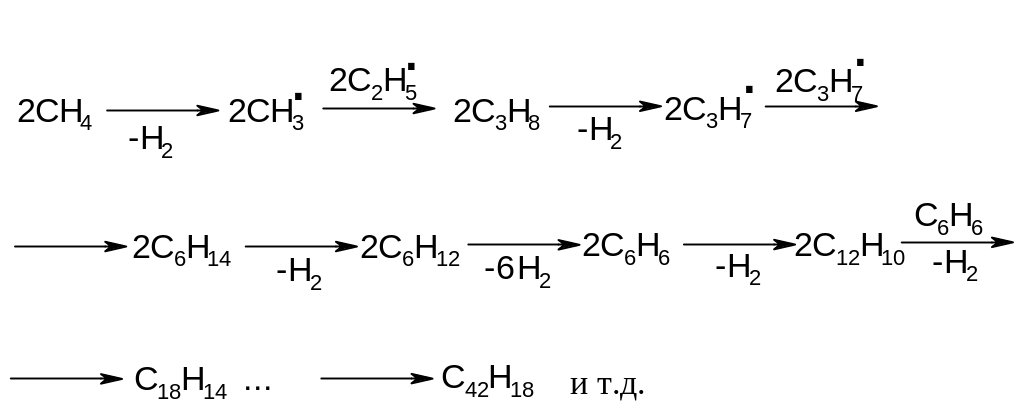
Рост углеродной цепи промежуточных радикалов следует рассматривать как радикально-цепной процесс, первой стадией которого является термическое инициирование по реакции: СН4 СН3 + Н. Далее оба радикала могут взаимодействовать с молекулой метана:
СН3 + СН4 С2Н5 + Н2;
Н + СН4 СН3 + Н2.
В результате первой реакции происходит рост длины углеродной цепи, этот процесс продолжается и дальше:
С2Н5 + СН4 С3Н7 + Н2.
При взаимодействии углеводородного радикала с молекулой углеводорода преимущественно образуется новый, более тяжелый (а потому и более устойчивый) углеводородный радикал. Можно было бы ожидать образования атома водорода и углеводородной молекулы, например:
С2Н5 + СН4 С3Н8 + Н,
но этот путь оказывается термодинамически невыгодным из-за очень высокой неустойчивости атомарного водорода.
Последующая полициклизация бензола, образовавшегося по этой схеме, сопровождается отщеплением водорода и ассоциацией фенильных радикалов. Она приводит к формированию полициклических конденсированных углеводородов. Образование плоских конденсированных молекул из ароматических колец, по-видимому, представляет собой цепной радикальный процесс, протекающий через промежуточное образование углеводородных радикалов с высокой степенью делокализации неспаренного электрона с их последующей конденсацией:
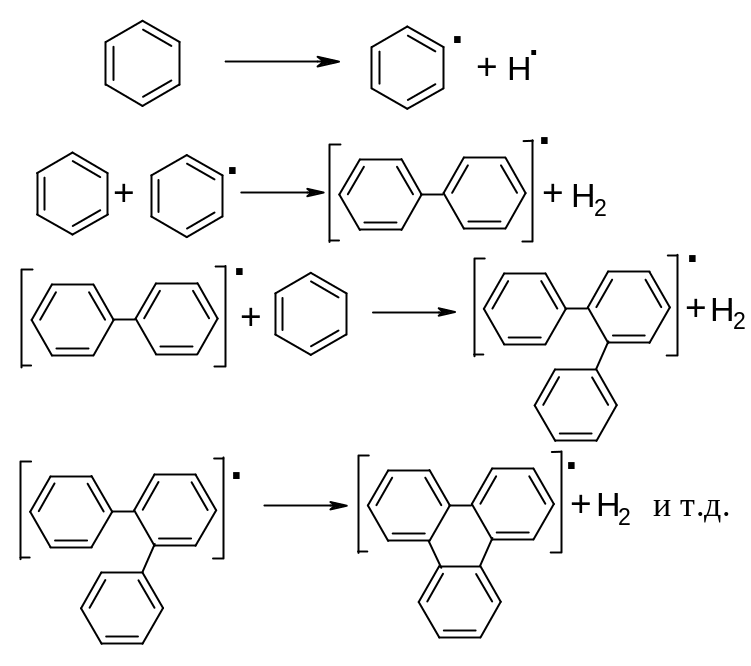
Полициклические углеводороды разрастаются и все дальше к периферии оттесняют имеющийся в них водород, относительное содержание которого становится все меньшим и меньшим. Происходит формирование кристаллитов, а последние затем объединяются в сажевые частицы. При их соударении формируются сажевые структуры.
Контрольные вопросы
Что такое пироуглерод?
Как происходит образование сажи?
Литература
1. Р.З.Магарил. Теоретические основы химических процессов переработки нефти. 1985.
2. В.Н.Эрих, М.Г.Расина, М.Г.Рудин. Химия и технология нефти и газа. 1977.
