
- •Содержание
- •Глоссарий 7
- •Конспект лекционных занятий
- •3. Практические занятия
- •4. Лабораторные занятия
- •5. Самостоятельная работа студентов
- •7 Экзаменационные вопросы 181
- •8 Технические средства обучения 182
- •Список рекомендуемой литературы 182
- •1. Глоссарий
- •2 Конспект лекционных занятий модуль 1 Лекция № 1. Перспективы развития технологии органических веществ (2 часа)
- •0,5 О2 носн2-сн2он
- •О носн2-сн2nh2
- •Лекция № 2. Физико-химические основы термического крекинга
- •Лекция № 3. Физико-химические основы каталитического крекинга
- •Лекция № 4. Физико-химические основы каталитического риформинга
- •Лекция № 5. Физико-химические основы гидрогенизационных процессов
- •Лекция № 7. Химизм и механизм технологических процессов переработки нефтяных газов
- •Лекция № 8 Технологическое оборудование и технологическое оформление основных аппаратов процессов переработки органических веществ
- •Лекция № 10 Теоретические основы очистки нефтяных фракций
- •Лекция № 11 Адсорбционные и каталитические методы очистки
- •Лекция № 12 Очистка с применением избирательных растворителей
- •Лекция № 13 Депарафинизация масел и дизельных фракций
- •3. Практические занятия
- •Практическое занятие №1
- •Тема: Расчетные методы определения физико-химических свойств
- •И состава нефти и нефтепродуктов
- •Задачи для решения
- •Практическое занятие №2 Тема: Расчетные методы вычисления материального баланса процесса термического крекинга
- •Составление материального баланса
- •Задачи для решения
- •Практическое занятие №3 Тема: Составление материального баланса процесса каталитического крекинга
- •Задачи для решения
- •Практическое занятие №4 Тема: Составление материального баланса процесса каталитического риформинга
- •Задачи для решения
- •Практическое занятие №5 Тема: Расчетные методы вычисления материального баланса гидрогенизационных процессов
- •Задачи для решения
- •Практическое занятие №6 Тема: Расчетные методы вычисления материального баланса процесса полимеризационных процессов
- •Задачи для решения
- •Практическое занятие №7 Тема: Задачи и упражнения по составлению уравнений химических реакций, протекающих при алкилировании и изомеризации с указанием механизма ее протекания
- •Задачи для решения
- •Практическое занятие №8 Тема: Технологический расчет основных аппаратов установок переработки органических веществ
- •Число тарелок
- •Практическое занятие №9 Тема: Приближенные методы построения линии однократного испарения (ои)
- •Задачи для решения
- •Практическое занятие №10 Тема: Решение задач по теоретическим основам процесса очистки нефтяных фракций
- •Задачи для решения
- •Практическое занятие №11 Тема: Решение задач по депарафинизации нефтяных фракций
- •Задачи для решения
- •Практическое занятие №12 Тема: Решение задач по закономерностям получения гомогенных растворов
- •Задачи для решения
- •4. Лабораторные занятия лабораторная работа №1 Тема: Термический крекинг (пиролиз) углеводородов и составление материального баланса опыта
- •Описание установки и методика проведения работы
- •Лабораторная работа №2 Тема: Каталитический крекинг углеводородов и составление материального баланса опыта
- •Проведение работы
- •Оформление результатов работы
- •Методика проведения эксперимента
- •Приготовление алюмохромового оксидного катализатора
- •Методика выполнения работы
- •Лабораторная работа №5 Тема: Полукоксование
- •Описание установки и методика проведения работы
- •Лабораторная работа №6 Аппараты установок термических и каталитических процессов. Тема: Методы разделения и анализа продуктов реакций
- •Методика проведения работы
- •Методика проведения работы
- •Лабораторная работа №7 Тема: Разгонка нефти на ректификационном аппарате
- •Лабораторная работа №8 Тема: Очистка сырой нефти от влаги и механических примесей
- •Определение сухого остатка
- •Методика определения
- •Прокаленный остаток
- •Методика определения
- •Лабораторная работа №9 Тема: Депарафинизация бензиновой фракции карбамидным методом
- •Методика определения
- •Лабораторная работа №10 Тема: Адсорбционная очистка масляных дистиллятов
- •Порядок выполнения работ
- •5. Самостоятельная работа студентов под руководством преподавателей (срсп) срсп №1. Реакционная способность органических соединений. Электронные эффекты
- •Срсп № 2. Классификация органических реакций
- •Срсп № 3. Характеристика основных механизмов реакций органических соединений
- •Срсп № 4. Образование пироуглерода и сажи
- •Срсп №5. Термические превращения углеводородов в жидкой фазе
- •Срсп №6. Процесс коксования нефтяного сырья
- •Срсп №7. Кислотный катализ
- •Реакции карбкатионов
- •Срсп №8. Классификация каталитических реакций и катализаторов
- •Энергия активации каталитической реакции
- •Срсп №9. Кинетика газофазных реакций в присутствии твердых катализаторов
- •Срсп №10. Теоретические основы подготовки и переработки газообразного сырья
- •6. Самостоятельная работа студентов срс
- •7 Экзаменационные вопросы
- •8 Технические средства обучения
- •Список рекомендуемой литературы
- •9.1 Основная литература
- •9.2 Дополнительная литература
Приготовление алюмохромового оксидного катализатора
При отсутствии промышленного алюмоплатинового катализатора можно приготовить менее активный, но более доступный алюмохромовый оксидный катализатор по следующей методике. 300 г γ-оксида алюминия пропитывают 130 мл 38%-ного водного раствора оксида хрома СгО3 до полной адсорбции раствора носителем. Полученную смесь высушивают в сушильном шкафу при температуре не выше 150 °С в течение 2 ч, охлаждают и обрабатывают 110 мл 8%-ного водного раствора нитрата калия. Тщательно перемешивают до полной адсорбции раствора и снова высушивают в сушильном шкафу при 150°С в течение 4 ч. Затем катализатор осторожно измельчают, просеивают через сито с размером ячеек 1,5—3,0 мм, необходимое количество загружают в реактор и восстанавливают.
Для восстановления катализатора в реактор через кран 2 подают водород со скоростью 50 мл/мин, включают обогрев реактора и нагревают его до 500 °С. По достижении указанной температуры увеличивают скорость подачи водорода до 150 мл/мин и восстанавливают катализатор в течение 4 ч. Полученный таким образом катализатор используют для опытов по ароматизации парафиновых углеводородов.
Контрольные вопросы
Назначение процесса ароматизации.
Реакции ароматизации.
Применение продуктов процесса ароматизации.
Литература
Одабашян Г.В. Лабораторный практикум по химии ТООНХС. М., Химия, 1982, с. 86-89.
Воскресенский П.И. Техника лабораторных работ. 10-е изд. М.. Химия, 1973, 717 с.
Лабораторная работа №4
Тема: Гидрокрекинг углеводородов и составление материального баланса опыта.
Гидрирование бензола в циклогексан
Теоретические основы процесса
Большое число важнейших химических соединений (циклогексан, циклогексанол, высшие спирты, амины, стирол, изобутилен, бутадиен-1,3 и др.) в промышленности получают при помощи процессов гидрирования и дегидрирования.
Реакции гидрирования и дегидрирования тесно связаны друг с другом, протекают в противоположных направлениях и в большинстве случаев находятся в термодинамическом равновесии:
АН2
![]() А + Н2
А + Н2
Реакция гидрирования сопровождается уменьшением объема реакционной массы и выделением тепла, а реакция дегидрирования — увеличением объема реакционной массы и поглощением тепла. Поэтому сдвиг равновесия в сторону гидрирования или дегидрирования зависит от условий процесса. Так, низкие температуры и высокие давления благоприятствуют реакции гидрирования, а высокие температуры и низкие давления — реакции дегидрирования. Процессы гидрирования и дегидрирования, как правило, проводят в присутствии катализаторов, которые значительно повышают скорость процесса и его селективность. В качестве катализаторов применяют металлы и их сплавы (Pt, Pd, Ni, Cu, Zn и др.), оксиды металлов и их смеси (Fe2O3, Сr3О3, ZnO, MgO и др.), сульфиды металлов и их смеси (NiSi, WS3, MoS3 и др.).
Металлы являются наиболее активными катализаторами, поэтому их чаще всего используют в процессах гидрирования, которые проводят при температурах до 220 °С и давлении до 6 МПа. В процессах дегидрирования применяют преимущественно оксидные катализаторы, которые по сравнению с металлами хотя и менее активны, но при 500—650 °С обладают большей селективностью, стабильностью и легко регенерируются.
Циклогексан и циклогексанол являются важными промежуточными продуктами в процессе получения циклогексанона, капролактама и адипиновой кислоты. Кроме того, они широко используются как растворители.
В промышленности циклогексан и циклогексанол получают гидрированием бензола и фенола соответственно. Процесс проводят под давлением при мольном отношении гидрируемого вещества к водороду, равном 1: (10÷30). Например, бензол гидрируют на никелевом катализаторе при 180—200 °С и 1,5—2,0 МПа или на сульфидных катализаторах при л;300°С и 20—30 МПа:
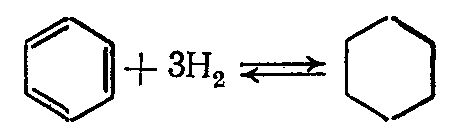
При гидрировании бензола на никелевом катализаторе повышение температуры выше 220 °С приводит к частичному распаду циклогексана на углерод, метан и другие побочные продукты и к. быстрой дезактивации катализатора.
Фенол гидрируют на никелевом катализаторе при температурах не выше 150°С и давлении 1,5—2,0 МПа в газовой фазе. При более высокой температуре значительная часть фенола гидрируется до циклогексанона и расходуется на образование других побочных продуктов:
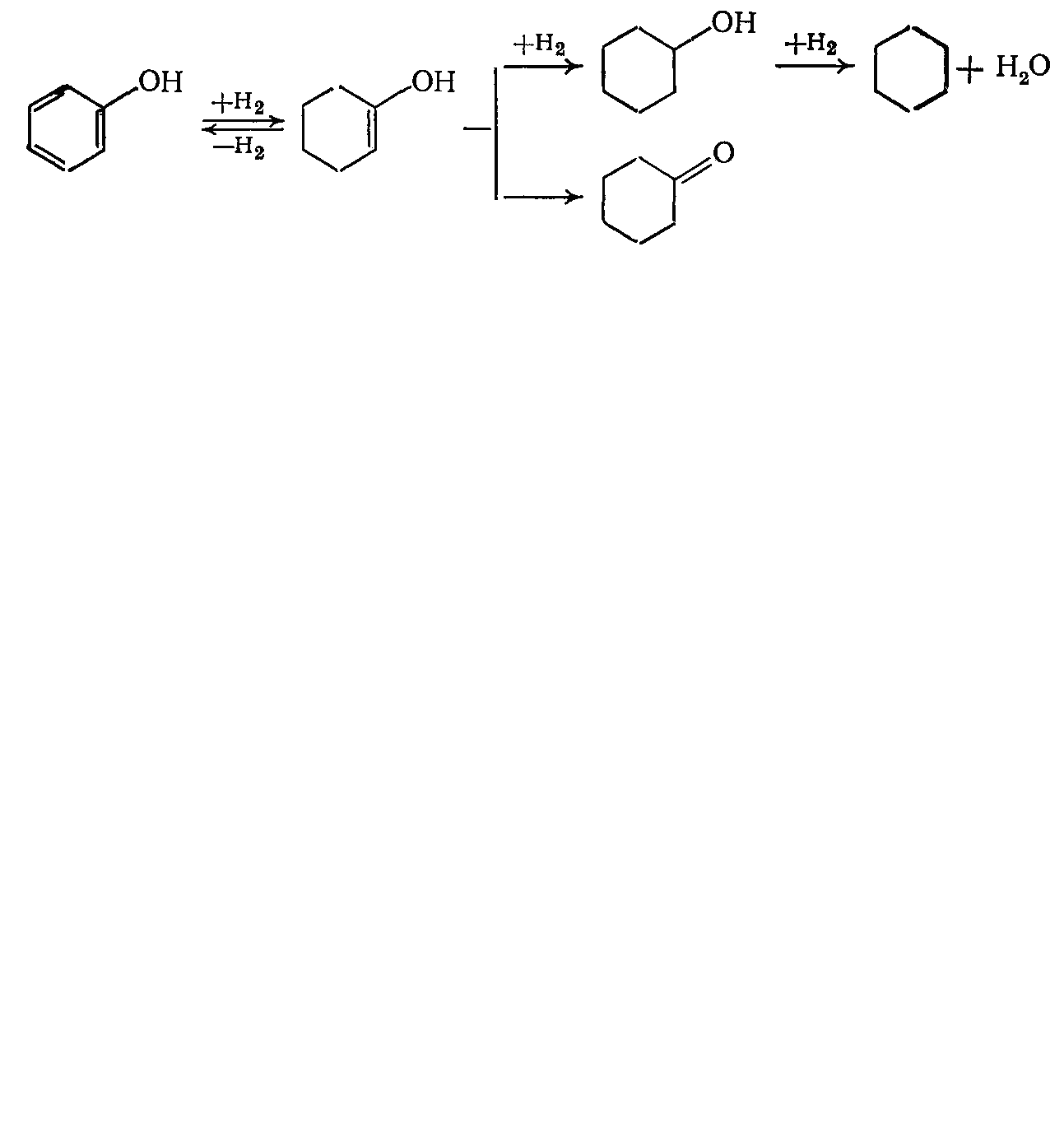
Циклогексанон можно гидрировать в циклогексанол, но условия гидрирования более жесткие. Селективность гидрирования бензола и фенола составляет 98% и выше.
Цель работы
Изучение реакции гидрирования бензола в циклогексан в газовой фазе при атмосферном давлении, определение степени конверсии бензола и составление материального баланса.
