
Содержание
1. Задание 1 3
18
1. Задание 1
Что называется элементарной кристаллической ячейкой металлов? Охарактеризуйте основные типы ячеек. Каково их практическое значение?
Ответ:
Элементарная кристаллическая ячейка – наименьший комплекс атомов, повторяя который многократно, можно построить весь кристалл.
У металлов чаще всего встречаются три типа элементарных кристаллических ячеек:
В кубической объемноцентрированной (ОЦК) решетке восемь ионов располагаются по вершинам и один в центре куба, на пересечении диагоналей. Объемноцентрированную кубическую решетку имеют кристаллы железа при комнатной температуре, хрома, вольфрама, молибдена, ванадия и др. Эта решетка характеризуется всего одним параметром решетки – расстоянием между центрами двух ионов, расположенных по одному ребру – a, обозначенным на рис.1:
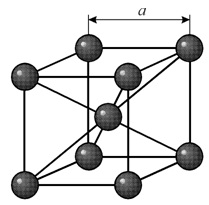
Рис. 1. Объемноцентрированная кубическая решетка (ОЦК), К8
Многие металлы, используемые в технике, имеют гранецентрированную кубическую решетку. В элементарной решетке гранецентрированного куба ионы расположены по вершинам куба и в центре каждой грани (на пересечении ее диагоналей). Центр куба остается свободным. Такую кристаллическую решетку имеют кристаллы меди, никеля, алюминия, свинца, серебра и др. Гранецентрированная решетка также характеризуется одним параметром – длиной ребра куба а, рис. 2:
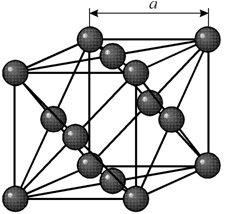
Рис. 2. Гранецентрированная кубическая решетка, К12
Элементарная ячейка гексагональной плотноупакованной решетки представляет собой шестигранную призму. По основаниям призмы расположены правильные шестиугольники по вершинам которых и в их центрах находятся ионы. Посередине между основаниями вклинивается правильный треугольник с ионами по вершинам:
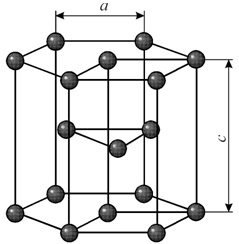
Рис. 3. Гексагональная решетка, Г12
Гексагональная решетка характеризуется двумя параметрами: а и с. Наибольшая плотность упаковки достигается при соотношении параметров с/а = 1.633. Гранецентрированная решетка с таким соотношением параметров называется гранецентрированной плотноупакованной. Такую решетку имеют титан, цирконий, кобальт, цинк, магний и др.
Элементарная кристаллическая ячейка характеризуется координационным числом, под которым понимают число атомов, находящихся на наиболее близком равном расстоянии от избранного атома. В объемно-центрированной кубической решетке атом находится на наиболее близком равном расстоянии от восьми атомов, расположенных в вершинах куба, то есть координационное число этой решетки, см. рис.1. В гранецентрированной кубической решетке (рис.2) атом находится на наиболее близком расстоянии от четырех атомов, расположенных в вершинах куба, от четырех атомов расположенных на гранях куба, и от четырех атомов, принадлежащих расположенной рядом кристаллической ячейке. Следовательно, для гранецентрированной кубической решетки координационное число равно 12 (К12). Для гексагональной плотноупакованной решетки координационное число также равно 12.
Практическое значение знаний о типе кристаллической решетки металлов заключается в том, что некоторые металлы (железо, титан, кобальт, цирконий и др.) при разных температурах имеют различные кристаллические решетки. Такое явление называется полиморфизмом или аллотропией. Процесс перехода из одного кристаллического строения в другое называется полиморфным (аллотропическим) превращением.
Строение, получающееся в результате полиморфного превращения, называется аллотропической формой. Аллотропическая форма, устойчивая при более низкой температуре, обозначается индексом α, при более высокой – , γ и так далее. Температура, при которой происходит переход решетки из одного вида в другой, называется температурой полиморфного превращения или температурой перекристаллизации. При этом изменяются свойства металла (плотность, теплопроводность, теплоемкость и др.).
Примером аллотропического видоизменения в зависимости от температуры является железо (Fe).
t < 911C – ОЦК – Feα;
911C < t < 1392C – ГЦК – Fe;
1392C < t < 1539C – ОЦК – Feδ; (высокотемпературное Feα)
Таким образом, используя явление полиморфизма, можно упрочнять и разупрочнять железоуглеродистые сплавы при помощи термической обработки.
