
- •16. Амины 11 Лекция 12. Амины
- •Действием аммиака на галогенпроизводные (реакция Гофмана).
- •При восстановлении нитроалканов и нитрилов образуются первичные амины:
- •Водные растворы алкиламинов имеют щелочную среду:
- •С кислотами алкиламины образуют соли алкиламмония:
- •Восстановление нитросоединений (реакция Зинина).
- •2. Взаимодействие галогенпроизводных с аммиаком и аминами.
- •3. Алкилирование первичных ариламинов.
- •Реакция галогенирования.

16. Амины 11 Лекция 12. Амины
Амины — производные аммиака, в молекуле которого один, два или три атома водорода замещены углеводородными радикалами. По числу замещенных атомов водорода они делятся на первичные, вторичные и третичные амины.
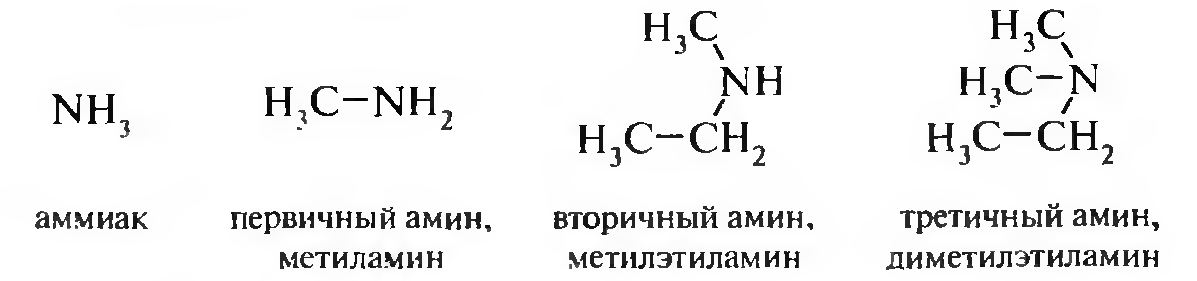
Существуют и четвертичные аммониевые соли, например хлорид тет-раметиламмония [(СН3)4N+]Сl-, соответствующее ему основание —гидроксид тетраметиламмония [(CH3)4N+]OH-, который представляет собой сильное основание, аналогичное гидроксидам щелочных металлов, так как связь с гидроксильной группой здесь ионная.
В зависимости от природы углеводородных радикалов амины подразделяются на алифатические, алициклические, ароматические и смешанные (имеющие алифатический и ароматический радикалы):
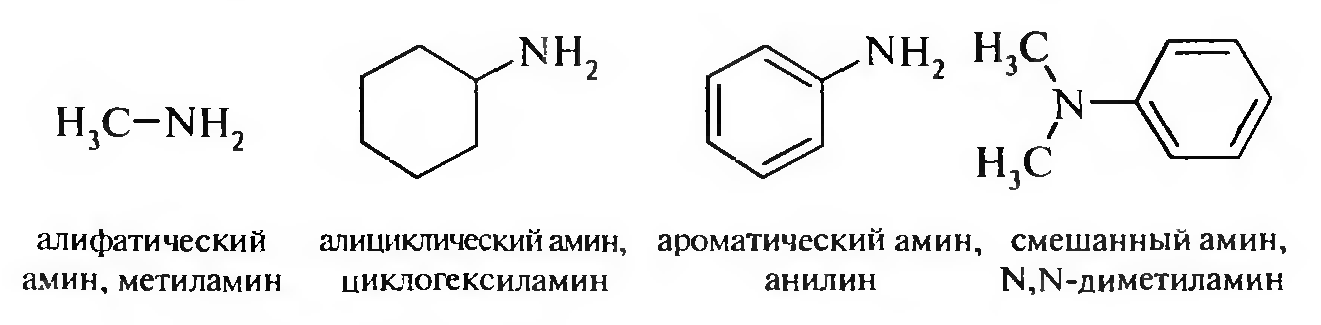
Для аминов характерна метамерия:

Эти соединения имеют общую формулу С3H9N, но отличаются друг от друга строением углеводородных радикалов.
Названия простых по строению аминов образуют от названий соответствующих углеводородных радикалов, связанных с атомом азота, добавляя в конце корень -амин. Кроме того, многие ароматические амины имеют тривиальные названия.

Производные толуола, содержащие аминогруппу в бензольном ядре, называются толуидинами:
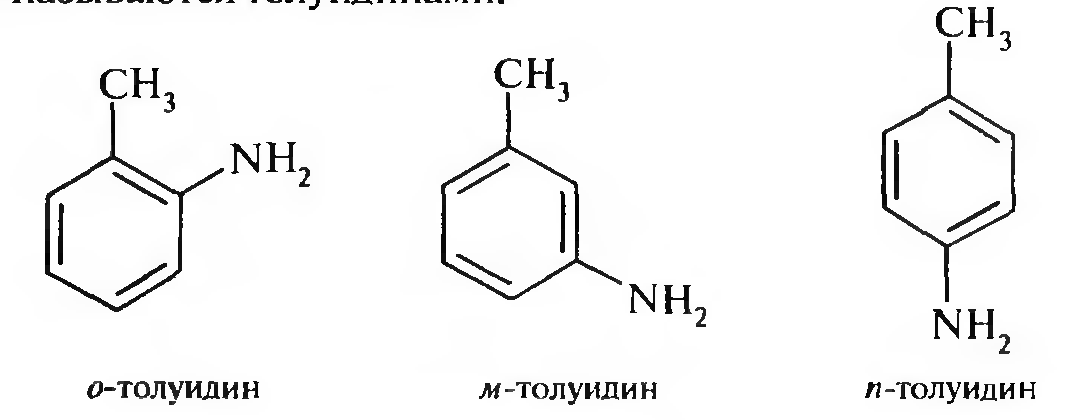
АМИНЫ АЛИФАТИЧЕСКОГО РЯДА (АЛКИЛАМИНЫ)
Способы получения
Действием аммиака на галогенпроизводные (реакция Гофмана).
![]()
Первоначально аммиак с хлористым метилом образует соль, которая под действием избытка аммиака превращается в первичный амин.
Метилирование может протекать и дальше. Образовавшийся первичный амин реагирует со следующей молекулой галогеналкана и т. д. В результате образуется вторичный амин, затем третичный и соль четвертичного аммониевого основания:
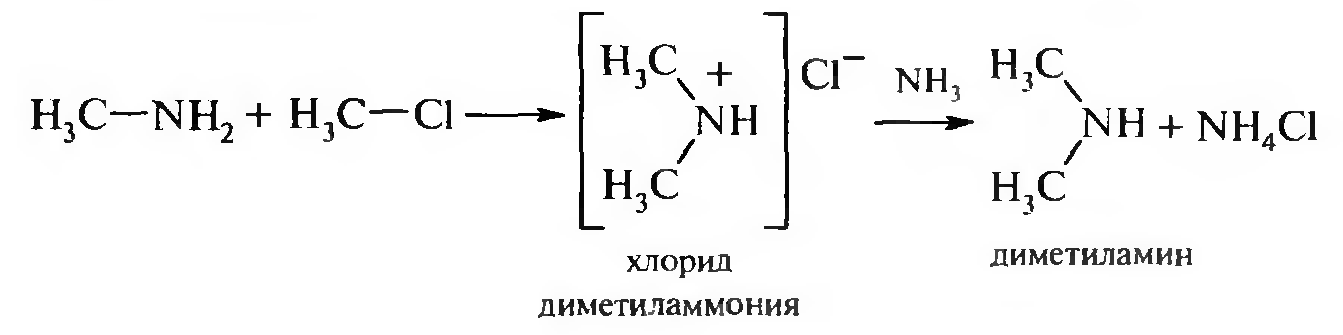

Преимущество этого метола — это простота, недостаток — трудно разделить образующиеся амины, однако для промышленного производства этот метод очень удобен.
Перегруппировка Гофмана. При обработке незамещенных амидов карбоновых кислот гипобромитом натрия (смесь брома и гидроксида натрия) образуются первичные амины, при этом углеродная цепь укорачивается на один атом:

Этот способ имеет большое значение и дает возможность получать чистые амины.
Способ Габриэля. Конденсацией фталимида калия с алкилгалоге- нидами с последующим гидролизом получают только первичные алифатические амины:

При восстановлении нитроалканов и нитрилов образуются первичные амины:
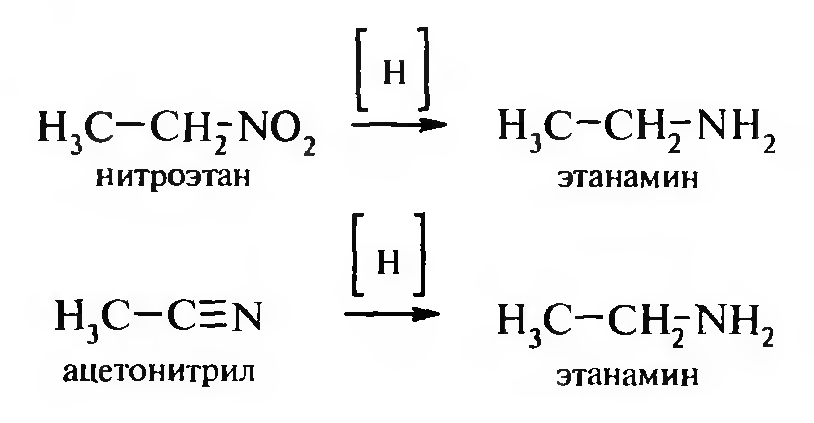
Низшие амины (метиламин и этиламин) — газы, с увеличением количества атомов углерода — жидкости, высшие амины — твердые вещества. Они обладают аммиачным запахом, а также запахом соленой сельди.
Низшие амины хорошо растворимы в воде, с увеличением молекулярной массы растворимость снижается, а высшие амины не растворимы в воде.
Химические свойства
Реакционная способность алифатических аминов определяется наличием у атома азота неподеленной пары электронов, которая обуславливает то, что амины активно выступают в роли нуклеофилов, а также являются сильными органическими основаниями.
Основность. Являясь производными аммиака, алкиламины подобно аммиаку проявляют ярко выраженные основные свойства, которые обусловлены способностью атома азота с неподеленной электронной парой к присоединению протона с образованием иона замещенного аммония. При этом амины в 10 раз сильнее, чем аммиак. Это связано с изменением электронной плотности на атоме азота.
![]()
Алкильные радикалы увеличивают электронную плотность на атоме азота за счет проявления +I-эффекта, что приводит к заметному усилению основности. Поэтому можно предположить, что третичные алкиламины, имеюшие три донорных заместителя, будут более сильными основаниями, чем вторичные, а вторичные, в свою очередь, более сильными, чем первичные и аммиак:
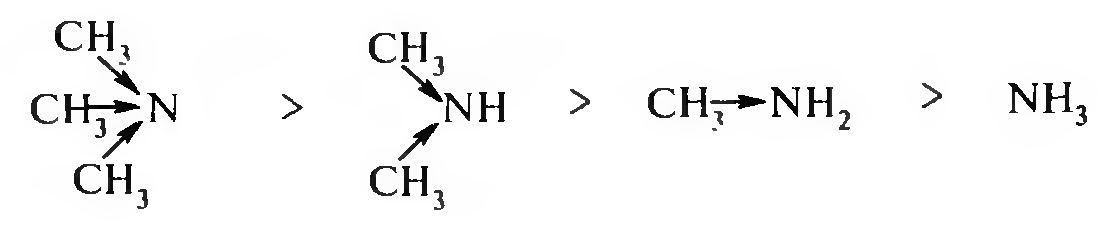
Такая закономерность изменения основности алкиламинов наблюдается в газовой фазе и в неводных растворах. В водных растворах наряду с электронными эффектами заместителей влияет и сольватационный эффект растворителя.
В результате совместного проявления этих двух факторов основность третичных аминов в водных растворах ниже основности первичных и вторичных:
