
- •Раздел 8
- •8.2. Аналитические реакции и их характеристика
- •8.3. Аналитическая классификация катионов
- •Раздел 9 первая аналитическая группа катионов
- •9.1. Общая характеристика группы
- •9.4. Систематический анализ смеси катионов первой аналитической группы
- •Отделение ионов аммония
- •Определение катионов Натрия и Калия
- •Раздел 10 вторая аналитическая группа катионов
- •10.1. Общая характеристика группы и биологическая роль катионов
- •10.3. Систематический анализ смеси катионов второй аналитической группы
- •1. Осаждение катионов второй аналитической группы
- •2 Исследование осадка
- •Раздел 11 третья аналитическая группа катионов
- •11.1. Общая характеристика группы
- •11.2. Биологическая роль и медицинское применение соединений
- •10. Реакция с групповым реактивом (сульфатной кислотой).
- •11.4. Систематический анализ смеси катионов третьей аналитической группы
- •Осаждение катионов в виде сульфатов
- •Превращение сульфатов катионов III группы в карбонаты
- •Разделение катионов и их определение
- •Раздел 12 четвертая аналитическая группа катионов
- •12.1. Общая характеристика группы
- •12.2. Биологическая роль и значение соединений катионов IV группы для медицины
- •14. Реакция с окислителями или восстановителями.
- •12.4. Систематический анализ смеси катионов четвертой аналитической группы
- •1. Действие группового реактива
- •2 Отделение катионов Алюминия
- •3 Анализ центрифугата
- •Раздел 13 пятая аналитическая группа катионов
- •13.1. Общая характеристика группы
- •13.2. Биологическая роль и медицинское применение соединений
- •13.4. Анализ смеси катионов пятой аналитической группы
- •1. Предыдущие испытания
- •2. Осаждение катионов V группы
- •4. Обнаружение катионов Мангана(іі)
- •Раздел 14 шестая аналитическая группа катионов
- •14.1. Общая характеристика группы
- •14.2. Биологическая роль и значения соединений катионов VI аналитической группы для медицины
- •14.4. Анализ смеси катионов шестой аналитической группы дробним методом
- •14.5. Систематический анализ смеси катионов шестой аналитической группы
- •1. Разделение катионов
- •2. Анализ центрифугата
- •Систематический анализ смеси катионов шестой аналитической группы
- •Раздел 1 6 качественные реакции анионов. Анализ неизвестного вещества и содержимого их некоторых примесей
- •16.1. Первая аналитическая группа анионов
- •16.1.1. Общая характеристика группы
- •16.1.2. Биологическая роль и медицинское применение соединений
- •16.1.3. Качественные реакции анионов so42-, so32-, ро43-, со32-, с2о42-, с4н4o62-, нс6н5o72-
- •Реакции сульфитов-ионов so32-
- •Реакции фосфат-ионов ро43-
- •Реакции карбонат-ионов co32-
- •Реакции оксалат-ионов с2о42-
- •13. Реакция с групповым реактивом ВаС12. Барий хлорид образует с анионами с2о42- белый осадок барий оксалата:
- •Реакции тартрат-ионов с4н4о62-
- •Реакции цитрат-ионов нс6н5о72-
- •16.2. Вторая аналитическая группа анионов
- •16.2.1. Общая характеристика группы, биологическая роль и медицинское применение соединений
- •16.2.2. Качественные реакции анионов Сl-, Br-, і-, s2-, с6н5соо- Реакции хлорид-ионов Сl-
- •Реакции бромид-иоиов Вr-
- •Реакции йодид-ионов I-
- •Реакции сульфид-ионов s2-
- •Реакции бензоат-ионов с6н5соо-
- •16,3. Третья аналитическая группа анионов
- •16.3.1. Общая характеристика группы, биологическая роль и медицинское применение соединений
- •16.3.2. Качественные реакции анионов no2-, no3-, МnО4-, сн3соо-, с6н4(он)соо- Реакции нитрит-ионов no2-
- •Реакции нитрат-ионов no3-
- •Реакции перманганат-ионов МnО4-
- •Реакции ацетат-ионов сн3соо-
- •Реакции салицилат-ионов с6н4(он)соо-
Разделение катионов и их определение
К полученному осадку, который содержит карбонаты, добавляют ацетатную кислоту до полного растворения осадка. Из этого раствора сначала осаживают ионы Ва2+ в виде барий хромата ВаCrO4 . Для этого к раствору добавляют натрий ацетат (приблизительно такой же объем) и действуют калий дихроматом до полного выделения осадка. Появление желтого осадка при наличии CH3COONa свидетельствует о наличии ионов Ва2+. Если он обнаружен, то проверяют полноту осаждения ионов Ва2+ и отделяют осадок от раствора центрифугированием.
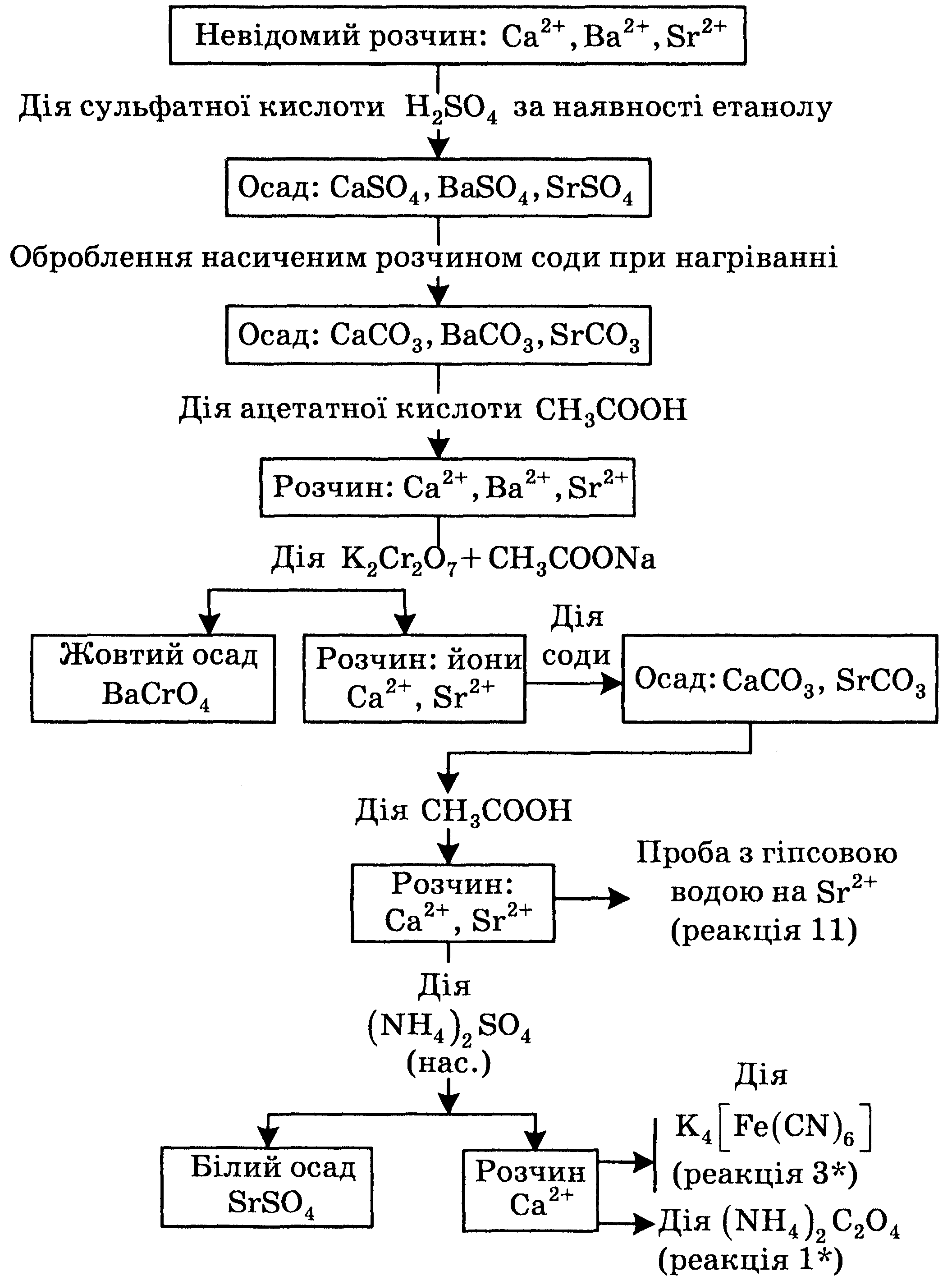
К раствору, который содержит ионы Са2+ и Sr2+, добавляют раствор соды, отделяют осадок и растворяют его в ацетатной кислоте. В отдельной порции раствора определяют ионы Sr2+ по реакции 11 с гипсовой водой CaSO4.
Для выделения катионов Са2+ от Sr2+ к раствору добавляют аммоний сульфат, который осаждает Стронций в виде сульфата, а в растворе остаются ионы Са2+ в виде комплексной соли (NH4)2[Са(SO4)2]. Ионы Кальция обнаруживают по качественной реакцией 3* с желтой кровяной солью или с помощью реакции 1*с аммоний оксалатом.
Раздел 12 четвертая аналитическая группа катионов
12.1. Общая характеристика группы
К четвертой аналитической группе принадлежат катионы: Zn2+, Cr3+, А13+, As3+, As5+, Sn2+, Sn4+. Групповым реактивом является раствор натрий гидроксида NaOH, который осаждает все перечисленные катионы в виде гидроксидов, которые имеют амфотерные свойства, т.е. растворяются в кислотах и в избытке щелочи. Учитывая значение этих ионов для медицины и фармацевтического анализа, рассмотрим качественные реакции катионов Цинка и Хрома, а также Алюминия и Арсена (мышьяка).
Катионы Цинка и Хрома(ІІІ) принадлежат к d-элементам, остальные являются р-элементами. Соединения Цинка и Алюминия характеризуются постоянной валентностью (II и III), а соответственно, и степенью окисления. Хром принадлежит к переходным металлам, поэтому обнаруживает разные степени окисления: +2, +3, +6. В связи с этим катионы Zn2+ и А13+ легче вступают в реакции комплексообразования, а ионы Хрома — в окислительно-восстановительные реакции, причем ионы с низшей степенью окиснення являются восстановителями, а с высшей — только окислителями.
Оксидам с низшими степенями окисления отвечают основания, с высшими - кислоты, а с промежуточными - и основания, и кислоты. Кислотно-основные свойства соединений Хрома в зависимости от его валентности приведены в табл. 12.1:
Катионы четвертой аналитической группы при взаимодействии со щелочами образуют гидроксиды, которые относятся к слабым основаниям. Они не растворяются в воде, но растворяются в кислотах. Обнаруживая типичные амфотерные свойства, гидроксиды этих катионов растворяются не только в кислотах, но и в щелочах. Например:
Таблица 12.1. Кислотно-основные свойства соединений Хрома
Степень окисления Хрома |
Формулы оксидов |
Формулы гидратных соединений |
Названия соединений |
Свойства соединений |
+2 |
СrО |
Сr(ОН)2 |
Хром (II) гидроксид |
Основные |
+3 |
Сr2О3 |
Сr(ОН)3 НСrО2 |
Хром (III) гидроксид Хромитная кислота |
Амфотерные |
+6 |
СrО3 |
Н2СrО4 Н2Сr2О7 |
Хроматная кислота Дихромароматная кислота |
Кислотные |
Zn(OH)2 +2 HCl = ZnCl2 + 2H2О;
Zn(OH)2 +2 КОН(р-н) =K2[Zn(OH)4];
Cr(ОН)3 + З НС1 = СrС13 + З Н2О;
Сr(ОН)3 +З КОН(р-н) =К3[Сr(ОН)6].
В водных растворах амфотерные электролиты (амфолиты) диссоциируют на ионы Гидрогена Н+ и гидроксид-ионы ОН- по уравнению
Zn(ОН)2 + 2 Н2О ↔ 2 Н+ + [Zn(ОН)4]2- (как кислота);
Zn(OH)2 ↔ ZnOH+ + OH- І ступень (как основание);
ZnOH+ ↔ Zn2+ + OН- II ступень.
Средние соли катионов третьей группы - хлориды, нитраты, сульфаты и ацетаты - хорошо растворяются в воде, а сульфиды, карбонаты и фосфаты в воде не растворимы, но хорошо растворяются в кислотах.
Поскольку растворимые в воде соли образованны слабыми основаниями типа Zn(OH)2, А1(ОН)3, Сr(ОН)3, то практически все они гидролизуются (см. п. 3.5), например:
Zn2+ + НОН ↔ ZnOH+ + Н+.
В результате гидролиза образуются основные соли, а реакция среды становится кислой (рН < 7).
Соли, которые содержат катион слабого основания и анион слабой кислоты, например карбонаты или сульфиды Алюминия и Хрома (III), в водных растворах не существуют, поскольку они гидролизуются полностью:
Cr2(CО3)3 + З НОН → 2Сr(ОН)3↓ +3 СО2;
Cr2S3 + 6 HОН →2 Сr(ОН)3↓ +3 H2S.
Алюминий — один из наиболее распространенных металлов земной коры (8% по массе). Он принадлежит к химически активным элементам, его соединению обнаруживают типичные амфотерные свойства. Связи в них имеют смешанный ионно-ковалентный характер, степень окисления является величиной постоянной и равняется +3.
В водных растворах гидратированные катионы Алюминия [А1(Н2O)6]3+ и Цинка [Zn(H2O)4]2+ бесцветны, а Хрома(ІІІ) [Сr(Н2O)6]3+ — окрашенны в зеленый цвет, что и используют в качественном анализе.
Арсен, как р-элемент VA группы ПСЭ, образует катионы со степенями окисления +3 и +5. Поскольку это амфотерный химический элемент, то в щелочной среде существуют анионы кислородсодержащих кислот AsО33- и AsО43- (арсенит и арсенат-ионы), а в кислой — катионы:
AsО33- ↔ As(OH)3 ↔ As3+
Щелочная Нейтральная Кислая
среда среда среда
Таким образом, определение Арсению в форме катионов проводят в сильнокислой среде, а в форме анионов - в слабокислой, нейтральной или щелочной.
Соединения Арсению очень токсичны, поэтому работа с ними требует особой осторожности и четкого соблюдении правил техники безопасности.
