
- •Процессы окисления
- •Характеристика процессов окисления Определение и классификация реакций окисления
- •Окислительные агенты и техника безопасности в процессах окисления Окислительные агенты
- •Молекулярный кислород
- •Азотная кислота
- •Пероксидные соединения
- •Техника безопасности процессов окисления
- •Энергетическая характеристика реакций окисления
- •Радикально-цепное окисление
- •Кинетика и катализ реакции радикально-цепного окисления
- •2Roo молекулярные продукты
- •2Rсоoo молекулярные продукты
- •Селективность окисления
- •Реакторы процессов жидкофазного окисления
- •Окисление углеводородов в гидропероксиды. Синтез фенола и ацетона
- •Получение гидропероксидов
- •Кислотное разложение гидропероксидов
- •Окисление парафинов
- •Окисление низших парафинов в газовой фазе
- •Окисление н-парафинов в спирты
- •Окисление парафинов в карбоновые кислоты
- •Окисление парафинов с4с8
- •Окисление твердого парафина в сжк
- •Окисление нафтенов и их производных
- •Циклоалканы и дикарбоновые кислоты
- •Окисление нафтенов в спирты и кетоны
- •Каталитическое окисление
- •Термическое окисление циклоалканов в присутствии борной кислоты
- •Получение дикарбоновых кислот
- •Окисление метилбензолов в ароматические кислоты
- •Производство диметилтерефталата
- •Одностадийное окисление метилбензолов в растворе уксусной кислоты
- •Окисление насыщенных альдегидов и кислот Окисление альдегидов
- •Синтез уксусной кислоты
- •Совместный синтез уксусной кислоты и уксусного ангидрида
- •Гетерогенно-каталитическое окисление углеводородов и их производных
- •Теоретические основы процесса Гетерогенные катализаторы окисления и механизм реакций
- •Кинетика и селективность гетерогенно-каталитического окисления
- •Реакторы процессов гетерогенно-каталитического окисления
- •Окисление олефинов по насыщенному атому углерода
- •Окисление пропилена в акролеин
- •Получение акриловой кислоты
- •Окислительный аммонолиз углеводородов
- •Синтез синильной кислоты
- •Окислительный аммонолиз олефинов
- •Окислительный аммонолиз метилбензолов
- •Синтез фталевого и малеинового ангидридов
- •Производство фталевого ангидрида
- •Производство малеинового ангидрида
- •Производство этиленоксида
- •Окисление этилена воздухом
- •Окисление этилена кислородом
- •Окисление олефинов в присутствии металлокомплексных катализаторов
- •Эпоксидирование ненасыщенных соединений
- •Эпоксидирование гидропероксидами
- •Технология совместного синтеза пропиленоксида и стирола
- •Окисление и окислительное сочетание олефинов при катализе комплексами металлов Синтез карбонильных соединений
- •Производство ацетальдегида из этилена
- •Синтез винилацетата из этилена (метод ацетоокисления)
- •Литература
- •Содержание
Окислительный аммонолиз метилбензолов
Окислительный аммонолиз метилбензолов применяется для синтеза динитрилов изо- и терефталевой кислот (фталонитрилы) из м-, п-ксилола и их смесей. Терефталонитрил – промежуточный продукт для синтеза терефталевой кислоты высокой чистоты. Изофталонитрил применяют для получения м-ксилидендиамина – мономера для синтеза термостойких полиамидов и т.д.
Окислительный аммонолиз ксилолов протекает ступенчато и сопровождается побочным образованием СО2 и синильной кислоты:
С
 6Н4(СН3)2
6Н4(СН3)2![]() СН3С6Н4СN
NСС6Н4СN
СН3С6Н4СN
NСС6Н4СN
терефталонитрил
СО2 + НСN динитрилфталевой к-ты
Промежуточный толуилонитрил можно выделить из смеси и возвратить на окислительный аммонолиз. Наиболее эффективным катализатором для этого процесса являются смеси оксидов ванадия и хрома, ванадия и молибдена, титана и молибдена, титана и висмута. Температура составляет 350-4800С, давление – атмосферное, время контакта 12 секунды. Применяют реакторы со стационарным и псевдоожиженным слоем. В отличие от синтеза акрилонитрила, используют значительный избыток NН3 и О2 (в виде воздуха) по отношению к ксилолу – 23-х кратный от стехиометрического.
Реакционный узел оформлен также, как и для процесса получения акрилонитрила, но разделение существенно различается: прежде отделяются малолетучие нитрилы, затем извлекают из реакционных газов аммиак, направляя остаточный газ на дожигание.
Синтез фталевого и малеинового ангидридов
Фталевый ангидрид применяют для производства алкидных полимеров, поликонденсацией его с глицерином, пентаэритритом и другими многоатомными спиртами.
Эфиры фталевой кислоты со спиртами С4С6 широко используются как пластификаторы полимерных материалов, а ее метиловые и этиловые эфиры как препараты для отпугивания кровососущих насекомых, для синтеза красителей.
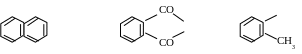
СН3
![]() О
О
![]()
Малеиновый ангидрид применяют для производства ненасыщенных полиэфиров. Малеиновый альдегид растворим в воде и гидролизуется в малеиновую кислоту, которая при нагревании изомеризуется в фумаровую кислоту (транс-изомер) – это необходимо учитывать при синтезе малеинового ангидрида.
Основной метод получения состоит в газообразном окислении бензола воздухом, но сейчас в качестве сырья все больше используют дешевые и менее дефицитные бутены и даже бутан.
Производство фталевого ангидрида
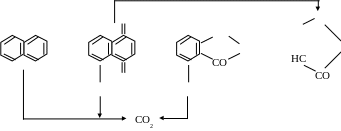
О СО
СО НС
![]() О
О
О
О![]()
О
1,4-нафтохинон фталевый ангидрид малеиновый ангидрид
Фталевый ангидрид стабилен к дальнейшему окислению, поэтому реакцию ведут до практически полной конверсии нафталина. Выход 1,4-нафтохинона и малеинового ангидрида настолько мал, что их невыгодно выделять из полученных смесей, а основным побочным процессом является окисление до СО2. Наиболее эффективным катализатором оказался V2O5 с добавкой K2SO4 на силикагеле; температура составляет 360-4000С, выход – 90 %.
При окислении о-ксилола схема процесса следующая:
 СО
СО

 СО
СО
СНО +О2
О + 4СО2
 СО
СО
СО2
Селективность о-ксилола значительно низкая, выход малеинового ангидрида возрастает до 5-8 % и поэтому его выгодно выделять в качестве товарного продукта. Лучшим катализатором является оксидный ванадий-титановый контакт, на котором выход фталевого ангидрида составляет 7075 %, при температуре 3704000С.
По технологии окисление нафталина и окисление о-ксилола аналогичны. Существуют установки, на которых можно перерабатывать оба вида сырья при атмосферном давлении и большом избытоке воздуха, обеспечивающем концентрацию реагента 0,7-0,9 % (об.), тогда сырье находится вне пределов взрывоопасных концентраций в смеси с воздухом. Наиболее распространеные многотрубные реакторы со стационарным слоем катализатора, охлаждаемые кипящим водным конденсатом или чаще нитрит-нитритной смесью, с производством пара. В последнее время большое внимание уделяется эффективной утилизации тепла, которого хватает для работы установки, и часть генерируемого пара (до 3,6 т на 1 т фталевого ангидрида) используют для других нужд. Температура составляет 360-4000С, селективность – 90 %, катализатор – V2O5 c K2SO4 на силикагеле.
Технологическая схема получения фталевого ангидрида из нафталина приведена на рис.15.
