
- •Передмова
- •8. Література
- •9. Додатки
- •1. Елементи астрофотометрії
- •2. Око людини як оптична система і приймач випромінювання а ) Будова ока та його характеристики як оптичної системи
- •Б) Око як приймач випромінювання
- •3. Шкала зоряних величин
- •4. Окомірна оцінка блиску зірок
- •5. Візуальний астрофотометр
- •5. Методичні вказівки щодо виконання робочого завдання
- •6. Контрольні запитання
- •8. Література
- •9. Додатки
- •1. Фотографія в астрономічних дослідженнях
- •2. Фотографічний процес а) будова фотоматеріалів
- •Б) технологія виготовлення фотоматеріалів
- •В) механізм виникнення схованого фотографічного зображення
- •Г) хіміко-фотографічна обробка світлочутливих матеріалів
- •3. Елементи сенситометрії та структурометрії
- •4. Трубчастий фотометр
- •5. Методичні вказівки щодо виконання робочого завдання
- •6. Контрольні запитання
- •Звіт про лабораторну роботу має містити:
- •8 Література
- •9. Додатки
- •1. Принцип та методи фотографічної фотометрії
- •2. Зоряні величини та показник кольору
- •3. Методи абсолютної фотографічної фотометрії
- •4. Абсолютна фотометрія протяжних об'єктів
- •5. Відносні фотометричні вимірювання
- •6. Позафокальна фотометрія
- •7. Інтернаціональні фотометричні стандарти
- •8. Похибки у фотографічній фотометрії
- •7.4 Телескоп і його характеристики
- •1. Мета роботи
- •2. Об'єкт та засоби досліджень
- •3. Робоче завдання
- •4. Програма підготовки до виконання робочого завдання
- •6. Методичні вказівки щодо виконання робочого завдання
- •5. Контрольні запитання
- •8. Література
- •9. Додаток I
- •1. Призначення телескопа
- •2. Характеристики лінз і дзеркал
- •Якщо предмет нескінченно віддалений, то:
- •9.3. Телескоп як афокальна система.
- •4. Характеристики телескопа
- •5. Типи окулярів
- •6. Монтування телескопа
- •Додаток II
- •7.5 Дослідження оптики астрономічних об'єктивів методом гартмана
- •1. Мета роботи
- •2. Об'єкт і засоби досліджень
- •3. Робоче завдання
- •4. Програма підготовки до виконання робочого завдання
- •5. Методичні вказівки щодо виконання робочого завдання
- •6. Контрольні запитання
- •Звіт про лабораторну роботу має містити:
- •8. Література
- •9. Додаток
- •1. Аберації оптичних систем
- •1.1 Причини та класифікація аберацій
- •1.2 Критерій Релея
- •1.3. Геометричні аберації
- •1.4. Хроматичні аберації
- •1.4.1 Дисперсія скла. Оптичні матеріали
- •1.4.2 Типи хроматичної аберації
- •2. Астрономічні об'єктиви
- •3. Метод Гартмана
- •4. Вимірювальний мікроскоп «Мир-12»
- •5. Приклад таблиць для оформлення результатів роботи.
- •6. Контрольні запитання
- •8. Література
- •9. Додаток I
- •1. Завдання фотографічної астрометрії
- •2. Телескоп як камера
- •3. Будова та класифікація астрографів
- •4. Наведення телескопа за координатами
- •5. Фактори що визначають якість астронегатива
- •6. Правила оформлення астронегативів та запису спостережень
- •7. Ототожнення зірок фотознімка ділянки неба за допомогою зоряного атласу й каталогу
- •8. Вимірювання астрографічних знімків
- •Річна прецесія по схиленню (р )
- •7.7 Основи астроспектроскопії вивчення призмового спектрографа
- •1. Мета роботи
- •2. Об'єкт і засоби дослідження
- •3. Робоче завдання
- •4. Програма підготовки до виконання робочого завдання
- •5. Методичні вказівки щодо виконання робочого завдання
- •6. Контрольні запитання
- •8. Література
- •9. Додаток I
- •1. Загальні характеристики спектральних приладів
- •2. Спектральні призми
- •3. Призмові спектрографи
- •4. Призмові спектрографи для ультрафіолетової ділянки спектра
- •5. Градуювальна та дисперсійна криві спектрографа
- •6. Оптичні спектри. Спектральний аналіз
- •6. Спектр і хімічний склад Сонця
- •Додаток II
- •Спектри Сонця та деяких хімічних елементів
6. Оптичні спектри. Спектральний аналіз
Оптичні спектри — спектри електромагнітного випромінювання в інфрачервоному, видимому та ультрафіолетовому діапазонах шкали електромагнітних хвиль. Оптичні спектри поділяють на:
- спектри випромінювання (емісійні спектри);
- спектри поглинання (абсорбційні спектри);
- спектри розсіяння;
- спектри відбивання.
Спектри
випромінювання отримуються від джерел
світла при розкладі його випромінювання
за довжинами хвиль спектральними
приладами і характеризуються функцією
f(
),
що показує розподіл енергії випромінювання
залежно від довжини хвилі
(енергія
розраховується на деякому інтервалі
![]() ).
).
Спектри
поглинання і розсіяння отримуються при
проходженні світла через речовину з
наступним розкладом випромінювання за
.
Спектри поглинання, розсіювання та
відбивання характеризуються частиною
енергії світла кожної довжини хвилі,
що відповідно поглинуто К(![]() )
, розсіяно
(
)
і відбито R(
).
)
, розсіяно
(
)
і відбито R(
).
За зовнішнім виглядом оптичні спектри поділяють на лінійчасті, які складаються з окремих ліній, що відповідають дискретним значенням , смугасті, які складаються із окремих смуг, кожна з яких охоплює деякий інтервал , суцільні (неперервні), які охоплюють широкий діапазон довжин хвиль. Строго кажучи, окрема спектральна лінія також не відповідає дискретному значенню довжини хвилі, а завжди має певну кінцеву ширину .
Спектри виникають при квантових переходах між рівнями енергії атомів, молекул, а також твердих тіл і рідин. Спектри випромінювання відповідають можливим квантовим переходам із верхніх рівнів на нижній, спектри поглинання – із нижніх рівнів на верхні.
Вигляд оптичних спектрів залежить від стану речовини. Якщо речовина знаходиться в стані термодинамічної рівноваги з випромінюванням, вона емітує неперервний спектр, розподіл енергії в якому за довжиною хвилі визначає закон випромінювання Планка. В переважній більшості випадків термодинамічна рівновага випромінювання з речовиною відсутня, і спектр має складніший вигляд. Наприклад, для атомів характерні лінійчасті (атомні), а для простих молекул типовими будуть смугасті (молекулярні) спектри.
Атомні спектри – оптичні спектри, отримувані при випромінюванні або поглинанні електромагнітних хвиль вільними (слабко зв'язаними) атомами чи іонами (наприклад, в газах); вони лінійчасті, бо складаються з окремих спектральних ліній. Слід зауважити, що спектри іонів зміщені відносно спектрів нейтральних атомів в область вищих частот.
Положення спектральних ліній в атомних спектрах визначаються певними закономірностями і в найпростішому випадку утворюють спектральні серії. Кожна спектральна серія утворюється можливими квантовими переходами з вище розміщених рівнів енергії на один і той же нижче розміщений рівень (для спектрів випромінювання). Проміжки між лініями однієї серії поступово зменшуються в напрямку зростання частоти – лінії сходяться до межі серії.
У спектрах атомів представлені не всі можливі квантові переходи, а лише дозволені правилами відбору. Кількісною характеристикою дозволених оптичних переходів є їх ймовірність, яка визначає інтенсивність лінії у спектрі. Ймовірність переходів пов’язана з коефіцієнтами Ейнштейна і в найпростішому випадку розраховується методами квантової механіки.
Молекулярні спектри – спектри випромінювання, поглинання і комбінаційного розсіювання, що належать вільним або слабко зв'язаним між собою молекулам. Типовими молекулярними спектрами є смугасті спектри, які спостерігаються у вигляді сукупності вузьких смуг в ультрафіолетовій, видимій і інфрачервоній ділянках спектра; при достатній роздільній здатності спектрального приладу молекулярні смуги розпадаються на сукупність близько розміщених ліній. Структура молекулярних спектрів ускладнюється із зростанням кількості атомів у молекулі.
Спектроскопія – розділ фізики, присвячений вивченню спектрів електромагнітного випромінювання.
Спектральний аналіз – фізичні методи кількісного та якісного визначення складу речовини, що ґрунтуються на отриманні й дослідженні її спектра. Теоретичною основою спектрального аналізу є квантова механіка, яка пояснює: дискретність енергостанів, дозволені переходи між ними, зовнішній вплив, взаємодію систем і таке інше. Експериментальною основою спектрального аналізу є спектроскопія атомів і молекул.
Якісний атомний спектральний аналіз реалізується шляхом зіставлення (ототожнення) ліній спектра досліджуваного об'єкта зі спектральними лініями відомих елементів, довжини хвиль яких наведені в спеціальних таблицях і атласах.
Кількісний спектральний аналіз ґрунтується на співвідношенні, що пов'язує концентрацію с елемента з відношенням інтенсивності лінії шуканої домішки I1 та лінії порівняння I2 :
![]()
або
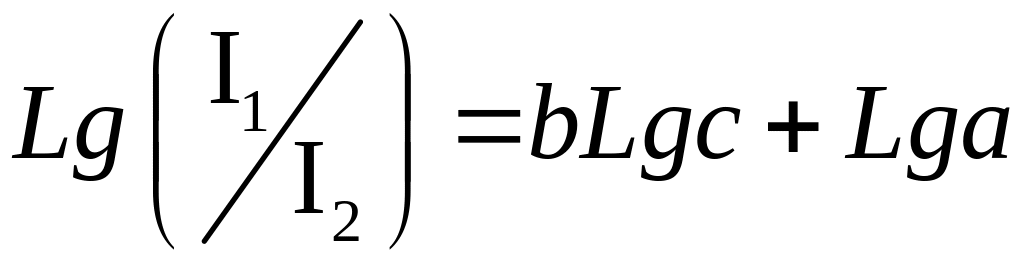 (7.31)
(7.31)
Постійні
а і b визначаються експериментальним
шляхом. За допомогою стандартних зразків
(не менше трьох) можна побудувати графічну
залежність
 від
від
![]() (градуювальна крива) та визначити за
нею а і b. Значення I1
та I2
вимірюють безпосередньо шляхом
фотометрування.
(градуювальна крива) та визначити за
нею а і b. Значення I1
та I2
вимірюють безпосередньо шляхом
фотометрування.
