
- •Введение
- •Физическая химия § 1. Предмет физической химии. Ее значение
- •§ 2. Краткий очерк истории развития физической химии
- •§ 3. Разделы физической химии. Методы исследования
- •Глава I первый закон термодинамики § 1. Энергия. Закон сохранения и превращения энергии
- •§ 2. Предмет, метод и границы термодинамики
- •§ 3. Теплота и работа
- •§ 4. Эквивалентность теплоты и работы
- •§ 5. Внутренняя энергия.
- •§6. Первое начало термодинамики.
- •§ 7. Уравнения состояния.
- •§ 8. Калорические коэффициенты
- •§ 9. Работа различных процессов
- •§ 10. Теплоемкость. Вычисление теплоты различных процессов
- •§ 11. Энтальпия
- •§ 12. Применение первого закона термодинамики к идеальным газам
- •Глава II. Второй закон термодинамики
- •§ 1. Самопроизвольные и несамопроизвольные процессы
- •§ 2. Второй закон термодинамики
- •§ 3. Методы расчета энтропии
- •§ 4. Постулат Планка. Абсолютные значения энтропии
- •Глава III энергия гельмгольца. Энергия гиббса. Приложения второго закона термодинамики
- •§ 1. Энергия Гельмгольца
- •§ 2. Энергия Гиббса
- •§ 3. Фазовые переходы. Уравнение Клапейрона—Клаузиуса
- •§ 4. Фазовые переходы первого рода. Плавление. Испарение
- •§ 5. Зависимость давления насыщенного пара от температуры
- •Глава IV термодинамика растворов. Газовые смеси (растворы)
- •§ 1. Растворы (определение). Концентрация.
- •§ 2. О молекулярной структуре растворов
- •§ 3. О теориях растворов
- •Глава V. Равновесие: жидкий раствор — насыщенный пар
- •§ 1. Давление насыщенного пара бинарных жидких растворов
- •§ 2. Закон Рауля. Идеальные растворы. Предельно разбавленные растворы
- •§ 3. Реальные растворы. Положительные и отрицательные отклонения от закона Рауля
- •§ 4. Диаграммы равновесия жидкость - пар в бинарных системах. Первый закон Коновалова. Фракционная перегонка
- •§ 5. Температура кипения растворов нелетучих веществ. Эбуллиоскопия Температура замерзания растворов нелетучих веществ. Криоскопия
- •§ 6. Второй закон Коновалова. Азеотропные растворы
- •Глава VI равновесие жидких растворов с газами. Некоторые классы растворов
- •§ 1. Растворимость газов в жидкостях
- •§ 2. Влияние давления на растворимость газов. Закон Генри
- •§ 3. Зависимость растворимости газов от температуры
- •§ 4. Влияние третьего компонента на растворимость газов
- •§ 5. Совместная растворимость нескольких газов
- •Глава VII. Предмет коллоидной химии
- •§1. Определение предмета коллоидной химии
- •§2. Признаки объектов коллоидной химии
- •§3. Значение коллоидной химии
- •Глава VIII. Поверхностные явления и адсорбция
- •§1. Поверхностное натяжение.
- •§2. Когезионные и поверхностные силы
- •§3. Зависимость энергетических параметров поверхности от температуры
- •5. Самопроизвольное уменьшение поверхностной энергии и формирование поверхностного слоя
- •Глава IX. Адсорбция и поверхностное натяжение
- •§1. Виды адсорбции, ее количественные характеристики и их связь с параметрами системы
- •§2. Фундаментальное адсорбционное уравнение Гиббса и примеры его применения
- •§3. Поверхностная активность. Поверхностно-активные и инактивные вещества
- •§4. Мономолекулярная адсорбция. Изотерма адсорбции Ленгмюра
- •§5. Теория полимолекулярной адсорбции бэт
- •§6. Изотермы адсорбции и поверхностного натяжения растворов пав.
- •§7. Классификация и общая характеристика поверхностно-активных веществ. Правило Дюкло – Траубе
- •§8. Хроматография. Основы метода.
- •Глава хi. Адгезия, смачивание и растекание жидкостей
- •§1. Адгезия и работа адгезии
- •§2. Смачивание и краевой угол. Закон Юнга
- •§3. Связь работы адгезии с краевым углом
- •§4. Флотация
- •§5. Моющее действие пав. Роль пав в повышении нефтеотдачи пластов
- •Глава XII. Капиллярные явления
- •§1. Влияние кривизны поверхности на внутреннее давление. Закон Лапласа
- •§2. Капиллярные явления. Формула Жюрена
- •§3. Роль капиллярных явлений при вытеснении нефти водой из пористых сред
- •Глава XIII. Дисперсные системы
- •§1. Классификация дисперсных систем
- •§2. Два метода получения дисперсных систем – диспергирование и конденсация
- •§3.Молекулярно-кинетические свойства дисперсных систем
- •§4. Устойчивость дисперсных систем
- •§5. Седиментация
- •§6. Седиментационный анализ дисперсности
- •§7. Диффузионно-седиментационное равновесие.
- •§8. Агрегативная устойчивость дисперсных систем
- •§9. Стабилизация и разрушение эмульсий
- •Дисперсные системы с жидкой дисперсной фазой и жидкой дисперсионной средой называются эмульсиями.
- •Глава XIV. Структурно-механические свойства дисперсных систем
- •§1. Основные понятия и идеальные законы реологии
- •§2. Вязкость
- •§3. Моделирование реологических свойств тел
- •§4. Классификация дисперсных систем по структурно-механическим свойствам
- •§5. Реологические свойства дисперсных систем
- •Д. Ю. Митюк, в. И. Фролов физическая и коллоидная химия
- •117917, Москва, Ленинский проспект, д. 65
§ 3. Методы расчета энтропии
Уравнения (II, 1) и (II, 1а), определяющие энтропию, являются единственными исходными уравнениями для термодинамического расчета изменения энтропии системы. Заменяя элементарную теплоту в уравнении (II, 1а) ее выражениями через калорические коэффициенты (см. уравнения (I, 10) и (I, 10а)), получаем для равновесных процессов:
dS
=
![]() =
=
![]() +
+
![]() (II,
3)
(II,
3)
dS
=
![]() +
+
![]() (II,
3а)
(II,
3а)
Уравнения (II, 3) и (II, 3а) являются полными дифференциалами энтропии как функции переменных V, Т или P, Т. Коэффициенты этих уравнений - частные производные энтропии по соответствующим переменным.
Подставив в уравнение (II, 3) значения калорических коэффициентов для одного моля идеального газа: l = P = RT/V [уравнение (I, 24)] и h = –V = –RT/P [уравнение
(I,
25)![]() и полагая СV
и СP
независимыми
от температуры (что допустимо лишь в
небольших температурных интервалах),
получим после интегрирования в известных
пределах:
и полагая СV
и СP
независимыми
от температуры (что допустимо лишь в
небольших температурных интервалах),
получим после интегрирования в известных
пределах:
S
=
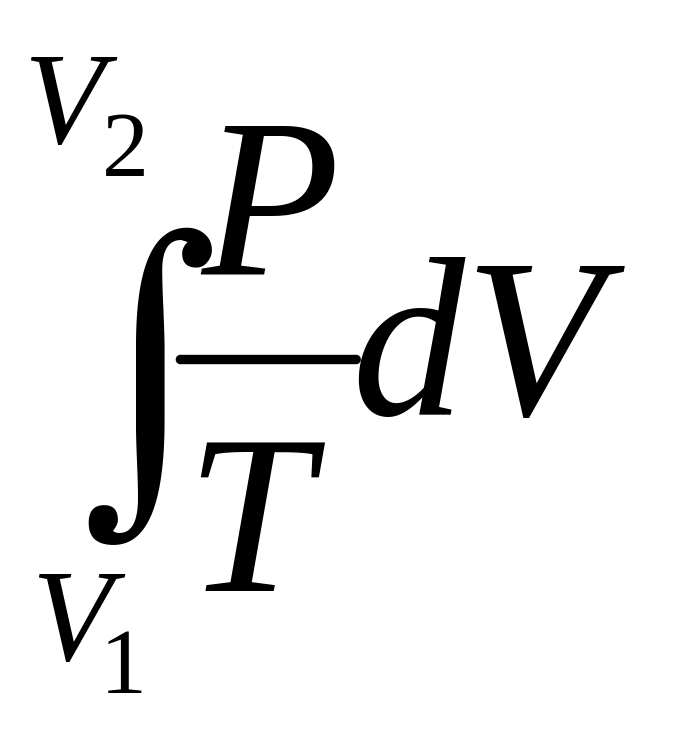 +
+
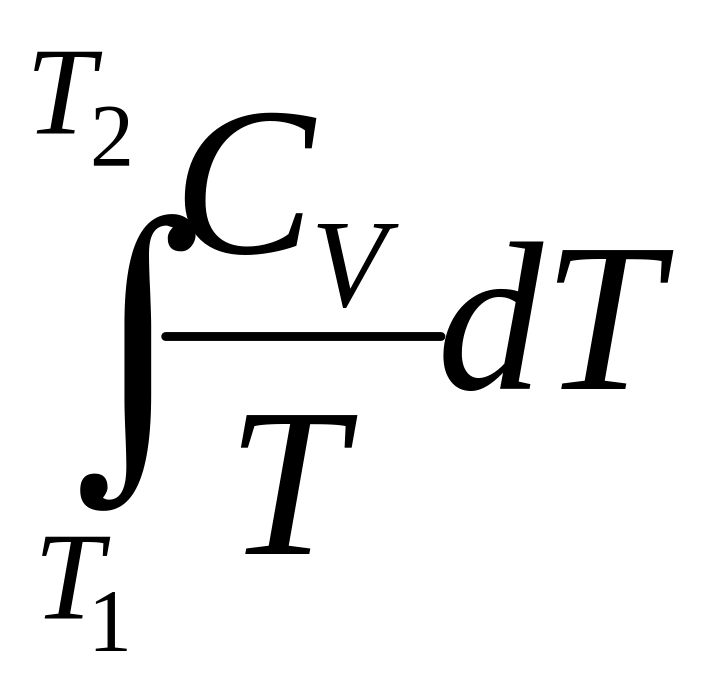 = R ln
= R ln![]() +
+
![]()
![]() (II,
4)
(II,
4)
S =
-
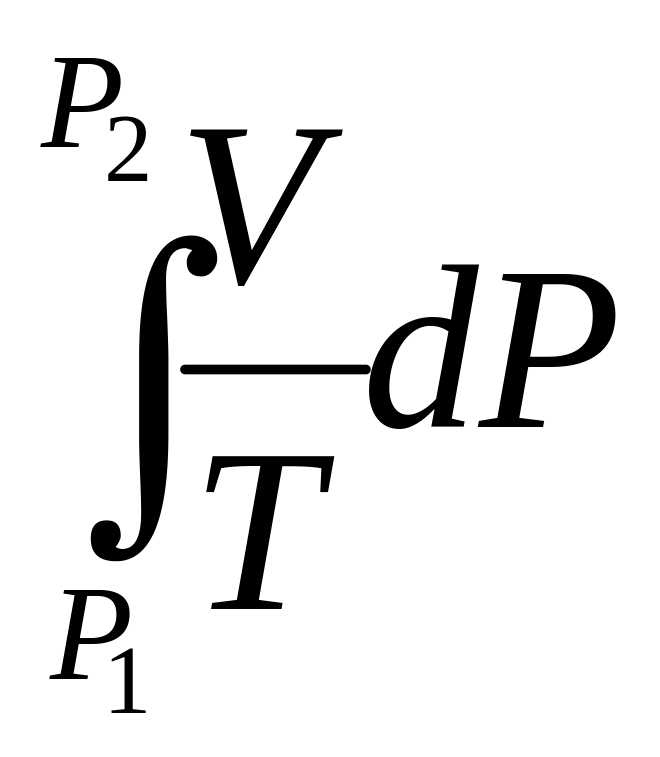 +
+
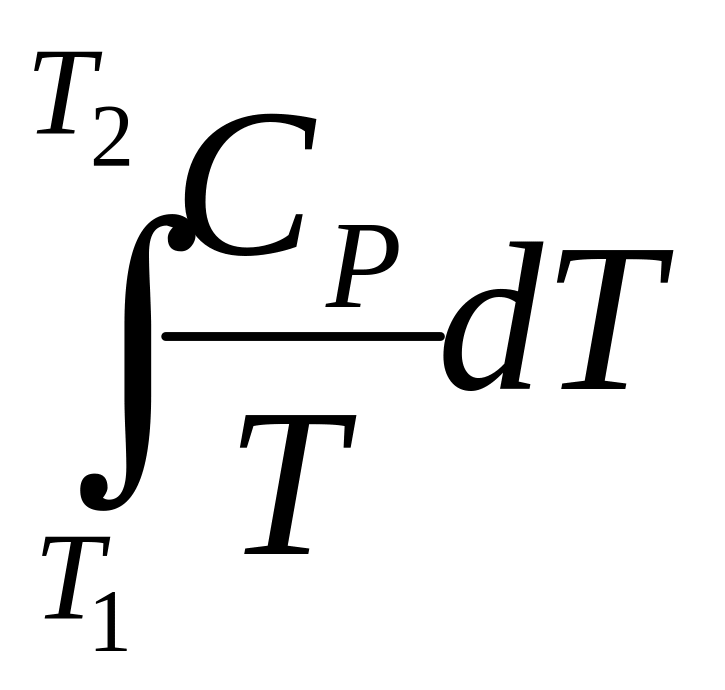 = -R ln
= -R ln![]() + CP
ln
+ CP
ln![]() (II,
4а)
(II,
4а)
Применим полученные выше соотношения для расчетов изменения энтропии при некоторых процессах:
1. Фазовые превращения (изотермические процессы; Т = const):
S2
– S1
= S
=
![]() =
=
![]() =
=
![]() (II,
5)
(II,
5)
Так, например, теплота плавления бензола равна 9,764 кДж/моль; температура плавления tпл. = 5,5°С. Следовательно, изменение энтропии 1 моль бензола при плавлении (энтропия плавления) равно:
Sпл.
=
![]() 35,06
Дж/моль
35,06
Дж/моль![]()
2. Нагревание при постоянном давлении (изобарный процесс; P = const). Из уравнения (III, 18а) получаем:
S = (II, 6)
Найдем изменение энтропии одного моля алюминия при нагревании от 25 до 600 °С. Истинная мольная теплоемкость алюминия может быть выражена уравнением:
Ср= 565,5 + 0,290 Т. По уравнению (II, 4а) изменение энтропии будет равно:
S
=
![]() = 565,5
= 565,5
![]() 2,303
2,303
![]() + 0,290(873 – 298) = 608,5 + 166,8 = 775,3 Дж/мольK
+ 0,290(873 – 298) = 608,5 + 166,8 = 775,3 Дж/мольK
§ 4. Постулат Планка. Абсолютные значения энтропии
По уравнению (II, 3) невозможно вычислить абсолютное значение энтропии системы. Такую возможность дает новое, недоказуемое положение, не вытекающее из двух законов термодинамики, которое было сформулировано М.Планком (1912). Согласно этому положению, называемому постулатом Планка, энтропия индивидуального кристаллического вещества при абсолютном нуле равна нулю:
S0 = 0
Строго говоря, постулат Планка справедлив только для индивидуальных веществ, кристаллы которых идеально построены (в кристаллической решетке все узлы заняты молекулами или атомами, правильно чередующимися и закономерно ориентированными). Такие кристаллы называются идеальными твердыми телами. Реальные кристаллы не являются таковыми, так как их кристаллическая решетка построена не идеально.
Энтропия кристаллической решетки, построенной в некоторой степени беспорядочно, больше энтропии идеально построенной кристаллической решетки. Поэтому реальные кристаллы и при 0 К обладают энтропией, большей нуля. Однако энтропии реальных хорошо образованных кристаллов индивидуальных веществ при абсолютном нуле невелики.
В соответствии с постулатом Планка уравнение (II, 6) для идеального твердого тела примет вид:
![]() =
=
![]() (II,
7)
(II,
7)
Постулат Планка используется при термодинамическом исследовании химических процессов для вычисления абсолютных значений энтропии химических соединений - величин, которые имеют большое значение при расчете химических равновесий.
Энтропия широко используется в технической термодинамике (теплотехнике), как один из важных параметров рабочего тела в тепловой машине, например, водяного пара. Величины энтропии водяного пара в данном состоянии вычисляются по сравнению с некоторым стандартным состоянием - обычно 0°С и 1 amм. Эти значения энтропии используются для построения так называемых энтропийных диаграмм состояния водяного пара в координатах S—Т или S—H (диаграмма Молье). В таких диаграммах подобно диаграммам V—P, можно изображать различные процессы, протекающие в рабочем теле тепловой машины и составляющие рабочие циклы машины.
В заключение следует отметить, что нам не придется углубляться в область термодинамики. Наша цель лишь проиллюстрировать основные идеи этой науки и объяснить причины, по которым возможно основываться на ее аргументах.
Наконец, два закона термодинамики часто формулируют так:
Первый закон: Энергия Вселенной всегда постоянна.
Второй закон: Энтропия Вселенной всегда возрастает.
Несмотря на некоторые недостатки приведенных выше формулировок обоих законов, они легко запоминаются и дают представление, о чем собственно идет речь.
Напомним, что второй закон термодинамики определяет критерии самопроизвольного протекания процессов в изолированных системах. Однако подобные условия (отсутствие обмена энергией и веществом с окружающей средой) реализуются сравнительно редко. Поэтому представляется важным сформулировать подобного рода критерии для закрытых систем, где возможен обмен энергией с окружающей средой. Для этого нам потребуется определить две новые функции состояния – энергию Гельмгольца и энергию Гиббса.
