
- •Основні види сировини
- •Зернові культури
- •Будова зерна
- •Хімічний склад зерна
- •Хімічний склад меляси
- •Мікрофлора меляси
- •Коротка характеристика хімічного складу тростинної та рафінадної меляс
- •Нетрадиційні види сировини
- •Топінамбур
- •Цикорій
- •Молочна сироватка
- •Допоміжні матеріали
- •Кислоти
- •Сірчана кислота
- •Соляна кислота
- •Антисептики та миючі засоби Хлорне вапно
- •Формалін
- •Сульфонол
- •Каустична сода
- •Контрольні питання і завдання
- •Розділ 2
- •Приймання зерна
- •Приймання меляси
- •Зберігання сировини
- •Дихання
- •Зміни хімічного складу сировини
- •Випаровування та поглинання вологи
- •Дія від'ємних температур
- •Вплив мікроорганізмів на зберігання сировини
- •Зберігання зерна
- •Зберігання меляси
- •Контрольні питання і завдання
- •Розділ з
- •Підготовка зерна
- •Повітряно-ситове сепарування
- •Магнітне сепарування
- •Відділення насіння бур'янів
- •Підготовка меляси
- •Підкислення і асептування меляси
- •Стерилізація меляси
- •Змішування меляси з водою
- •Кларифікація мелясних розчинів
- •Контрольні питання і завдання
- •Розділ 4
- •Оцукруючі матеріали
- •Характеристика ферментів загальні поняття про ферменти
- •Механізм дії ферментів
- •Концентрація ферменту
- •Температура
- •Активатори та інгібітори ферментів
- •Оксидоредуктази
- •Трансферази
- •Гідролази
- •Ізомерази
- •Активність ферментів
- •Виробництво солоду
- •Замочування зерна
- •Фізико-хімічні процеси під час замочування зерна
- •Біохімічні процеси при замочуванні зерна
- •Способи замочування зерна
- •Пророщування зерна Теоретичні основи пророщування зерна
- •Морфологічні зміни при пророщуванні зерна
- •Біохімічні зміни в зерні при пророщуванні
- •Хімічні зміни зерна при пророщуванні
- •Оптимізація процесів солодорощення
- •Способи солодорощення
- •Пророщування зерна в пневматичній солодовні
- •Токове солодорощення
- •Витрати зерна на солод
- •Виробництво мікробних ферментних препаратів
- •Продуценти ферментів
- •Контрольні питання і завдання
- •Ємкісна (мічурінська) апаратурно-технологічна схема
- •Трубчаста (мироцька) апаратурно-технологша схема
- •Контрольні питання і завдання
- •Розділ 6 спиртові дріжджі
- •Температура і рН
- •Склад живильного середовища Потреба дріжджів у живильних речовинах
- •Види і джерела живлення
- •Інші фактори
- •Аеробний розпад вуглеводів
- •Молочнокислі бактерії
- •Оцтовокислі бактерії
- •Маслянокислі бактерії
- •Гнилісні бактерії
- •Мікрофлора води та повітря
- •Розділ 7
- •Розділ 8
- •Характеристика дріжджів
- •Приготування чистої культури дріжджів
- •Періодичне культивування
- •Культивування дріжджів у виробництві спирту із меляси
- •Розділ 9 зброджування сусла
- •Періодичний спосіб
- •Безперервно-проточний спосіб
- •Циклічний спосіб
- •Технологічні показники бродіння
- •Порівняльна характеристика способів зброджування
- •Теоретичні основи процесів перегонки і ректифікації
- •Одержання спирту-сирцю
- •Непрямої дії
- •Брагоректифікаційна установка побічно-прямотечійної дії
- •Виділення сивушного масла
- •Одержання технічного спирту
- •Одержання абсолютного спирту
- •Умови безпечної експлуатації ректифікаційних установок
- •Розділ 11
- •Вихід спирту
- •Облік і зберігання спирту
- •Розділ 12
- •Сушка дріжджів
- •Термоліз дріжджів
- •Упарювання мелясної барди
- •Склад газів спиртового бродіння
- •Очистка діоксиду вуглецю від домішок
- •Технологія рідкого дІоксиду вуглецю
- •Розділ 13
- •Характеристика стічних вод
- •Механічні способи
- •Хімічні способи
- •Фізико - хімічні способи
- •Біологічні способи
- •14.1. Використання спирту етилового технічного як органічної сировини
- •14.2. Застосування спирту етилового як моторного палива
- •14.3. Виробництво спирту етилового технічного з нехарчової сировини
- •14.4. Виробництво спирту етилового технічного з вуглеводовм1сної сировини
- •14.5. Брагоректифікаційні установки для виробництва сет з вуглеводовмісної сировини
- •14.6. Дегідратація етилового спирту
- •14.8. Перспективні напрями використання спирту етилового технічного в україні
- •Контрольні питання і завдання
- •Розділ 15
- •15.1 Маловідходні та безвідходні технології
- •15.2 Основні напрями створення мало-та безвідходних технологій
- •15.3 Вторинні енергетичні ресурси та їх раціональне використання
- •15.4 Ресурсо- та енергозберігаюча технологія спиртових бражок
- •15.5 Вплив технологічних параметрів на ефективність дії концентрованих ферментних препаратів
- •15.6 Особливості використання концентрованих
- •Ферментних препаратів у залежності
- •Від технологічної схеми водно-теплової
- •Обробки сировини
- •15.7 Особливості приготування виробничих дріжджів та спиртової бражки
- •15.8 Закордонний досвід комплексної переробки зернової сировини в етиловий спирт
- •15.9 Ресурсо- та енергозберігаюча технологія перегонки та ректифікації спирту
- •15.10 Переробка спиртовмісних вторинних продуктів ректифікації в системі бру мелясних заводів
- •15.11 Виділення етилового спирту з головної фракції, збагаченої метиловим спиртом
- •15.12 Централізована переробка головної фракції етилового спирту
- •15.13 Утилізація концентрату головної фракції
- •15.14 Енергозбереження в процесі перегонки та ректифікації спирту
- •15.15 Брагоректифікацшні установки зі ступеневим використанням теплової енергії
- •15.16 Підвищення теплового потенціалу вторинних енергоресурсів
- •15.17 Енергетична характеристика брагоректифікаційних установок
- •Контрольні питання і завдання
- •Розділ 16
- •Та очистки стічних вод у спиртовій промисловості
- •Актуальні проблеми розділення сумішей за допомогою молекулярних фільтрів у спиртовій промисловості
- •Мембранне газорозділення
- •Мембранна технологія води у спиртовому виробництві
- •Мембранна технологія спирту
- •Контрольні питання і завдання
- •Розділ 17 правила охорони праці на спиртових заводах
- •Основні вимоги з техніки безпеки для апаратника ректифікації спирту, а також для приймальника- здавача та зливальника-розливальника спирту
- •Література
Оксидоредуктази
До класу оксидоредуктаз належать ферменти, які каталізують окисно-відновні реакції. У них проходить перенос електронів або атомів водню від молекули, яка окислюється (донора) до молекули, яка відновлюється (акцептора). До оксидоредуктаз належать ферменти з тривіальними назвами дегідрогеназ, редуктаз, оксидаз, пероксидаз, оксигеназ, гідроксилаз, каталази та ін.
Характерними особливостями дії оксидоредуктаз є такі: перша полягає в тому, що вони утворюють системи (так звані ланцюги окисно-відновних ферментів), у яких здійснюється багатоступеневий перенос атомів водню або електронів від первинного субстрату до кінцевого акцептора, яким є, як правило, кисень. У результаті атоми водню переносяться на кисень і утворюється вода. Ті оксидоредуктази, які переносять водень або електрони безпосередньо на атоми кисню, називаються аеробні дегідрогенази, або оксидази. Із них важливе значення мають глюкозооксидаза і поліфенолоксидаза. На відміну від них, анаеробні дегідрогенази переносять атоми водню й електрони від одного компонента окислювального ланцюга ферментів до іншого без передачі їх на кисневі атоми.
Друга особливість оксидоредуктаз полягає в тому, що вони є двокомпонентними ферментами з дуже обмеженим набором активних груп (коферментів), але
![]()
здатні прискорювати багато різноманітних окисно-відновних реакцій. Це досягається за рахунок того, що один і той же кофермент здатний з'єднуватися з багатьма апоферментами.
Третя особливість оксидоредуктаз як особливого класу ферментів полягає в тому, що вони прискорюють хімічні реакції, пов'язані з вивільненням енергії, яка використовується для біохімічних процесів.
Відомо більше двохсот індивідуальних оксидоредуктаз. Найбільш поширені оксидоредуктази, які мають у своєму складі в якості активної групи нікотинаміда-деніндикуклеотид (НАД) або нікотинамідаденіндинуклеотидфосфат (НАДФ). Утворений фермент-протеїд здатний віднімати від субстратів (спиртів, альдегідів, дика-рбонових і кетокислот та ін.) атоми водню, окислюючи таким чином названі сполуки. Такі фермент-протеїди (піридинпротеїди) є анаеробними дегідрогеназами.
Розглянемо
механізм дії одного із піридинпротеїдів
- алкогольдегідрогенази. Він
складається з двох субодиниць, кожна
із яких має молекулу НАД і атом цинку.
У процесі відняття атому водню від
спирту утворюється потрійний апофермент
-кофермент-субстратний
комплекс, який утримується атомом
цинку. Безпосередньо від
молекули спирту до НАД переходить один
атом водню H+.
Другий
атом водню,
який віднімається від молекули спирту,
втрачає електрон і перетворюється в
протон
(![]() )
і
поступає в реакційне середовище.
Рівняння реакції окислення спирту з
участю НАД має такий вигляд -
)
і
поступає в реакційне середовище.
Рівняння реакції окислення спирту з
участю НАД має такий вигляд -
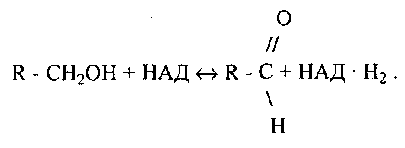
Найбільш складний і найпоширеніший варіант окислювально-відновлюваль-ного процесу в клітині полягає в окисленні атомів водню, які зняті з субстрату первинними дегідрогеназами з участю цитохромної системи. Цитохромну систему утворюють декілька оксидоредуктаз, які мають в якості простетичних груп залізо-порфірини. З'єднуючись з білками різної побудови, залізопорфірини 4 типів дають початок родині хромопротеїдів, які об'єднують загальною назвою - цитохроми. Відомо декілька десятків цитохромів. Вони є переносниками електронів.
Оксидоредуктази
окислюють спирти до відповідних
альдегідів, альдегідів або кетонів
-
до
кислот, відщеплюють атоми водню від![]() -
груп
з утворенням
-
груп
з утворенням
подвійного
зв'язку, окислюють групи![]() або
або![]() .
До
них належать ката-
.
До
них належать ката-
лаза,
яка розкладає перекис водню, і піроксидаза,
яка окислює за допомогою![]() поліфеноли.
поліфеноли.
69
![]()
