
- •Основні види сировини
- •Зернові культури
- •Будова зерна
- •Хімічний склад зерна
- •Хімічний склад меляси
- •Мікрофлора меляси
- •Коротка характеристика хімічного складу тростинної та рафінадної меляс
- •Нетрадиційні види сировини
- •Топінамбур
- •Цикорій
- •Молочна сироватка
- •Допоміжні матеріали
- •Кислоти
- •Сірчана кислота
- •Соляна кислота
- •Антисептики та миючі засоби Хлорне вапно
- •Формалін
- •Сульфонол
- •Каустична сода
- •Контрольні питання і завдання
- •Розділ 2
- •Приймання зерна
- •Приймання меляси
- •Зберігання сировини
- •Дихання
- •Зміни хімічного складу сировини
- •Випаровування та поглинання вологи
- •Дія від'ємних температур
- •Вплив мікроорганізмів на зберігання сировини
- •Зберігання зерна
- •Зберігання меляси
- •Контрольні питання і завдання
- •Розділ з
- •Підготовка зерна
- •Повітряно-ситове сепарування
- •Магнітне сепарування
- •Відділення насіння бур'янів
- •Підготовка меляси
- •Підкислення і асептування меляси
- •Стерилізація меляси
- •Змішування меляси з водою
- •Кларифікація мелясних розчинів
- •Контрольні питання і завдання
- •Розділ 4
- •Оцукруючі матеріали
- •Характеристика ферментів загальні поняття про ферменти
- •Механізм дії ферментів
- •Концентрація ферменту
- •Температура
- •Активатори та інгібітори ферментів
- •Оксидоредуктази
- •Трансферази
- •Гідролази
- •Ізомерази
- •Активність ферментів
- •Виробництво солоду
- •Замочування зерна
- •Фізико-хімічні процеси під час замочування зерна
- •Біохімічні процеси при замочуванні зерна
- •Способи замочування зерна
- •Пророщування зерна Теоретичні основи пророщування зерна
- •Морфологічні зміни при пророщуванні зерна
- •Біохімічні зміни в зерні при пророщуванні
- •Хімічні зміни зерна при пророщуванні
- •Оптимізація процесів солодорощення
- •Способи солодорощення
- •Пророщування зерна в пневматичній солодовні
- •Токове солодорощення
- •Витрати зерна на солод
- •Виробництво мікробних ферментних препаратів
- •Продуценти ферментів
- •Контрольні питання і завдання
- •Ємкісна (мічурінська) апаратурно-технологічна схема
- •Трубчаста (мироцька) апаратурно-технологша схема
- •Контрольні питання і завдання
- •Розділ 6 спиртові дріжджі
- •Температура і рН
- •Склад живильного середовища Потреба дріжджів у живильних речовинах
- •Види і джерела живлення
- •Інші фактори
- •Аеробний розпад вуглеводів
- •Молочнокислі бактерії
- •Оцтовокислі бактерії
- •Маслянокислі бактерії
- •Гнилісні бактерії
- •Мікрофлора води та повітря
- •Розділ 7
- •Розділ 8
- •Характеристика дріжджів
- •Приготування чистої культури дріжджів
- •Періодичне культивування
- •Культивування дріжджів у виробництві спирту із меляси
- •Розділ 9 зброджування сусла
- •Періодичний спосіб
- •Безперервно-проточний спосіб
- •Циклічний спосіб
- •Технологічні показники бродіння
- •Порівняльна характеристика способів зброджування
- •Теоретичні основи процесів перегонки і ректифікації
- •Одержання спирту-сирцю
- •Непрямої дії
- •Брагоректифікаційна установка побічно-прямотечійної дії
- •Виділення сивушного масла
- •Одержання технічного спирту
- •Одержання абсолютного спирту
- •Умови безпечної експлуатації ректифікаційних установок
- •Розділ 11
- •Вихід спирту
- •Облік і зберігання спирту
- •Розділ 12
- •Сушка дріжджів
- •Термоліз дріжджів
- •Упарювання мелясної барди
- •Склад газів спиртового бродіння
- •Очистка діоксиду вуглецю від домішок
- •Технологія рідкого дІоксиду вуглецю
- •Розділ 13
- •Характеристика стічних вод
- •Механічні способи
- •Хімічні способи
- •Фізико - хімічні способи
- •Біологічні способи
- •14.1. Використання спирту етилового технічного як органічної сировини
- •14.2. Застосування спирту етилового як моторного палива
- •14.3. Виробництво спирту етилового технічного з нехарчової сировини
- •14.4. Виробництво спирту етилового технічного з вуглеводовм1сної сировини
- •14.5. Брагоректифікаційні установки для виробництва сет з вуглеводовмісної сировини
- •14.6. Дегідратація етилового спирту
- •14.8. Перспективні напрями використання спирту етилового технічного в україні
- •Контрольні питання і завдання
- •Розділ 15
- •15.1 Маловідходні та безвідходні технології
- •15.2 Основні напрями створення мало-та безвідходних технологій
- •15.3 Вторинні енергетичні ресурси та їх раціональне використання
- •15.4 Ресурсо- та енергозберігаюча технологія спиртових бражок
- •15.5 Вплив технологічних параметрів на ефективність дії концентрованих ферментних препаратів
- •15.6 Особливості використання концентрованих
- •Ферментних препаратів у залежності
- •Від технологічної схеми водно-теплової
- •Обробки сировини
- •15.7 Особливості приготування виробничих дріжджів та спиртової бражки
- •15.8 Закордонний досвід комплексної переробки зернової сировини в етиловий спирт
- •15.9 Ресурсо- та енергозберігаюча технологія перегонки та ректифікації спирту
- •15.10 Переробка спиртовмісних вторинних продуктів ректифікації в системі бру мелясних заводів
- •15.11 Виділення етилового спирту з головної фракції, збагаченої метиловим спиртом
- •15.12 Централізована переробка головної фракції етилового спирту
- •15.13 Утилізація концентрату головної фракції
- •15.14 Енергозбереження в процесі перегонки та ректифікації спирту
- •15.15 Брагоректифікацшні установки зі ступеневим використанням теплової енергії
- •15.16 Підвищення теплового потенціалу вторинних енергоресурсів
- •15.17 Енергетична характеристика брагоректифікаційних установок
- •Контрольні питання і завдання
- •Розділ 16
- •Та очистки стічних вод у спиртовій промисловості
- •Актуальні проблеми розділення сумішей за допомогою молекулярних фільтрів у спиртовій промисловості
- •Мембранне газорозділення
- •Мембранна технологія води у спиртовому виробництві
- •Мембранна технологія спирту
- •Контрольні питання і завдання
- •Розділ 17 правила охорони праці на спиртових заводах
- •Основні вимоги з техніки безпеки для апаратника ректифікації спирту, а також для приймальника- здавача та зливальника-розливальника спирту
- •Література
Стерилізація меляси
Швидкість
загибелі мікроорганізмів при
летальній температурі описується
кінетичним
рівнянням хімічної реакції першого
порядку: N
= N0
eKt![]()
де N - кількість мікроорганізмів через час t у хв; N0 - початкова кількість мікроорганізмів; е - основа натуральних логарифмів; К - константа швидкості відмирання мікроорганізмів.
Рис. 3.1 Змішувач меляси з кислотою,
антисептиком і живильними
речовинами
Спорові мікроорганізми більш термо-резистентні, ніж вегетативні форми. Молоді клітини гинуть швидше старих.
Через те, що при підвищенні летальної температури різко знижується тривалість її дії на мікроорганізми, то найбільш ефективна
короткочасна стерилізація при температурі до 140° С. Щоб загальмувати швидкість інверсії цукрози і розкладу інвертного цукру, рН мелясного розчину підтримують не нижче 6. Для досягнення більшого ефекту відмирання мікроорганізмів концентрацію меляси знижують до 60...65%.
Теплову обробку меляси за способом Alvo - therm на установці "Alfa - Javal" проводять таким чином.
Меляса із збірника 1 (рис. 3.2) і вода із збірника 2 змішуються у насосі 3 до концентрації сухих речовин 45...50 %, суміш подають у збірник 4 , а з нього насосом 5 у кларифікатор 6. Завдяки надлишковому тиску на виході з кларифікатору освітлений розчин надходить у збірник 7, з якого насосом 8 передається у теплообмінник 9. У ньому розчин нагрівається у дві стадії: у першій - екстрапарою з випа-рувальної камери 11, у другій - гострою парою і при температурі 85. ..90° С насосом 12 подається в стерилізатор 10, де нагрівається гострою парою до температури стерилізації 140° С. Після витримки протягом біля 4 с розчин над-
48
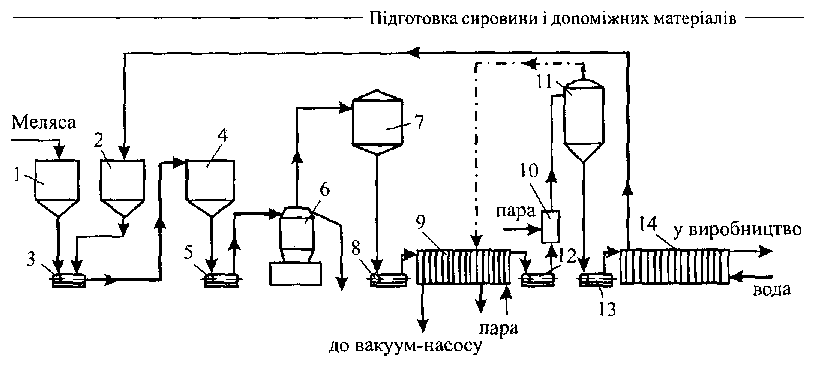
Рис. 3.2 Апаратурно-технологічна схема розведення, кларифікації та стерилізації меляси за способом Albo-therm
ходить у випаровувальну камеру - 11, де створене слабке розрідження. Тут відбувається миттєве охолодження розчину до 85° С, яке супроводжується виділенням вторинної пари, яку направляють у теплообмінник-9. Насосом- 13 розчин подають у пластинчатий теплообмінник - 14 для охолодження водою. Відпрацьовану воду використовують для розведення меляси.
Національним державним університетом харчових технологій (к. КТІХП) рекомендовано проводити стерилізацію інфікованої меляси при концентрації сухих речовин 50 %, температурі 120... 130° С протягом 1 хв в установці, яка складається Із парової контактної головки (стерилізатора), витримувача, випаровувальної камери, конденсатора і вакуум-насоса. Висока ефективність такого способу стерилізації меляси встановлена також співробітниками ВНДІ харчової біотехнології.
Збагачення меляси живильними речовинами для дріжджів
Для кращого харчування дріжджів при бродінні до меляси у змішувачі додають ортофосфорну кислоту, сечовину, інколи дІамонійфосфат. Як антисептики додають розведену сірчану або соляну кислоту, а також інші речовини, які забезпечують біологічну чистоту бродіння.
Витрати 70 %-ної ортофосфорної кислоти Gp (кг на 1000 дал спирту):
де
F
- вміст
у зрілій бражці дріжджів вологістю 75
%, т; Р - вміст Р205
у дріжджах, %
(біля 1%); 0,3 - коефіцієнт, що враховує
30%-ні витрати Р2О5
на обмінні реакції; М-витрати
меляси, т;![]() -
вміст Р2О5
в мелясі, %; 1,97 -коефіцієнт перерахунку
Р205
на 70 %-ну ортофосфорну кислоту, яка
містить 50,7 % Р2О5
(100:50,7).
-
вміст Р2О5
в мелясі, %; 1,97 -коефіцієнт перерахунку
Р205
на 70 %-ну ортофосфорну кислоту, яка
містить 50,7 % Р2О5
(100:50,7).
Формулою можна користуватися для розрахунку витрат будь-якого джерела фосфору, змінивши відповідно значення коефіцієнта 1,97.
49
![]()
Норма витрати 70 %-ної ортофосфорної кислоти на виробництво спирту становить 13 кг на 1000 дал, на виробництво хлібопекарських дріжджів - 5 кг/т. Для підвищення виходу дріжджів рекомендується встановити єдину (загальну) витрату ортофосфорної кислоти - 0,06 % до маси меляси, або 21,5 кг на 1000 дал спирту.
При дефіциті у мелясі засвоюваного азоту вносять сульфат амонію або сечовину. Діамоній фосфат, який містить азот і фосфор, використовують досить рідко. У сечовині азоту міститься у 2,2 рази більше, ніж у сульфаті амонію, відповідно менші і її витрати. При засвоєнні дріжджами азоту сечовини не звільнюється кислотний залишок, внаслідок чого рН зброджуваного сусла не знижується.
Витрати речовин, які містять азот, (кг на 1000 дал спирту):
![]()
де n1 - вміст азоту у дріжджах 75 %-ної вологості, % (звичайно біля 2 %); 0,07 -коефіцієнт, що враховує 7 %-ну втрату азоту на обмінні реакції; N2 - вміст засвоюваного азоту у мелясі, %; К - коефіцієнт перерахунку азоту на джерело азотистого живлення.
Нормальна витрата сульфату амонію 40 кг, сечовини 9-20 кг на 1000 дал спирту. Застосовують їх у вигляді декантованих розчинів з п'яти - шестикратною кількістю води.
Живильні речовини і кислоту змішують з мелясою у змішувачі, аналогічному зображеному на рис. 3.1.
Співробітниками Воронезького об'єднання спиртової промисловості запропонована установка для безперервного підкислювання, асептування меляси і збагачення її живильними солями. Установка складається із чотирьох чи більше циліндричних посудин з конічним дном, які з'єднані переточними трубами. Загальна місткість усіх цистерн розрахована на добовий запас меляси.
Перша посудина розташована на 0,6... 1 м вище наступних і призначена для змішування меляси з розчинами соляної чи сірчаної кислоти, антисептиків і живильних солей. У нижній частині збірника знаходиться повітряний барботер для перемішування, аерування і видалення легких органічних кислот з меляси, Для кращого перемішування і підвищення ступеня використання повітря на внутрішні поверхні циліндричної частини змішувача закріплено п'ять - шість гвинтоподібних направляючих із листової сталі, що має товщину 5...6 мм і ширину 200...250 мм. У другому збірнику - відстоювані - осідають гіпс та інші нерозчинені домішки. На внутрішній поверхні наступних (не менше двох) посудин - витримуваній під кутом 40...45° приварені дві такі ж гвинтоподібні пластини, як і у змішувачі. Вони придають обертальний рух мелясі, що сприяє усуненню застоїв біля стінок. Для розділення меляси на кінцях перетокових труб встановлені розсікані.
Меляса з вагів надходить у змішувач, куди одночасно дозуються кислота та інші допоміжні речовини. Змішуючись з ними, меляса послідовно проходить по перетокових трубах у відстоювач і витримувані, потім подасться у напірний збірник асептованої меляси. Осади виводять із відстоювача при дезінфікації обладнання. Установка дозволяє покращити асептування меляси і впровадити автоматизацію на цій ділянці.
50
![]()
