
Билет№10
Получите водород. Докажите наличие этого газа в пробирке.
***
Оформление:
Получение:
Zn + 2HCl = ZnCl2 + H2↑
Zn + 2H+ = Zn2+ + H2↑
Доказательство наличия: при поднесении горящей спички к водороду слышен характерный хлопок.
Инструкция к работе:
Положите 4-5 гранул цинка в пробирку, налейте туда 2 мл. соляной кислоты HCl, наблюдайте выделение газа водорода в виде пузырьков.
Чтобы доказать, что это именно водород, зажмите пробирку плотно большим пальцем и держите ее до тех пор, пока палец не будет выталкиваться газом, в этот момент поднесите к отверстию пробирки горящую спичку, уберите палец – вы услышите характерный хлопок.
Билет№13
Выделите чистую поваренную соль из смеси ее с песком.
***
Оформление:
Смесь растворяют в воде
Раствор фильтруют : песок остается на фильтре, а раствор соли проходит в стакан.
Чистый раствор соли выпаривают в фарфоровой чашке: вода испаряется, в чашке остается сухая соль.
Инструкция к работе:
1. Растворение загрязненной поваренной соли.
Насыпьте 3 мерных ложечки смеси соли с песком в стакан, налейте 1/3 стакана воды, перемешайте. Песок осядет на дно, а соль растворится.
2. Фильтрование полученной смеси.
С
 оберите
прибор, как показано на рисунке 1:
оберите
прибор, как показано на рисунке 1:
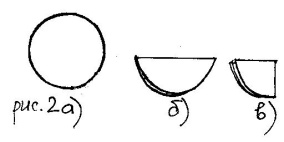
возьмите стакан, поставьте в него воронку, в воронку поместите сложенный вчетверо бумажный фильтр (см.рис.2), повторяющий форму воронки. В фильтр вылейте немного растворенной смеси. Песок останется на фильтре, а раствор соли пройдет сквозь него в стакан.
( Всю смесь фильтровать не надо).
3 . Выпаривание полученного раствора.
Налейте полученный раствор (фильтрат) в фарфоровую чашку (большую каплю). Чашку поместите на кольцо штатива, под которое поставьте спиртовку – см. рис.3.
(Чашку можно закрепить ручным держателем).
Зажгите спиртовку. Нагревайте раствор так, чтобы кончик пламени - самая горячая часть – касался дна чашки. Вода закипает и постепенно испаряется, а на чашке остается сухая соль. После этого можно прекращать нагревание и тушить спиртовку.
Внимание! Горячую фарфоровую чашку руками не трогать!!! Можно получить сильный ожог!
Билет№14
Осуществите превращения: сульфат меди CuSO4 → гидроксид меди Cu(OH)2 → оксид меди CuO
***
Оформление:
CuSO4 + 2NaOH = Cu(OH)2↓+ Na2SO4
голубой р-р синий
Cu2+ + 2OH- = Cu(OH)2↓
t° C
Cu(OH)2↓= CuO+H2O
синий черный
Инструкция к работе:
1) Налейте в 2 пробирки 0,5 мл. сульфата меди CuSO4, затем в каждую – 1 мл. гидроксида натрия NaOH – вы увидите образование синего желеобразного осадка.
2) Затем пробирку нагрейте: для этого закрепите ее держателем на расстоянии 2 см. от края пробирки (передвинув зажим держателя примерно на середину) .
Зажгите спиртовку и поместите пробирку над пламенем спиртовки под наклоном (примерно 35-45°), направляя отверстие пробирки от себя в сторону, где никого нет, предварительно прогрейте пробирку над пламенем по всей длине 2-3 раза. Нагревание продолжайте до изменения цвета (в крайнем случае – до кипения! Иначе кипящий раствор выплеснется из пробирки!!!). В результате реакции синий осадок должен почернеть. Потушите спиртовку.
