
- •§1. Молекулярно-кинетический метод, метод статистической механики и термодинамический метод.
- •§2. Основные положения мкт идеального газа.
- •§3. Параметры состояния. Уравнение состояния. Газовые законы.
- •§4. Идеальный газ и уравнение его состояния.
- •§5. Барометрическая формула. Опыт Перрена. Распределение частиц в силовом поле.
- •§6. Закон Максвелла для распределения молекул идеального газа по скоростям и энергиям теплового движения.
- •§7 Среднее число столкновений и средняя длина свободного пробега молекул.
- •Раздел II. Основы термодинамики.
- •§8 Закон равномерного распределения энергии по степеням свободы.
- •§9 Первое начало термодинамики.
- •§12. Обратимые и необратимые процессы.
- •§13. Энтропия, ее связь с термодинамической вероятностью.
- •§14. Второе начало термодинамики.
- •§15. Третье начало термодинамики - теорема Нернста. Цикл Карно.
- •Раздел III Элементы кинетики
- •§16. Явления переноса.
- •Раздел IV Реальные газы и жидкости
- •§17. Молекулярные силы.
- •§18. Уравнения Ван-дер Ваальса.
- •§19. Жидкое состояние вещества
§14. Второе начало термодинамики.
Обратимы те процессы, при которых степень беспорядочности молекулярных движений во всей системе участвующих тел не увеличивается и энтропия системы остается постоянной. Необратимые же процессы идут сами собой в направлении, при котором степень заотичности молекулярных движений увеличивается и энтропия всей системы возрастает.
2-е начало тер-ки: При всех процессах, происходящих в макроскопической системе, система не может самопроизвольно переходить из более вероятного состояния в менее вероятное. Конечное состояние всегда имеет туже или большуу вероятность и энтропию. Краткая математическая запись:
![]() (14.1).
(14.1).
Клаузиус: теплота никогда не может переходить сама собой от тел с более низкой температурой к телам с более высокой температурой.
Томсон и Планк: В природе не возможен процесс, полный эффект которого состоял бы только в охлаждении теплового резервуара и в эквивалентном подъеме груза (т.е. эквивалентной механической работе).
Эти формулировки эквивалентны.
Вечный двигатель 2-го рода – машина, работающая за счет ВЭ одного теплового резервуара. Тогда 2-е начало: Перпетуум мобиле второго рода невозможно.
2-е начало термодинамики имеет границы применимости:
1) Поэтому неравенство (14.1), строго говоря, следует формулировать так: наиболее вероятным изменением энтропии системы является ее возрастание.
2-еНТ как и все выводы статистической физики справедливы с точностью до флуктуаций. Флуктуации плотности и давления – это процессы, при которых энтропия может убывать.
С точки зрения МКТ увеличение энтропии есть лишь наиболее вероятный, но отнють не обязательный путь развития системы. Уменьшение энтропии не невозможно, а маловероятно.
2) Конечное состояние почти изолированной системы зависит от состояния резервуара, в котором она находится, к-е будет определять все статистические закономерности системы.
3) Бессмысленно применять законы статистической физики к незамкнутой системе, такой как Вселенная в целом – системе безграничной и развивающейся.
§15. Третье начало термодинамики - теорема Нернста. Цикл Карно.
Система, находящаяся
в равновесии при абсолютном нуле, не
может больше отдавать энергию окружающим
телам, и ее ВЭ распределена между
составляющими ее частицами одним-единственным
определенным способом. Благодаря полной
упорядоченности этого единственного
состояния его термодинамическая
вероятность W=1, тогда
![]() .
.
Первые два начала
термодинамики дополняются третьим –
теоремой Нернста-Планка: энтропия всех
тел в состоянии равновесия стремится
к нулю по мере приближения температуры
к нулю Кельвина:
![]() .
.
Т.к. энтропия определяется с точностью до постоянной, то эту постоянную удобно взять равной 0. Из теоремы Нернста-Планка следует, что теплоемкости Ср и СV тоже при Т=0 равны нулю.
Идея вечного двигателя ( с КПД=1) означает, что все полученное тепло от нагревателя должно переводиться в работу. Французский физик и инженер Н.Л.С. Карно (1796-1832) показал, что для работы теплового двигателя необходимо не менее двух источников теплоты с различными температурами, иначе это бы противоречило 2-му началу термодинамики.
Принцип действия теплового двигателя и холодильной машины:
В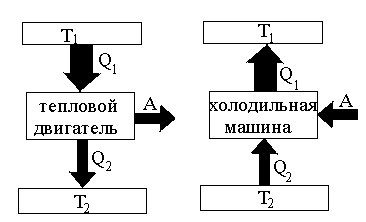 ывод:
без совершения работы нельзя отбирать
тепло от менее нагретого тела и отдавать
ее более нагретому. Это утверждение
есть не что иное как 2-е начало тер-ки в
формулировке Клаузиуса.
ывод:
без совершения работы нельзя отбирать
тепло от менее нагретого тела и отдавать
ее более нагретому. Это утверждение
есть не что иное как 2-е начало тер-ки в
формулировке Клаузиуса.
Но оно не запрещает переход теплоты от менее нагретого тела к более нагретому (ведь такой переход имеет место в холодильной машине), но при этом надо помнить, что этот переход не является единственным результатом процесса.
Т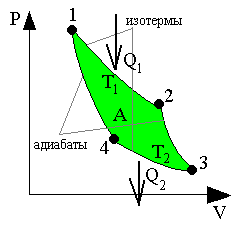 еорема
Карно: из всех периодически действующих
тепловых машин, имеющих одинаковые
температуры нагревателей (Т1) и
холодильников (Т2), наибольшим
КПД обладают обратимые машины; при этом
КПД обратимых машин не
зависят от природы рабочего тела
(тела, совершающего круговой процесс и
обменивающегося энергией с другими
телами) и равны при одинаковых Т1
и Т2.
еорема
Карно: из всех периодически действующих
тепловых машин, имеющих одинаковые
температуры нагревателей (Т1) и
холодильников (Т2), наибольшим
КПД обладают обратимые машины; при этом
КПД обратимых машин не
зависят от природы рабочего тела
(тела, совершающего круговой процесс и
обменивающегося энергией с другими
телами) и равны при одинаковых Т1
и Т2.
Цикл Карно - наиболее экономичный цикл – состоит из 2 изотерм и 2 адиабат (рис). Рабочее тело – идеальный газ под поршнем в сосуде.
![]() - работа изотермического
расширения;
- работа изотермического
расширения;
![]() - работа адиабатического расширения за
счет ВЭ;
- работа адиабатического расширения за
счет ВЭ;
![]() - работа изотермического сжатия;
- работа изотермического сжатия;
![]() .
Суммарная работа: A=Q1-Q2.
.
Суммарная работа: A=Q1-Q2.
Термический
КПД цикла Карно с учетом уравнений
адиабат (Пуассона):
![]() ,
,
![]() откуда
откуда
![]() .
Подставим:
.
Подставим:
 ,
т.е.
,
т.е.
для цикла Карно КПД определяется значениями температур нагревателя и холодильника. Для его повышения необходимо увеличивать разность температур. Для всякого реального теплового двигателя из-за трения и неизбежных тепловых потерь КПД гораздо меньше вычисленного для цикла Карно.
Обратный цикл Карно лежит в основе тепловых насосов.
Теорема Карно
послужила основанием к созданию
термодинамической шкалы температур:
![]() ,
т.е. для сравнения температур необходимо
осуществить обратимый цикл Карно, в
котором одно тело используется в качестве
нагревателя, другое – холодильника.
Причем из теоремы Карно следует, что на
результаты сравнения температур не
окажет влияние химический состав тел.
,
т.е. для сравнения температур необходимо
осуществить обратимый цикл Карно, в
котором одно тело используется в качестве
нагревателя, другое – холодильника.
Причем из теоремы Карно следует, что на
результаты сравнения температур не
окажет влияние химический состав тел.
