
- •Органічна хімія (частина перша)
- •Органічна хімія
- •§1. Поняття про органічні сполуки. Спільні та відмінні ознаки неорганічних та органічних речовин Коротка історія виникнення органічної хімії
- •Спільні ознаки неорганічних та органічних речовин
- •Відмінні ознаки неорганічних та органічних речовин
- •Класифікація органічних речовин
- •Завдання для самоконтролю
- •Насичені вуглеводні Поняття та класифікація вуглеводнів
- •§2. Метан Склад і будова молекули
- •Фізичні властивості та поширення в природі
- •Хімічні властивості
- •Застосування
- •Завдання для самоконтролю
- •§3. Гомологи метану Гомологічний ряд
- •Структурні формули
- •Фізичні властивості
- •Хімічні властивості
- •Одержання насичених вуглеводнів
- •Завдання для самоконтролю
- •§4. Ізомерія насичених вуглеводнів Радикали та їх назви
- •Явище ізомерії, ізомери
- •Завдання для самоконтролю
- •§5. Теорія хімічної будови органічних речовин Виникнення теорії хімічної будови органічних речовин
- •Основні положення теорії хімічної будови органічних речовин
- •Значення теорії хімічної будови органічних речовин
- •Завдання для самоконтролю
- •§6. Визначення молекулярної формули газуватої речовини
- •Завдання для самоконтролю
- •Ненасичені вуглеводні
- •Н енасичені вуглеводні
- •§7. Етиленові вуглеводні Поняття етиленові вуглеводні. Гомологічний ряд
- •Електронна будова етилену
- •Фізичні властивості етилену
- •Хімічні властивості етилену
- •Одержання етилену
- •Застосування етилену
- •Завдання для самоконтролю
- •§ 8. Ацетиленові вуглеводні Поняття ацетиленові вуглеводні. Гомологічний ряд
- •Електронна будова ацетилену
- •Фізичні властивості ацетилену
- •Хімічні властивості ацетилену
- •Одержання ацетилену
- •Застосування ацетилену
- •Завдання для самоконтролю
- •§ 9. Дієнові вуглеводні Поняття та класифікація дієнових вуглеводнів
- •Хімічні властивості
- •Застосування
- •Завдання для самоконтролю
- •§ 10. Ізомерія ненасичених вуглеводнів
- •Завдання для самоконтролю
- •§ 11. Поняття про полімери. Поліетилен
- •С клад і будова поліетилену
- •Властивості поліетилену
- •Застосування поліетилену.
- •Завдання для самоконтролю
- •§ 12. Пластмаси
- •Завдання для самоконтролю
- •§ 13. Розв’язування розрахункових задач на виведення формули речовини за продуктами спалювання
- •Завдання для самоконтролю
- •Циклічні та ароматичні вуглеводні
- •§ 14. Циклічні сполуки
- •Гомологічний ряд та номенклатура циклічних сполук
- •Завдання для самоконтролю
- •§ 15. Бензен
- •Завдання для самоконтролю
- •§16. Поняття про хімічні засоби захисту рослин
- •Завдання для самоконтролю
- •§17. Взаємозв’язок насичених, ненасичених і ароматичних вуглеводнів
- •2 Наси чені 5
- •Завдання для самоконтролю
- •Природні джерела вуглеводнів
- •§18. Природний та супутній нафтовий гази Природний газ
- •Супутній нафтовий газ
- •Завдання для самоконтролю
- •§19. Нафта Походження нафти
- •Фізичні властивості нафти
- •Склад нафти
- •Переробка нафти
- •Крекінг нафтопродуктів
- •Детонаційна стійкість бензинів
- •Застосування нафтопродуктів
- •Завдання для самоконтролю
- •§20. Вугілля та продукти його переробки
- •Завдання для самоконтролю
Завдання для самоконтролю
84. Визначити формулу вуглеводню, при спалюванні 4,4 г якого одержали 13,2 г карбон(ІV) оксид і 7,2 г води. Відносна густина його парів за воднем дорівнює 22.
85. Спалили 7,2 г органічної речовини, густина якої за воднем дорівнює 36. У результаті було одержано 22 г карбон(ІV) оксид і 10,8 г води. Визначте молекулярну формулу цієї речовини.
86. При спалюванні 1,84 г органічної речовини утворюється 3,36 л (н.у.) карбон(ІV) оксиду і 1,44 г води. Молярна маса речовини 92 г/моль. Визначити молекулярну формулу сполуки.
87. У результаті спалювання 112 мл газу утворилося 448 мл карбон(ІV) оксиду і 0,45 г води. Густина речовини за воднем – 29. Визначити молекулярну формулу газу.
Циклічні та ароматичні вуглеводні
§ 14. Циклічні сполуки
Циклічні сполуки – це сполуки, які мають замкнутий ланцюг.
Циклічні сполуки ще називають циклопарафінами.
Гомологічний ряд та номенклатура циклічних сполук
 СН2
Н2С
СН2
Н2С СН2
СН2
 СН2
СН2
Н2С СН2
Н2С СН2 Н2С СН2 Н2С СН2
циклопропан циклобутан циклопентан
 Н
Н 2С
СН2
Н2С
СН2
2С
СН2
Н2С
СН2 Н2С
СН2
Н2С
СН2
Н2С СН2 Н2С СН2 Н2С СН2
Н2С СН2 Н2С СН2 Н2С СН2
циклогексан СН2 Н2С СН2
циклогептан циклооктан
Назва циклічних сполук походить від назв насичених вуглеводнів із додаванням префікса цикло-.
Знаходження в природі
Циклічні сполуки головним чином знаходяться в складі деяких нафт. Звідси й інша назва циклічних сполук – нафтени.
Фізичні властивості
Циклопропан і циклобутан за звичайних умов – гази, а циклопентан і циклогексан – рідини. Циклічні сполуки у воді практично не розчиняються.
Хімічні властивості
Приєднання водню (гідрування):
СН2
t, kt
+ Н2 → CН3-СН2-СН3
Н2С СН2 пропан
циклопропан
2. Заміщення (хлорування):
 Н
Н
 Н
H
Cl
Н
H
Cl
 С
C
С
C
Н2С
СН2
t, kt, hυ
+
Сl
Н2С СН2 Н2С СН2
СН2 СН2
циклогексан хлорциклогексан
3. Дегідрування (відщеплення водню):
СН2 CН
Н2С
СН2
t, kt
 СН
СН
 +
3Н2
+
3Н2
Н2С
СН2
НС
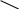 СН
СН
СН2 СН
циклогексан бензен
Одержання
1. Дегідрування (відщеплення водню) насичених вуглеводнів:
t, kt
CН3-СН2-СН3 → + Н2
пропан Н2С СН2
циклопропан
2. Взаємодія металічного натрію з дигалогенпохідних насичених вуглеводнів:
СН2-СН2-С
+ 2Na
→
+ 2NaCl
СН2-СН2-Сl Н2С-СН2
дихлорбутан циклобутан
Застосування
Із циклічних сполук практичне значення мають циклогексан, метилциклогексан та деякі інші. В процесі ароматизації нафти ці сполуки перетворюються в ароматичні вуглеводні – в бензен, толуен та інші речовини, які широко використовуються для синтезу барвників, медикаментів тощо. Циклопропан використовують для наркозу.
