- •Лекция 4 (II часть). Углеводороды. Электронное строение, реакционные центры.
- •Типы реакций.
- •Механизм электрофильных реакций алкенов и аренов.
- •1. Генерирование электрофильной частицы. Алкены.
- •4. Стабилизация карбкатиона.
- •Особенности протекания некоторых реакций.
- •Факторы, обуславливающие региоселективность.
- •2. Региоселективность реакций присоединения к несимметричным алкенам и алкинам реагентов типа н-х.
- •Современная электронная интерпретация правила Марковникова.
- •Примеры реакций присоединения, идущих:
- •4. Стереоспецифичность реакции гидроксилирования алкенов (реакция Вагнера).
- •5. Химические особенности сопряженных диенов:
- •6. Влияние заместителей на реакционную способность и ориентацию в реакциях электрофильного замещения в бензольном кольце. Классификация заместителей.
- •Типы реакций se аренов.
- •Механизм ориентирующего влияния заместителей.
- •Резонансные структуры карбкатиона (3).
- •Согласованная и несогласованная ориентация электрофильного замещения у дизамещенных бензола.
- •Примеры.
- •Реакции идентификации углеводородов.
4. Стереоспецифичность реакции гидроксилирования алкенов (реакция Вагнера).
Химизм.

Механизм.

Внешний эффект реакции.
Исчезновение малиновой окраски перманганата калия.
Образование бурого осадка оксида марганца (IV).
5. Химические особенности сопряженных диенов:
- повышенная термодинамическая устойчивость, ER ~ 15 кДж/моль;
- повышенная реакционная способность в реакциях присоединения и полимеризации (в сравнении с алкенами);
- вступают в реакции AE с образованием не только 1,2-аддукта, но и 1,4-аддукта.

6. Влияние заместителей на реакционную способность и ориентацию в реакциях электрофильного замещения в бензольном кольце. Классификация заместителей.
Таблица 4
Группы заместителей |
Заместители |
Тип эффекта |
Влияние на реакционную способность |
I. Активирующие и о-, n- ориентирующие (ЭД). |
- NH2, -NHR, -NR2, -OH -O-, -NHCOCH3, -OCH3, -CH3 и другие алкилы -C6H5, -CH = CH2 |
+ M >> -I + M, + I + M > - I + I + M > - I |
+++ +++ ++ + + |
II. Дезактивирующие и о-, n- ориентирующие (ЭА). |
-F, -Cl, -Br, -I |
- I > + M |
- |
III. Дезактивирующие и м-ориентирующие. |
-C N, -CHO, -COR, -COOH -COOR, -SO3H, -N+R3, -CF3, -CCl3, -NO2, -N+2. |
- I, - M - I, - M - I - I, - M |
- - - - - - - - - - |
Примечание: (+) – увеличение реакционной способности.
(-) – уменьшение реакционной способности.
Типы реакций se аренов.
Таблица 5
|
Галогенирование |
Нитрование |
Сульфирование |
Алкилирование |
Ацилирование |
Азосочетание |
Нитрозирование |
Карбоксилирование |
|
++ |
++ |
++ |
++ |
++ |
- |
- |
- |
|
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
|
+ |
+ |
+ |
+ |
+ |
- |
- |
- |
- могут вступать в реакции с нуклеофильными реагентами.
Механизм ориентирующего влияния заместителей.
Влияние заместителей на реакционную способность и ориентацию в реакциях SE можно интерпретировать с позиций:
- статических факторов (распределение электронной плотности в бензольном кольце под влиянием заместителя и стерические возможности атаки электрофила);
- кинетических факторов (стабильность интермедиата – карбкатиона).
Стабильность карбкатиона определяется степенью делокализации его положительного заряда.
Делокализацию заряда можно изобразить:
- методом мезомерии;
- методом резонанса, т.е. с помощью набора предельных (резонансных структур).

Резонансные структуры карбкатиона (3).
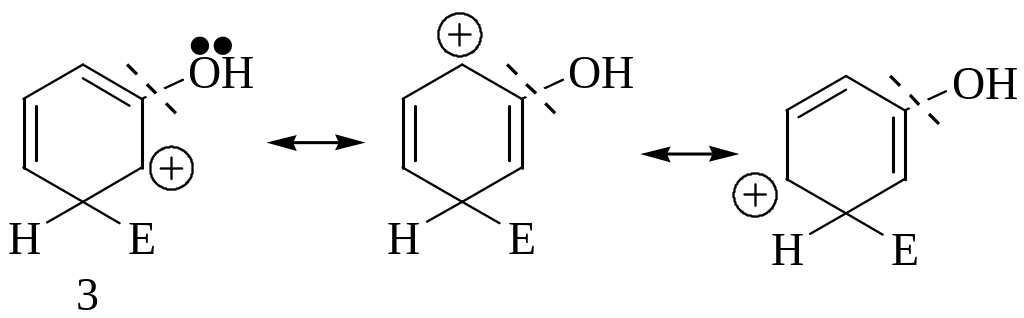
Карбкатион (3) менее стабилен, чем (1), т.к. в его стабилизации не участвует заместитель.