
- •Лекция 2 пространственное строение органических молекул. Стереоизомерия.
- •Виды изомерии.
- •Способы установления хиральности молекулы.
- •2. Использование элементов симметрии.
- •3. Наличие хиральных центров.
- •Способы изображения конфигурации.
- •Стереохимические формулы в клиновидной записи.
- •2. Проекционные формулы Фишера l-молочной кислоты.
- •Способы преобразования проекционных формул.
- •Стереохимические ряды.
- •Диастереомерия.
- •Трео- и эритро- изомеры.
- •Свойства стереоизомеров.
- •Энантиомеры, рацематы, диастереомеры, мезо-формы (свойства).
- •Сравнение свойств винных кислот.
- •Необходимые условия проявления оптической активности.
- •Конформации ациклических соединений.
- •Потенциальная энергия конформации н-бутана.
- •Стабилизация аксиального конформера за счет водородной связи.
- •Конформационный анализ дизамещенных циклогексанов.
Лекция 2 пространственное строение органических молекул. Стереоизомерия.

Структура молекулы – определенная последовательность соединения атомов в молекуле и характер их связей.
Конфигурация молекулы – фиксированное расположение в пространстве заместителей вокруг стерических центров.
Конформации молекулы – различные пространственные формы молекулы, возникающие при изменении относительной ориентации отдельных ее частей в результате внутреннего вращения атомов вокруг простых связей.
Виды изомерии.
Энантиомерия – вид стереоизомерии, характеризующейся наличием энантиомеров, т.е. изомеров, относящихся друг к другу как предмет и несовместимое с ним зеркальное изображение.
Хиральность (гр. cheir – рука) – несовместимость молекулы со своим зеркальным изображением.
Способы установления хиральности молекулы.
1. Построение модели молекулы (1) и модели ее зеркального изображения (2). Молекула хиральна, если модели не полностью совмещаются.
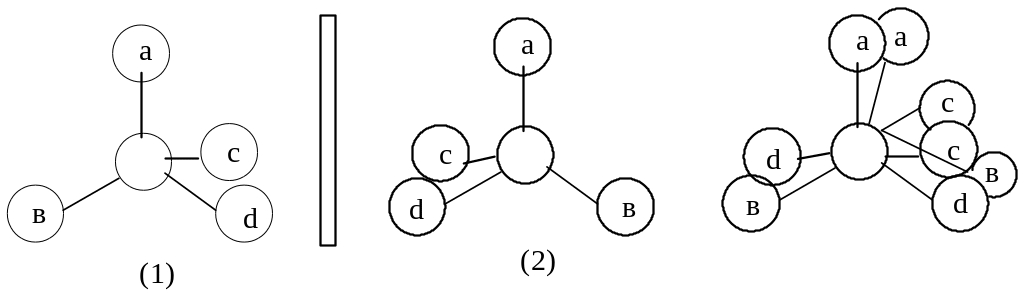
Молекула хиральна
2. Использование элементов симметрии.
Молекула хиральна, если отсутствуют плоскость и центр симметрии. Ось симметрии может быть.
Плоскость симметрии – это воображаемая плоскость, которая рассекает объект на две зеркально противоположные половины.
Центр симметрии – это точка, относительно которой на прямой, проходящей через нее, можно встретить тождественные точки на одном и том же расстоянии.
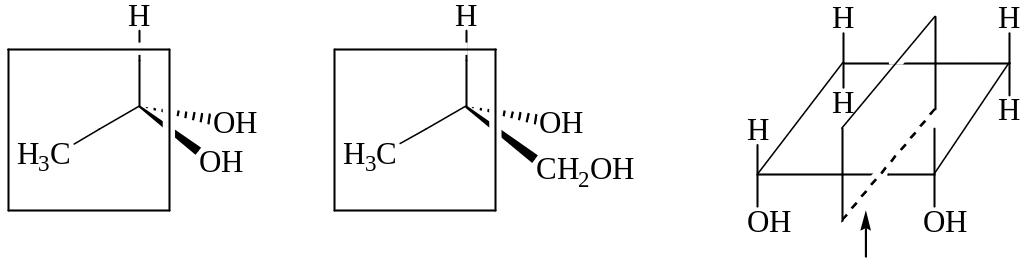
Молекула ахиральна Молекула хиральна Плоскость симметрии – молекула ахиральна
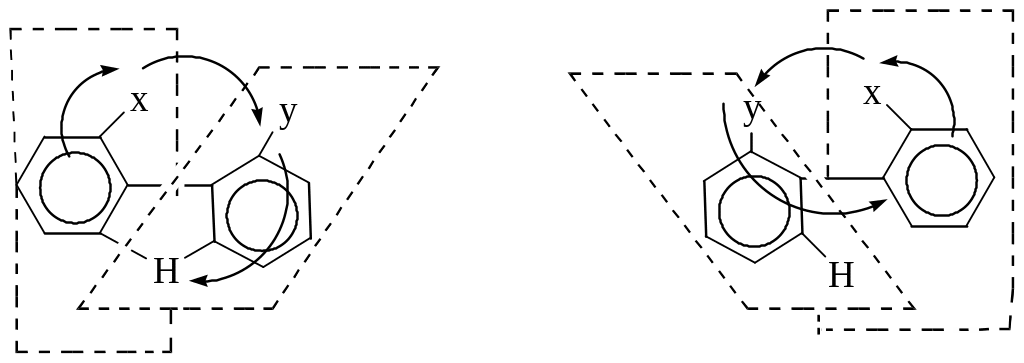
Схемы зеркальных изомеров производных дифенила
3. Наличие хиральных центров.
Хиральный центр – sp3-гибридизованный атом (C, N, Si, P) с четырьмя разными лигандами.
Асимметрический атом углерода – хиральный атом, т.е. sp3-гибридизованный с четырьмя разными партнерами. В структурной формуле обозначается С*.
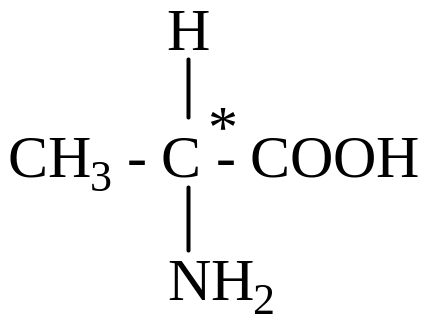 2-аминопропановая кислота
2-аминопропановая кислота
Способы изображения конфигурации.
Стереохимические формулы в клиновидной записи.
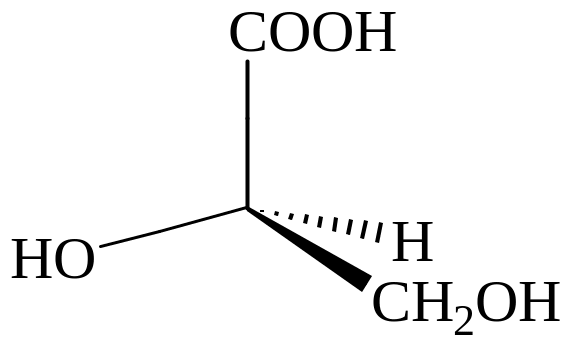
2. Проекционные формулы Фишера l-молочной кислоты.

Способы преобразования проекционных формул.
Формулы можно вращать в плоскости чертежа на 180о.
Произвести четное число перестановок заместителей у хирального центра.
Вращение трех заместителей по часовой или против часовой стрелки, не затрагивая четвертый.
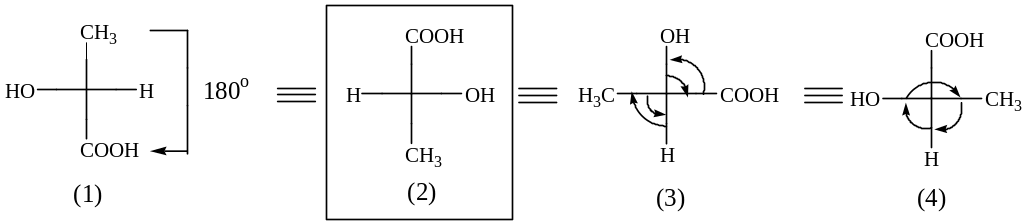
Проекция (2) – стандартная проекция Фишера: у нее атомы углерода на вертикальной линии со старшей функцией наверху, неуглеродные заместители – на горизонтальной линии. В точках пересечения С*; символ атома углерода не пишется. В стандартной проекции выделяется стереохимический колюч – хиральный атом с не углеводородными заместителями (берется в рамку), который определяет принадлежность изомера к D- или L-стереохимическому ряду. Стереохимический ключ у моносахаридов - асимметрический атом углевода, наиболее удаленный от карбонильной группы. У α-гидрокси- и α-аминокислот стереохимический ключ – асимметрический атом углерода в α-положении.
