
- •Оглавление
- •Предисловие
- •Введение
- •Раздел I. Химия почв
- •1. Химический состав почв
- •1.1. Элементный состав почв
- •1.2. Фазовый состав почвы
- •1.3. Соединения щелочных и щелочно-земельных элементов в почвах
- •1.4. Формы соединений химических элементов в почвах и их доступность растениям
- •Контрольные вопросы
- •2. Почвенные растворы
- •2.1. Концентрации и активности ионов и солей в почвенных растворах
- •2.2. Методы определения активности ионов
- •Контрольные вопросы
- •3. Катионообменная способность почв
- •3.1. Селективность катионного обмена
- •3.2. Кинетика обмена катионов
- •3.3. Уравнения и изотермы катионного обмена
- •3.4. Катионный обмен и адсорбция
- •3.5. Обменные катионы в почвах
- •Контрольные вопросы
- •4. Окислительно-восстановительные реакции и процессы в почвах
- •4.1. Окислительно-восстановительный потенциал почвы
- •4.2. Потенциалопределяющие системы в почвах
- •4.3. Окислительное состояние основных типов почв
- •4.4. Типы окислительно-восстановительных режимов
- •4.5. Влияние окислительно-восстановительных процессов на химическое состояние почв
- •4.6. Методы определения окислительных потенциалов и изучения окислительно-восстановительных режимов
- •Контрольные вопросы
- •Раздел II. Физика почв
- •1. Подготовка почвы к определению показателей физических свойств
- •1.1. Заложение и описание почвенного разреза
- •1.2. Морфологическое описание почвенного разреза
- •Пример морфологического описания почвы Разрез № 217
- •Контрольные вопросы
- •2. Определение гранулометрического состава почвы
- •Классификация почв и пород по гранулометрическому составу
- •2.1. Методы определения гранулометрического состава
- •2.1.1 Определение гранулометрического состава визуально и на ощупь
- •Визуальные методы определения гранулометрического
- •2.1.2 Лабораторные методы определения гранулометрического состава
- •Подготовка почвы к гранулометрическому анализу
- •Форма записи при определении гигроскопической влажности почвы
- •Определение гранулометрического состава в стоячей воде. Метод пипетки
- •Плотность и вязкость воды в зависимости от температуры
- •Интервалы во времени при взятии проб суспензии в зависимости от температуры суспензии и плотности частиц
- •Расчёт результатов анализа
- •Пример вычисления:
- •Пример записи данных гранулометрического анализа
- •Контрольные вопросы
- •3. Методы изучения структуры почвы
- •3.1. Морфологическое изучение почвенной структуры
- •3.2. Лабораторные методы изучения структуры почвы
- •3.2.1. Агрегатный анализ почвы (метод сухого рассева)
- •Форма записи результатов агрегатного анализа
- •3.2.2. Определение водопрочности структурных агрегатов по п.И. Андрианову
- •3.2.3. Микроагрегатный анализ
- •Форма записи результатов микроагрегатного анализа
- •3.2.4. Определение порозности агрегатов
- •Форма записи при определении порозности агрегата
- •Контрольные вопросы
- •4. Методы определения показателей общих физических свойств почвы
- •4.1. Определение плотности твёрдой фазы почвы
- •Состав и плотность некоторых минералов
- •Форма записи определения твёрдой фазы почвы
- •4.2. Определение плотности почвы
- •Форма записи определения плотности почвы
- •4.3. Определение пористости (порозности, скважности) почвы
- •4.4 Определение дифференциальной порозности методом расчёта
- •Форма записи определения дифференциальной порозности
- •4.5 Оценка показателей общих физических свойств почвы
- •Характеристика уплотненности почвы по величине плотности сложения (dV, г/см3) и порозности (p, % от объёма почвы)
- •Контрольные вопросы
- •5. Методы изучения водных свойств почвы
- •5.1 Определение влажности почвы
- •5.2 Определение водопроницаемости почвы
- •Оценка водопроницаемости почв тяжёлого гранулометрического состава
- •Форма записи результатов определения водопроницаемости почвы
- •5.3 Определение гидрологических характеристик почвы
- •Максимальная гигроскопичность почв, различных по гранулометрическому составу и средней гумусированности
- •5.4 Определение влагоёмкости почвы
- •Форма записи результатов определения капиллярной влагоёмкости
- •Оценка предельной полевой (наименьшей) влагоёмкости
- •5.5 Расчёты запасов влаги при определении наиболее важных гидрологических характеристик почвы
- •Контрольные вопросы
- •Раздел III. Статистическая обработка данных при изучении свойств почв
- •1. Статистические показатели вариационных рядов
- •Пример расчёта статистических показателей
- •Результаты статистической обработки данных определения плотности лугово-чернозёмной почвы в слое 0 – 20 см
- •2. Оценка существенности разницы выборочных средних
- •Примеры расчётов
- •Влияние использования лугово-чернозёмной почвы на водопрочность структуры
- •3. Корреляция и регрессия
- •Пример расчёта
- •Влажность устойчивого завядания растений при различной плотности пахотного слоя чернозёма обыкновенного
- •Расчет корреляционной зависимости между влажностью устойчивого
- •Слоя чернозёма обыкновенного
- •Заключение
- •Библиографический список
Контрольные вопросы
1. Дать определение элементного состава почв, его характеристику и значение.
2. Что понимают под фазовым составом почв. Значение фазового состава почв.
3. Какие единицы измерения используют для выражения результатов определения элементного состава почвы?
4. Дайте определение понятиям макроэлементы и микроэлементы. Какие элементы относят к макро- и микроэлементам?
5. Что положено в основу деления элементов на водные и воздушные мигранты?
7. Какие биогеохимические зоны выделяют?
8. Дайте краткую характеристику и укажите значение в почвообразовании следующих элементов: алюминий, бор, железо, кальций, углерод, натрий, магний, сера, фосфор, кремний, азот, кислород.
9. Дать краткую характеристику элементам группы бора, литию, цезию, рубидию, свинцу, цинку, мышьяку, сурьме, висмуту, ванадию.
2. Почвенные растворы
Состав почвенных растворов обусловлен преимущественно легкорастворимыми соединениями, в числе которых большую роль играют соли, содержащие катионы металлов I и II групп. Почвенный раствор – это жидкая фаза почвы в природных условиях.
В почвенном растворе осуществляются важнейшие почвенно-химические реакции; растения и микроорганизмы получают необходимые им вещества главным образом из почвенного раствора.
Немало методических трудностей возникает при выделении почвенного раствора. Предложено несколько принципиально различных способов:
1) вытеснение почвенного раствора водой или другими жидкостями;
2) отделение при центрифугировании;
3) отжимание почвенных растворов в специальных пресс-формах при высоком давлении;
4) имитация почвенных растворов путем получения водных вытяжек;
5) получение растворов с помощью лизиметров.
Несовершенства и принципиальные трудности методов выделения почвенных растворов заставили исследователей искать иные пути познания этой важнейшей фазы почв. Были разработаны два новых подхода:
1) измерение свойств почвенных растворов непосредственно в живой почве in suti с помощью ионоселективных электродов;
2) эмпирический подбор таких растворов, состав которых не изменяется после взаимодействия с почвой.
При достаточно надежной технике измерения состав таких растворов можно с высокой степенью достоверности приравнять к составу нативных почвенных растворов. Состав почвенных растворов меняется в очень широких пределах. В незаселенных почвах концентрация почвенного раствора находится в диапазоне от десятых долей до нескольких целых граммов в литре, или примерно от 5–7 до 100–150 мг-экв/л катионов и анионов. В почвенном растворе присутствуют Са2+, Mg2+, К+, NH4+, Na+, HCO3-, SO42-, NО3-, Сl-. При изменении влажности почвы концентрация отдельных ионов изменяется по различным законам. Так, концентрация ионов Na+, NО3-, Сl- нарастает пропорционально уменьшению влажности почвы, а концентрация фосфат-иона, обусловленная произведением растворимости фосфатов кальция, остается значительно более стабильной. Для характеристик свойств почвенных растворов недостаточно знать только концентрации составляющих их веществ. Свойства растворов зависят от того, в каких формах находятся в них различные ионы и вещества.
В состав почвенных растворов входят незаряженные (нейтральные) молекулы, ионы и ионные пары, тройники и другие ассоциаты ионов. Ионные пары возникают за счет электростатического взаимодействия зарядов ионов и сольватации. Образование ионных пар характеризует неполную диссоциацию сильного электролита. Например, в растворе могут возникать незаряженные молекулы СаСОз:
Са2+ + СО32- = CaCO30
Ионные пары могут нести заряд:
Na+ + SО42- = NaSO4-
Константа диссоциации ионной пары записывается так же, как константа для слабого электролита (квадратные скобки означают активности ионов):
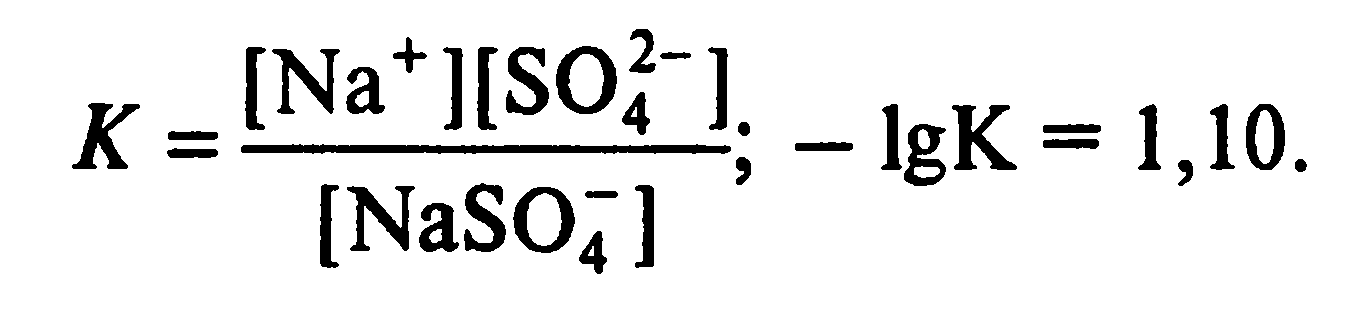
Отличие от слабых электролитов заключается в том, что взаимодействие в ионных парах вызвано кулоновскими силами, тогда как ограниченная диссоциация слабых электролитов обусловлена наличием ковалентной связи. Таким образом, полный анализ почвенных растворов основан на определении активности ионов и солей и учета всех образующихся в растворе ассоциатов.
