
- •Методы анализа биологичеcки активных веществ и их свойства.
- •Химические свойства
- •Группы сырья по бав
- •1. Полисахариды
- •Количественное определение
- •2. Оценка качества сырья, содержащего жиры. Методы анализа.
- •3. Эфирные масла
- •4. Качественные реакции на антраценпроизводные
- •Реакция образования фенолятов со щелочью:
- •2. Реакция микросублимации (микровозгонки).
- •3.Реакция образования лаков.
- •1. Фотоэлектроколориметрический метод.
- •2. Спектрофотометрический метод.
- •5. Качественный анализ дубильных веществ.
- •3. Физико-химические методы.
- •6. Методы анализа сырья, содержащего сапонины.
- •Реакции, основанные на физических свойствах.
- •7. Анализ сырья, содержащего сг.
- •1. Реакции на стероидную структуру.
- •2. Реакции на ненасыщенное лактонное кольцо.
- •3. Реакции на углеводную часть молекулы.
- •8. Методы анализа сырья, содержащего простые фенольные соединения.
- •Простые фенолы и агликоны фенологликозидов дают
- •Специфические реакции (гф х1):
- •Хроматографическое исследование
- •9. Качественное определение.
- •3. Реакция с треххлористой сурьмой.
- •Реакция с 1 %-ным раствором основного ацетата свинца.
- •3. Спектрофотометрический метод (сфм)
- •Хроматоспектрофотометрический метод.
- •Предварительное разделение на колонке с полиамидом (плоды боярышника)
- •3. В траве сушеницы топяной выделяют следующие стадии количественного определения:
- •4. Количественное содержание ксантонов в траве золототысячника:
- •10. Методы анализа кумаринов
- •Качественный анализ
- •1 Группа. Йод и его растворы.
- •2 Группа. Комплексные йодиды металлов:
- •1. Извлечение суммы алкалоидов из сырья.
- •2. Очистка извлечения от балластных веществ.
- •3. Разделение суммы алкалоидов и выделение индивидуальных алкалоидов.
- •Гравиметрический (весовой) метод.
- •2) Титриметрические методы:
- •3) Физико-химические (инструментальные) методы:
- •12. Анализ сырья, содержащего сг.
- •1. Реакции на стероидную структуру.
- •2. Реакции на ненасыщенное лактонное кольцо.
- •3. Реакции на углеводную часть молекулы.
- •13. Оценка качества сырья, содержащего витамины.
9. Качественное определение.
Специфических реакций для всех групп флавоноидов не существует.
Часто используют следующие качественные реакции и хроматографическое исследование:
1. Характерной реакцией на флавоноиды - Цианидиновая проба или
проба Синода (проба Chinoda)(основана на восстановление их атомарным водородом в кислой среде в присутствии магния или цинка).
Флавоноиды при восстановлении магнием или цинком в присутствии концентрированной хлористоводородной кислоты образуют красное окрашивание, обусловливаемое образованием антоцианидинов:
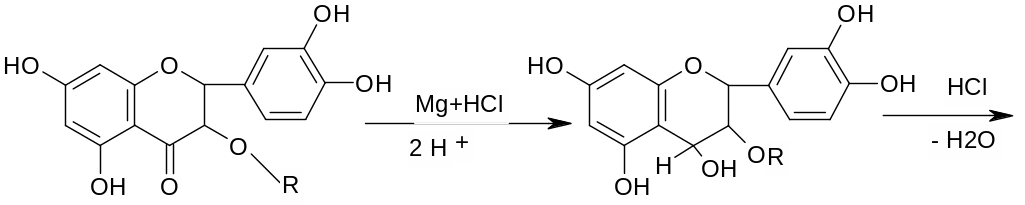
хроменол
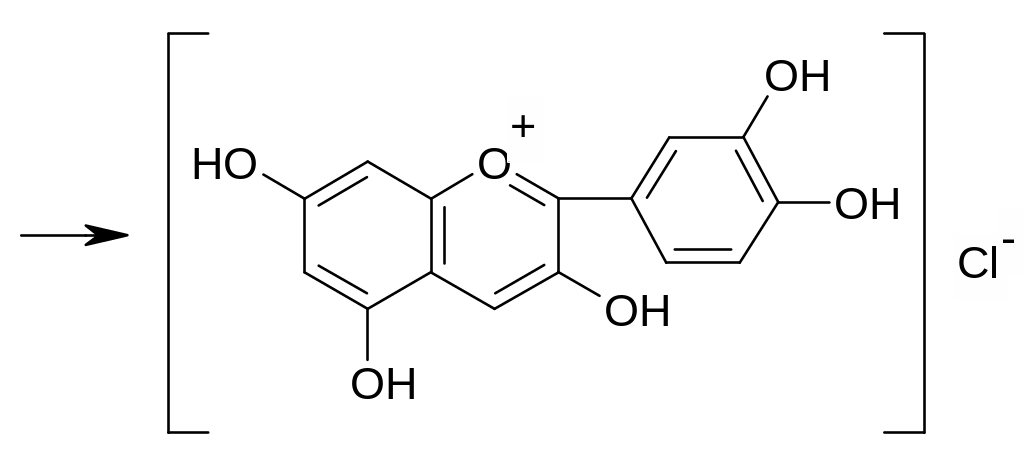
цианидин хлорид
Реакция очень чувствительна, основана на восстановлении карбонильной группы и образовании антоцианида.
Халконы и ауроны при помощи цианидиновой реакции не обнаруживаются, но при добавлении конц. HCl (без магния) образуют красное окрашивание за счет образования оксониевых солей.
Борно-лимонная реакция с реактивом Вильсона (по 0,5 г борной и лимонной кислот в метаноле).
Реакция отличия флавоноидов от фуранохромонов. Флавоноиды дают комплексы с борной кислотой желтой окраски с желто-зеленой флюоресценцией, которые не разрушаются лимонной кислотой (образование батохромного комплекса):
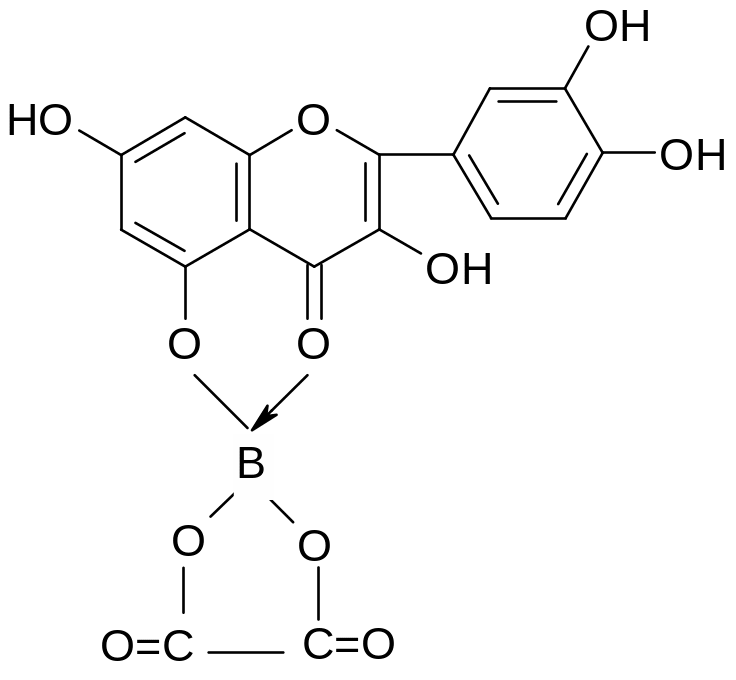
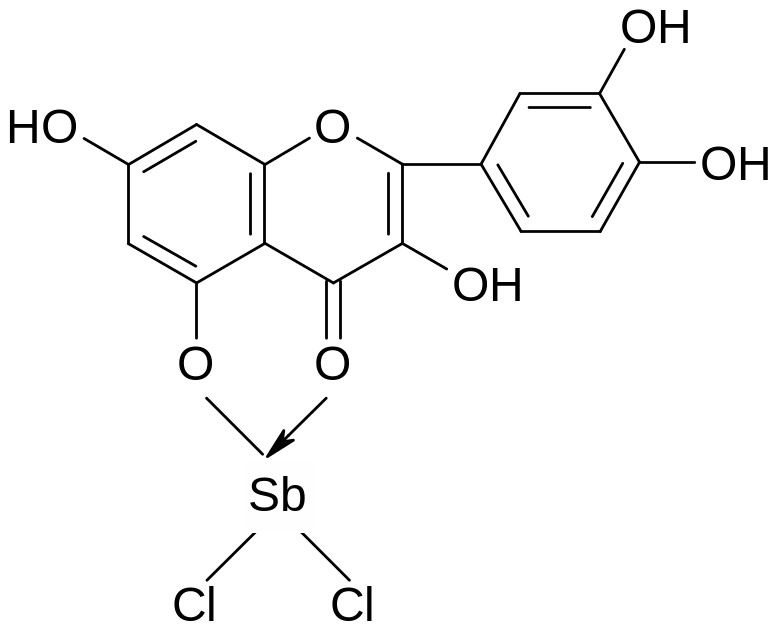
3. Реакция с треххлористой сурьмой.
5-оксифлавоны и 5-оксифлавонолы, взаимодействуя с треххлористой сурьмой, образуют комплексные соединения, окрашенные в желтый или красный цвет:
С 2-5 %-ным спиртовым раствором AlCl3 желто-зеленое окрашивание говорит о наличии флавоноидов. Образуются хелатные комплексы за счет водородных связей, возникающих между карбонильной и оксигруппой, желтого цвета с желто-зеленой флюоресценцией.
Эта реакция приведена в ГФ Х1 изд. для подтверждения подлинности сырья
зверобоя, горца перечного и птичьего. Аналогично образуются комплексы с солями циркония.
Реакция с солями железа (хлорид окисного железа), образуются комплексные соединения, окрашенные в черно-синий цвет, если флавоноиды триоксипроизводные и в зеленый, если диоксипроизводные.
Реакция с 1 %-ным раствором основного ацетата свинца.
Антоцианидины дают синий аморфный осадок. Флавоны, халконы и ауроны – осадки ярко-желтого цвета.
Реакция с 10 %-ным раствором щелочи с образованием фенолятов желтого цвета на флавоны и флавонолы. Антоцианидины образуют со щелочами соли от синего до оливково-зеленого цвета.
Реакция азосочетания с диазосоединениями. Образуется азокраситель оранжевого, красного или вишнево-красного цвета.
8. С 1 %-м раствором ванилина в конц. HCl образуют красно-малиновое окрашивание катехины (производные флороглюцина и резорцина).
4. С раствором аммиака, щелочи флавоны, флаваноны, флавонолы, флаванонолы дают желтое окрашивание, при нагревании переходящее в оранжевое или красное;
халконы и ауроны тотчас же дают красное или пурпурное окрашивание.
Чистые катехины окрашивания не дают, однако присутствие даже в небольшом количестве примесей (продуктов окисления) вызывает появление желтой окраски.
Антоцианы в присутствии аммиака или карбоната натрия дают синее или фиолетовое окрашивание.
5. С 1 %-м раствором ванилина в конц. HCl образуют красно-малиновое окрашивание катехины (производные флороглюцина и резорцина).
6. Флавоны, халконы, ауроны, содержащие свободные орто-гидроксильные группировки в кольце В, при обработке спиртовых растворов средним ук-
суснокислым свинцом образуют осадки, окрашенные в ярко-желтый и красный цвета.
Антоцианы образуют осадки, окрашенные как в красный, так и в синий цвета.
7. С 1-2 %-ным спиртовым раствором AlCl3 желто-зеленое окрашивание говорит о наличии флавоноидов.
С целью обнаружения флавоноидов в растительном материале широко
используется хроматография на бумаге и в тонком слое сорбента, колоночная хроматография.Используют различные системы растворителей:
БХ чаще всего БУВ (бутанол-уксусная кислота- вода) 4:1:5; 4:1:2;
ТСХ – хлороформ-метанол 8:3; 8:2.
Обнаружение компонентов на хроматограмме осуществляется просматриванием их в УФ свете.
Идентифицируют флавоноиды по характерному свечению на хроматограммах в УФ-свете и после проявления хромогенными реактивами.
Катехины и лейкоантоцианиды не флюоресцируют. Гликозиды флавонов и изофлавонов флюоресцируют голубым или синим светом, флавонолов – темно-коричневым или черным, агликоны флавонов – коричневым, флавонолов – желтым, халконы и ауроны имеют желтую или оранжевую флюоресценцию.
После просматривания в УФ свете хроматограммы можно обработать одним из реактивов:
1) 5 %-ным спиртовым раствором AlCl3 c последующим нагреванием при 105 0С в течение 3-5 минут; (ярко-желтая окраска пятна в видимом свете и яркую желто-зеленую флуоресценцию в УФ –свете);
2) с 5 %-ной SbCl3 в четыреххлористом углероде (реактив Мартини-Беттоло); Желтая или желто-оранжевая окраска указывает на наличие флавонов, флавонолов, флаванонов и изофлавонов;красная или красно-фиолетовая – халконов.
3) с 2 %-ным спиртовым раствором щелочи
4) при обработке пятна парами аммиака усиливается голубая флуоресценция (изофлавоноиды)
что позволяет получить зоны с более яркой флуоресценцией в УФ свете.
5) Реактив Вильсона (раствор борной и б\в лимонной кислоты в б\в метаноле)
6) Реакция азосочетания – на наличие 7-оксифлаванолов, 7-оксиизофлаванолов.
Хроматографические методы анализа.
С целью обнаружения флавоноидов в растительном материале широко
используется хроматография на бумаге и в тонком слое сорбента.
Обнаружение компонентов на хроматограмме осуществляется просматриванием их в УФ свете.
При этом флавоны, флавонол-3-гликозиды, флаваноны, халконы и их 7-гликозиды – в виде желтых или желто-зеленых пятен; флавонолы и их 7-гликозиды – в виде желтых или желто-зеленых пятен; ксантоны в виде оранжевых пятен.
Изофлавоны при этом не проявляются.
После просматривания в УФ свете хроматограммы можно обработать одним из реактивов:
1) 5 %-ным спиртовым раствором AlCl3 c последующим нагреванием при 105 0С в течение 3-5 минут; (ярко-желтая окраска пятна в видимом свете и яркую желто-зеленую флуоресценцию в УФ –свете);
2) с 5 %-ной SbCl3 в четыреххлористом углероде (реактив Мартини-Беттоло); Желтая или желто-оранжевая окраска указывает на наличие флавонов, флавонолов, флаванонов и изофлавонов;красная или красно-фиолетовая – халконов.
3) с 2 %-ным спиртовым раствором щелочи
4) при обработке пятна парами аммиака усиливается голубая флуоресценция (изофлавоноиды)
что позволяет получить зоны с более яркой флуоресценцией в УФ свете.
Реактив Вильсона (раствор борной и б\в лимонной кислоты в б\в метаноле)
5) Реакция азосочетания – на наличие 7-оксифлаванолов, 7-оксиизофлаванолов.
Количественное определение.
В последние годы все большее распространение получают различные:
1. физико-химические методы анализа, которые имеют ряд существенных преимуществ в сравнении, например, с гравиметрическими и титрометрическими методами, а именно, быстрота и точность определения, обнаружение даже незначительных количеств и, что особенно важно, возможность выделения отдельных флавоноидов из растительного сырья.
К таким методам относятся фотоэлектроколориметрия, спектрофотометрия, денситометрия с использованием хроматографии на бумаге и в тонком слое сорбента.
1. Сущность хроматоденситометрического метода заключается в выделении и разделении флавоноидов с непосредственной количественной денситометрической оценкой окрашенной зоны на хроматограмме.
Метод имеет преимущества в быстроте проведения анализа и точности определения, так как в данном случае исключается стадия элюирования.
2. фотоэлектроколориметрический метод, основанный на измерении оптической плотности окрашенных растворов, полученных в цветных реакциях флавоноидов с солями различных металлов (алюминия, циркония, титана, хрома, сурьмы), с лимонно-борным реактивом и на реакции восстановления цинком или магнием в кислой среде, в реакции азосочетания с солями диазония.
ГФ Х1 издания дает ФЭК-метод для определения содержания суммы флавоноидов в листьях вахты трехлистной. Предварительно сырье очищают от хлорофилла хлороформом, получают спиртовое извлечение флавоноидов, затем измеряют оптическую плотность окрашенного раствора с помощью фотоэлектроколориметра. Содержание суммы флавоноидов рассчитывают по калибровочному графику, построенному по стандартному образцу рутина.
Известна цветная реакция флавоноидов с азотнокислым и уксуснокислым уранилом, позволяющая количественно определять рутин в смеси с кверцитином.
В настоящее время широко используется метод спектрофотометричекий.
