
- •1. Атомно-мол.Теория
- •2. История развития пред-й о строении атома
- •4. Совр.Предст-я о строении атомов хим.Элементов
- •5. Периодический закон и строение атомов элементов
- •6. Теоретические основы совр.Моделей строения атомов
- •7. Строение элементов 4 периода8.Строение атомов элементов 5и 6 периодов
- •10. Типы хим.Связи
- •11. Ковалентная хим.Связь
- •3.6. Полярность и поляризуемость химической связи
- •12. Механизмы образования ковалентной хим.Связи
- •13. Водородная связь.Обьекты в кот.Она присутствует.
- •14. Металлическая связь
- •15. Силы Ван-дер-Ваальса
- •16. Теория гибридизации
- •17. Делокализация связи.
- •18. Роль атомных орбиталей в обр-ии хим.Связи
- •20. Методы описания ковалентной связи.
- •1 Теория метода валентных связей
- •2.Мо лкао
15. Силы Ван-дер-Ваальса
Межмолекулярное взаимодействие - взаимодействие молекул между собой, не приводящее к разрыву или образованию новых химических связей. В их основе, как и в основе химической связи, лежат электрические взаимодействия.
Силы Ван-дер-Ваальса включают все виды межмолекулярного притяжения и отталкивания. Они получили название в честь Я.Д. Ван-дер-Ваальса, который первым принял во внимание межмолекулярные взаимодействия для объяснения свойств реальных газов и жидкостей. Эти силы определяют отличие реальных газов от идеальных, существование жидкостей и молекулярных кристаллов. От них зависят многие структурные, спектральные и другие свойства веществ.
Основу ван-дер-ваальсовых сил составляют кулоновские силы взаимодействия между электронами и ядрами одной молекулы и ядрами и электронами другой. На определенном расстоянии между молекулами силы притяжения и отталкивания уравновешивают друг друга, и образуется устойчивая система.
Ван-дер-ваальсовы силы заметно уступают химическому связыванию. Например, силы, удерживающие атомы хлора в молекуле хлора почти в десять раз больше, чем силы, связывающие молекулы Cl2 между собой. Но без этого слабого межмолекулярного притяжения нельзя получить жидкий и твердый хлор.
Ориентационное взаимодействие
Полярные молекулы, в которых центры тяжести положительного и отрицательного зарядов не совпадают, например HCl, H2O, NH3, ориентируются таким образом, чтобы рядом находились концы с противоположными зарядами. Между ними возникает притяжение. Для взаимодействия двух диполей энергия притяжения между ними (энергия Кеезома) выражается соотношением: EК = −2 μ1 μ2 / 4π ε0 r3
Индукционное взаимодействие.
Взаимодействие между постоянным диполем и наведенным (индуцированным). Поляризация нейтральной частицы под действием внешнего поля (наведение диполя) происходит благодаря наличию у молекул свойства поляризуемости γ. Постоянный диполь может индуцировать дипольное распределение зарядов в неполярной молекуле. Под действием заряженных концов полярной молекулы электронные облака неполярных молекул смещаются в сторону положительного заряда и подальше от отрицательного. Неполярная молекула становитсяполярной, и молекулы начинают притягиваться друг к другу, только намного слабее, чем две полярные молекулы.
Дисперсионное взаимодействие
Между неполярными молекулами также может возникнуть притяжение. Электроны, которые находятся в постоянном движении, на миг могут оказаться окажется сосредоточенными с одной стороны молекулы, то есть неполярная частица станет полярной. Это вызывает перераспределение зарядов в соседних молекулах, и между ними устанавливаются кратковременные связи
16. Теория гибридизации
американский ученый Л. Полинг разработал теорию о гибридизации атомных орбиталей.
Основные положения теории гибридизации следующие:
а) введение гибридных орбиталей служит для описания направленных локализованных связей. Гибридные орбитали обеспечивают максимальное перекрывание АО в направлении локализованных σ-связей;
б) число гибридных орбиталей равно числу АО, участвующих в гибридизации;
в) гибридизуются близкие по энергии валентные АО независимо от того, заполнены они в атоме полностью, наполовину или пусты;
г) в гибридизации участвуют АО, имеющие общие признаки симметрии.
Гибридизация – выравнивание по форме и энергии АО (облаков) с образованием новых АО, одинаковых по форме и энергии. Новые облака называются гибридными, их число равно сумме АО, участвующих в гибридизации. как физический процесс, гибридизация орбиталей не существует. В гибридной АО электронная плотность смещается в одну сторону от ядра, поэтому при взаимодействии ее с АО другого атома происходит макс имальное перекрывание, которое приводит к повышению энергии связи. химические связи, образованные гибридными орбиталями, прочнее, а полученная молекула более устойчива.
Характер гибридизации валентных орбиталей центрального атома и их пространственное расположение определяют пространственную конфигурацию (геометрическую форму) молекул:
1. Если в химическую связь вступает атом, у которого на внешней оболочке имеется s- и р – электроны, то у данного атома в процессе образования связи происходит sp – гибридизация АО
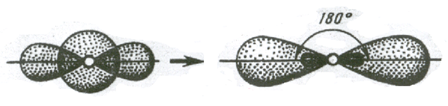
Две sp – гибридные орбитали расположены симметрично под углом 180˚, отсюда и связи, образуемые с участием электронов этих орбиталей, также располагаются под углом 180˚. Например, у атома бериллия sp – гибридизация орбиталей проявляется в молекуле BeCl2, которая вследствие этого имеет линейную форму. s-p – гибридизация характерна для атомов элементов II группы периодической системы (Be, Mg, Cd, Hg и т. д.), для углерода в СО2, в органических соединениях с тройной углерод – углеродной связью.
2. Если у атома, вступающего в химическую связь, на внешней оболочке имеется один s- и два p- электрона, то происходит sp2 – гибридизация АО

Три sp2 – гибридные орбитали расположены под углом 120˚. Под таким же углом располагаются и связи, образованные с участием электронов этих орбиталей. Например, вследствие sp2 – гибридизации орбиталей атома бора молекула BCl3 имеет треугольную форму.
sp2 – гибридизация встречается в молекулах элементов III группы периодической системы, а также в органических соединениях с двойной углерод – углеродной связью.
3. У атома, имеющего на внешней оболочке один s- и три р- электрона, при химическом взаимодействии происходит sp3 – гибридизация этих АО.
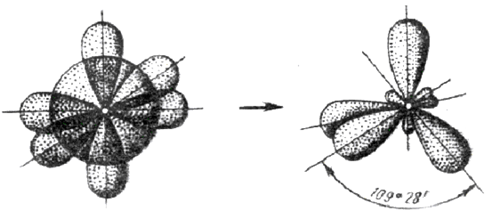
Четыре sp3 – гибридные орбитали симметрично ориентированы в пространстве под углом 109˚28′ к четырем вершинам тетраэдра (рис. 3.13, в). Тетраэдрическое расположение связей и форма тетраэдра характерны для элементов IV группы, в том числе для многих соединений углерода, например, CH4.
4. Возможны также более сложные виды гибридизации с участием d- и f- орбиталей атомов, при которых образуются молекулы ещё более сложной конфигурации.
Комбинация орбиталей типа одной s-, трех р- и одной d- приводит к sp3d-гибридизации. Это соответствует пространственной ориентации пяти sp3d-гибридных орбиталей к вершинам тригональной бипирамиды (рис. 3.13, г). В случае sp3d2-гибридизации шесть sp3d2-гибридных орби¬талей ориентируются к вершинам октаэдра (рис. 3.13, д). Ориентация семи орбиталей к вершинам пентагональной бипирамиды (рис. 3.13, е) соответствует sp3d3 (или sp3d2f) – гибридизации валентных орбиталей центрального атома молекулы (комплекса).
Для ряда молекул и ионов, особенно имеющих несимметричное строение, рассмотренных представлений оказывается недостаточно. В подобных случаях применяют теорию полной гибридизации (Джиллеспи), в которой и связывающие, и неподеленные электронные пары центрального атома подвергаются sp3 – гибридизации. sp3 – гибридизация центральных атомов имеет место в молекулах NH3, H2O и им подобным, образованным их электронными аналогами.
У атома азота на четыре sp3 – гибридные орбитали приходятся пять электронов. Следовательно, одна пара электронов оказывается несвязывающей и занимает одну из sp3-гибридных орбиталей, направленных к вершине тетраэдра (рис. 3.14). Молекула NH3 имеет форму тригональной пирамиды.
