
- •1. Атомно-мол.Теория
- •2. История развития пред-й о строении атома
- •4. Совр.Предст-я о строении атомов хим.Элементов
- •5. Периодический закон и строение атомов элементов
- •6. Теоретические основы совр.Моделей строения атомов
- •7. Строение элементов 4 периода8.Строение атомов элементов 5и 6 периодов
- •10. Типы хим.Связи
- •11. Ковалентная хим.Связь
- •3.6. Полярность и поляризуемость химической связи
- •12. Механизмы образования ковалентной хим.Связи
- •13. Водородная связь.Обьекты в кот.Она присутствует.
- •14. Металлическая связь
- •15. Силы Ван-дер-Ваальса
- •16. Теория гибридизации
- •17. Делокализация связи.
- •18. Роль атомных орбиталей в обр-ии хим.Связи
- •20. Методы описания ковалентной связи.
- •1 Теория метода валентных связей
- •2.Мо лкао
10. Типы хим.Связи
Основополагающий вклад в учение о строении химических соединений внес русский химик А. М. Бутлеров. Химическая связь – это сложные протонно-электронные взаимодействия атомов, которые приводят к образованию молекул простых или сложных веществ или кристаллов. Признак химической связи – устойчивость образовавшейся молекулы.Причина устойчивости – понижение полной энергии системы. природа химической связи едина – это взаимодействие электрических полей, образуемых электронами и ядрами атомов, участвующих в создании молекулы.Типы:ковалентная(общ.эл.пара),металлическая(,водородная,межмолекулярное взаимодействие(разноименные заряды на раз.частях молекул)
Основные характеристики химической связи:
1.Энергия связи, Есв, определяет ее прочность – это количество энергии, которое нужно затратить на ее разрыв или количество энергии, выделяемое при образовании молекулы из атомов). Энергия химической связи изменяется в интервале 40 ÷ 400 кДж/моль.
2. Длина связи, ℓ, - расстояние между центрами двух атомов, образующих молекулу. Измеряется в м (нм) или Å.
3. Валентный угол – угол между прямыми, соединяющими центры ядер атомов в молекуле. Валентными углами определяется пространственное строение молекул. Величины валентных углов зависят от природы атомов и характера связи. двухатомные молекулы типа А2 и АВ имеют линейную структуру: их валентные углы равны 180º.
По характеру распределения электронной плотности в веществе различают три основных типа химической связи: ковалентную, ионную и металлическую. В «чистом» виде перечисленные типы связи проявляются редко. Кроме того, между молекулами возникает водородная химическая связь и происходят вандерваальсовы взаимодействия.
Правило октета. В результате образования химической связи атомы могут приобретать такую же конфигурацию, как у благородных газов, которые (за исключением гелия) имеют на внешней оболочке восемь (октет) электронов.
11. Ковалентная хим.Связь
Химическая связь между атомами, осуществляемая обобществленными электронами, называется ковалентной. Ковалентная связь возникает за счет образования общих электронных пар между атомами в молекуле.
Идея об образовании этой хим. связи высказана в 1916г американским физико – химиком Дж. Льюисом.
Ковалентная связь существует между атомами как в молекулах, так и в кристаллах. Она возникает как между одинаковыми атомами (например, в молекулах Н2, Cl2, О2, в кристалле алмаза), так и между разными атомами (например, в молекулах Н2О и NН3, в кристаллах SiC).
Ковалентная связь обладает следующими свойствами:насыщаемость; направленность; полярность и поляризуемость.
Поляризуемость – изменение полярности ков.связи под действием внеш.электрического поля.
Насыщаемость ковалентной связи (валентные возможности атома, максимальная валентность) характеризует способность атомов участвовать в образовании определенного ограниченного числа ковалентных связей и определяет стехиометрический состав молекул. Принцип насыщаемости указывает на то, что устойчивым соединением должно быть NH3, а не NH2, NH или NH4.
Валентность. Валентность элемента (В) - его способность к образованию химических связей. В представлении МВС численное значение валентности соответствует числу ковалентных связей, которые образует атом.Количественной мерой валентности в обменном механизме метода ВС считают число неспаренных электронов у атома в основном или возбужденном состоянии атома.
Например, валентность элементов главной подгруппы I группы равна единице, так как на внешнем уровне атомы этих элементов имеют один электрон.
Постоянную валентность проявляют s – элементы, а переменную – р- и d- элементы(исключение составляют N, O, F; они в пределах 2-го энергетического уровня не имеют свободных атомных орбиталей). Низшая валентность проявляется в невозбужденном состоянии, высшая – в наиболее возбужденном. Для большинства атомов высшая валентность равна номеру группы. Таким образом, суммарная валентность элемента равна числу не спаренных электронов (обменный механизм) плюс число связей, образованных по донорно-акцепторному механизму.
Направленность заключается в том, что максимальное перекрывание валентных электронных облаков взаимодействующих атомов возможно при определенной их взаимной ориентации. Направленность ковалентной связи определяет пространственную конфигурацию молекул.
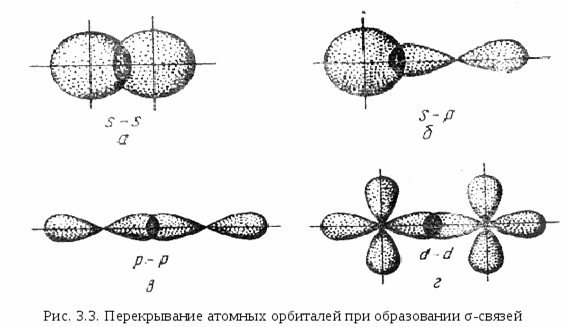
В зависимости от направления перекрывания атомных орбиталей различают σ -, π – и δ – связи.
Связь, образованная перекрыванием АО по линии, соединяющей ядра взаимодействующих атомов, называется σ – связью. Сигма-связь может возникать при перекрывании s – орбиталей, s – , p – орбиталей , р – орбиталей , d – орбиталей , а также d – и s – орбиталей, и f – орбиталей с друг другом и другими орбиталями. Сигма – связь обычно охватывает два атома и не простирается за их пределы, поэтому является локализованной двухцентровой связью. Простейший случай σ – связи наблюдается у молекулы Н2, образующейся за счет перекрывания s-орбиталей атомов водорода (s-s перекрывание, рис. 3.4). Геометрическая форма молекулы линейная.
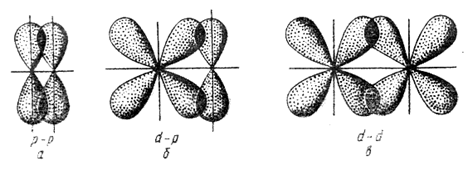
Связь, образованная перекрыванием АО по обе стороны линии, соединяющей ядра атомов (боковые перекрывания), называется π-связью. Пи-связь может образовываться при перекрывании р – р-орбиталей, p – d-орбиталей , d – d-орбиталей, а также f – p-, f – d- и f – f-орбиталей.
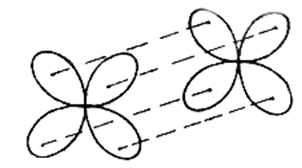
Связь, образованная перекрыванием d-орбиталей всеми четырьмя «лепестками» называется δ-связью (дельта-связью) Соответственно, s-элементы могут образовывать только σ-связи, р-элементы – σ- и π-связи, d-элементы – σ-, π- и δ-связи, а f-элементы – σ-, π-, δ- и еще более сложные связи.
Кратность связи. Связь, которая образована одной электронной парой между двумя атомами, называется одинарной. Одинарная связь всегда σ – связь. При наложении π-связи на σ-связь образуется двойная связь, например в молекулах кислорода, этилена, диоксида углерода. Кратная связь изображается двумя черточками: О =О, С = С, О = С = О. При наложении двух π-связей на σ-связь возникает тройная связь, например в молекулах азота, ацетилена и оксида углерода. Тройная связь изображается тремя черточками: N ≡ N, ─ C ≡ C ─, C ≡ O. Энергия тройной связи выше, а длина связи ниже, чем энергии и длины простой и двойной связей.
Число связей между атомами в МВС называется кратностью связи.
