
- •Атомно-молекулярное учение
- •2.10.1. Расчет относительных и абсолютных масс атомов и молекул
- •4) Строение атома
- •6.3. Атом водорода. Линейчатые спектры
- •Экспериментальное подтверждение гипотезы де Бройля. Опыт Дэвиссона и Джермера.
- •Дифракция электронов на двух щелях
- •Содержание
- •Распределение электронов по орбиталям в водородоподобных и многоэлектронных атомах[править | править исходный текст]
- •Взаимодействие ионов
- •Ионные радиусы
- •Энергия ионной связи
- •Ковалентная химическая связь
- •Виды гибридизации[править | править исходный текст]
- •Межмолекулярная и внутримолекулярная водородная связь
- •Межмолекулярная и внутримолекулярная водородная связь
- •Силы межмолекулярного взаимодействия
- •Недостатки существующей классификации термодинамических систем
- •Внутренняя энергия и энтальпия
- •Закон Гесса[править | править исходный текст]
- •4. Энергия Гиббса. (g).
- •5. Химический потенциал ().
- •Второй закон термодинамики. Направление химических процессов.
- •[ Лед ] ↔ {вода} ↔ (пар)
- •Первый закон Рауля
- •Отклонения от закона Рауля
- •Второй закон Рауля
- •Понижение температуры кристаллизации растворов
- •Повышение температуры кипения растворов
- •Криоскопическая и эбулиоскопическая константы
- •Растворы электролитов
- •Свойства разбавленных растворов неэлектролитов
- •Понижение давления пара над раствором
- •Температура кипения и замерзания
- •Значения криоскопических и эбуллиоскопических постоянных некоторых растворителей
- •Основные положения теории Аррениуса.
- •Диссоциация солей, кислот и оснований
- •Классификация
- •2.Сильные и слабые электролиты. Константа диссоциации.
- •3.Закон разбавления Оствальда.
- •Изображение реакций ионного обмена
- •Правила написания реакций ионного обмена
- •Окислительно-восстановительные реакции подразделяют на межмолекулярные, внутримолекулярные, диспропорционирования (или самоокисления-самовосстановления), конпропорционирования.
- •Измерение потенциалов
- •Способы устранения омической составляющей при измерении
- •Основные факторы, влияющие на потенциал
- •Вывод уравнения Нернста
- •Применение электролиза в технике
- •Формулировка законов
- •Математический вид
- •Электрохимическая коррозия
- •Коррозия оцинкованного и луженого железа при местном повреждении
Распределение электронов по орбиталям в водородоподобных и многоэлектронных атомах[править | править исходный текст]
По мере увеличения суммарного числа электронов в атомах (при возрастании зарядов их ядер, или порядковых номеров химических элементов) атомные орбитали заселяются таким образом, что появление электронов на орбитали с более высокой энергией зависит только отглавного квантового числа n и не зависит от всех остальных квантовых чисел, в том числе и от l. Физически это означает, что в водородоподобном атоме (в отсутствие межэлектронного отталкивания) орбитальная энергия электрона определяется только пространственной удаленностью зарядовой плотности электрона от ядра и не зависит от особенностей его движения в поле ядра. Поэтому энергетическая последовательность орбиталей в водородоподобном атоме выглядит просто:
1s<2s=2p<3s=3p=3d<4s=4p=4d=4f<5s...
Здесь орбитальная энергия электрона повышается только по мере увеличения главного квантового числа и не меняется при увеличении орбитального квантового числа l; состояния с различными значениями l, но с одним и тем же значением n (например, 3s, Зр, 3d) энергетически эквивалентны, то есть соответствующие атомные орбитали (3s, Зр, 3d) обладают одинаковой энергией и оказываются энергетически вырожденными (не следует путать обсуждаемое вырождение по энергии атомных орбиталей различного типа в гипотетических водородоподобных атомах с энергетическим вырождением атомных орбиталей одного и того же типа, например Зрx, Зру и Зрz в реальных изолированных атомах).
В многоэлектронных атомах в результате эффекта межэлектронных взаимодействий происходит энергетическое расщепление (расхождение) орбиталей различного типа, но с одним и тем же значением главного квантового числа (3s<3p<3d и т. д.). Если бы это расщепление было небольшим и меньшим расщепления по энергии атомных орбиталей под воздействием изменения главного квантового числа n, то энергетическая последовательность атомных орбиталей выглядела бы так:
1s«2s<2p"3s<3p<3d"4s<4p<4d<4f"5s...
В действительности же расщепление по l, начиная с n≥З, оказывается большим, чем расщепление по n. Сложный характер явления межэлектронных взаимодействий предопределяет сильную зависимость орбитальной энергии каждого электрона уже не только от пространственной удаленности его зарядовой плотности от ядра (от главного квантового числа n), но и от формы его движения в поле ядра (от орбитального квантового числа l). Именно межэлектронное взаимодействие приводит к резко усложнённой (по сравнению с вышеописанной) энергетической последовательности заселяющихся электронами атомных орбиталей. Итак, в реальных многоэлектронных атомах картина энергетического распределения орбиталей оказывается очень сложной. Строгая квантовомеханическая теория электронного строения атомов и экспериментальная спектроскопия обнаруживают энергетическую последовательность атомных орбиталей в следующем виде:
![]()
Эта
энергетическая последовательность
легко может быть описана при помощи
эмпирического правила суммы двух первых
квантовых чисел, разработанного в 1951-м
году В. М. Клечковским и
иногда называемого правилом (n+l).
Это правило основано на зависимости
орбитальной энергии от квантовых
чисел n и l и
описывает энергетическую последовательность
атомных орбиталей как функцию суммы ![]() .
Суть его очень проста:
.
Суть его очень проста:
орбитальная
энергия последовательно повышается по
мере увеличения суммы
,
причём при одном и том же значении этой
суммы относительно меньшей энергией
обладает атомная орбиталь с меньшим
значением главного квантового
числа
. Например,
при ![]() орбитальные
энергии подчиняются последовательности
орбитальные
энергии подчиняются последовательности ![]() ,
так как здесь для
,
так как здесь для ![]() -орбитали
главное квантовое число наименьшее
-орбитали
главное квантовое число наименьшее ![]() ,
для
,
для ![]() -орбитали
-орбитали ![]() ;
наибольшее
,
-орбиталь
занимает промежуточное положение
;
наибольшее
,
-орбиталь
занимает промежуточное положение ![]() .
.
Или же:
При
заполнении орбитальных оболочек атома
более предпочтительны (более энергетически
выгодны), и, значит, заполняются раньше
те состояния, для которых сумма главного
квантового числа
и
побочного (орбитального) квантового
числа ![]() ,
т.е.
,
имеет меньшее значение.
,
т.е.
,
имеет меньшее значение.
Правило (n+l) в целом хорошо иллюстрирует таблица 1, где по мере постепенного возрастания суммы (n+l) приведена энергетическая последовательность атомных орбиталей. В этой таблице не указаны нереальные (запрещенные квантовой механикой атома) варианты, для которых не выполняется обязательное требование n>l, в частности не указаны комбинации для (n+l)=6:
n |
1 |
2 |
3 |
l |
5 |
4 |
3 |
Таблица 1. Энергетическая последовательность орбиталей в изолированных атомах |
||||
(n+l) |
n |
l |
Атомные орбитали |
|
1 |
1 |
0 |
1s |
Первый период |
2 |
2 |
0 |
2s |
Второй период |
3 |
2 |
1 |
2p |
|
3 |
0 |
3s |
Третий период |
|
4 |
3 |
1 |
3p |
|
4 |
0 |
4s |
Четвёртый период |
|
5 |
3 |
2 |
3d |
|
4 |
1 |
4p |
||
5 |
0 |
5s |
Пятый период |
|
6 |
4 |
2 |
4d |
|
5 |
1 |
5p |
||
6 |
0 |
6s |
Шестой период |
|
7 |
4 |
3 |
4f |
|
5 |
2 |
5d |
||
6 |
1 |
6p |
||
7 |
0 |
7s |
Седьмой период |
|
8 |
5 |
3 |
5f |
|
6 |
2 |
6d |
||
7 |
1 |
7p |
||
8 |
0 |
8s |
Начало восьмого периода |
|
Приведённую в таблице очерёдность заполнения электронами атомных орбиталей удобно представить в виде схемы:
Принцип Паули
[править | править исходный текст]
Материал из Википедии — свободной энциклопедии
Эта статья о квантовой физике; о сходной по названию шутке научного юмора см.: Эффект Паули.
|
|||||||||
|
|||||||||
Принцип неопределённости |
|||||||||
Введение Математические основы |
|||||||||
|
|||||||||
См. также: Портал:Физика |
При́нцип Па́ули (принцип запрета) — один из фундаментальных принципов квантовой механики, согласно которому два и более тождественных фермиона (частиц с полуцелым спином) не могут одновременно находиться в одномквантовом состоянии.
Принцип был сформулирован для электронов Вольфгангом Паули в 1925 г. в процессе работы над квантомеханической интерпретацией аномального эффекта Зеемана и в дальнейшем распространён на все частицы с полуцелым спином. Полное обобщённое доказательство принципа было сделано им в теореме Паули (теореме о связи спина со статистикой) в 1940 г. в рамках квантовой теории поля. Из этой теоремы следовало, что волновая функция системы фермионовявляется антисимметричной относительно их перестановок, поведение систем таких частиц описывается статистикой Ферми — Дирака.
Принцип Паули можно сформулировать следующим образом: в пределах одной квантовой системы, в данном квантовом состоянии, может находиться только один фермион, состояние другого должно отличаться хотя бы одним квантовым числом.
В
статистической физике принцип Паули
иногда формулируется в терминах чисел
заполнения:
в системе одинаковых частиц, описываемых
антисимметричной волновой функцией,
числа заполнения могут принимать лишь
два значения ![]()
Строение атомов и принцип Паули[править | править исходный текст]
Принцип Паули помогает объяснить разнообразные физические явления. Следствием принципа является наличие электронных оболочек в структуре атома, из чего, в свою очередь, следует разнообразие химических элементов и их соединений. Количество электронов в отдельном атоме равно количеству протонов. Так как электроны являются фермионами, принцип Паули запрещает им принимать одинаковые квантовые состояния. В итоге, все электроны не могут быть в одном квантовом состоянии с наименьшей энергией (для невозбуждённого атома), а заполняют последовательно квантовые состояния с наименьшей суммарной энергией (при этом не стоит забывать, что электроны неразличимы, и нельзя сказать, в каком именно квантовом состоянии находится данный электрон). Примером может служить невозбуждённый атом лития (Li), у которого два электрона находятся на 1S орбитали (самой низкой по энергии), при этом у них отличаются собственные моменты импульса и третий электрон не может занимать 1S орбиталь, так как будет нарушен запрет Паули. Поэтому, третий электрон занимает 2S орбиталь (следующая, низшая по энергии, орбиталь после 1S).
Литература[править | править исходный текст]
Правило Хунда определяет порядок заполнения орбиталей определённого подслоя и формулируется следующим образом: суммарное значение спинового квантового числа электронов данного подслоя должно быть максимальным. Сформулировано Фридрихом Хундом в 1925 году.
Это означает, что в каждой из орбиталей подслоя заполняется сначала один электрон, а только после исчерпания незаполненных орбиталей на эту орбиталь добавляется второй электрон. При этом на одной орбитали находятся два электрона с полуцелыми спинамипротивоположного знака, которые спариваются (образуют двухэлектронное облако) и, в результате, суммарный спин орбитали становится равным нулю.
Правило октета (октетная теория) — предложено Г. Н. Льюисом для объяснения причин образования ковалентных химических связей. Согласно этому правилу при образовании молекул атомы удовлетворяют свою потребность в достижении 8 электронной валентной оболочки, подобной электронной конфигурации благородных газов за счет попарного обобществления своих валентных электронов. По своей важности это фундаментальное открытие Льюиса стоит в одном ряду с такими открытиями, как Периодический закон элементов и теория строения органических соединений. Широко распространенное мнение, что правило октета выполняется лишь в ограниченном числе случаев также ошибочно, как и утверждение того, что Периодический закон элементов не имеет всеобщего характера. Все примеры «невыполнения» правила октетов можно подразделить на следующие три группы:
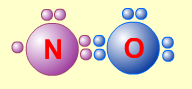
1. Сумма валентных электронов атомов, образующих молекулу, нечётна. Пример — молекула оксида азота NO.
![]()
В данном случае сумма валентных электронов атома азота (5) и кислорода (6) равна 11, поэтому в этой молекуле атом кислорода достигает восьмиэлектронной оболочки, а атом азота — нет. В данном случае изначально невозможно достижение обоими атомами восьмиэлектронной оболочки. Стремление атома азота заполнить свою электронную оболочку объясняет химическую реакционную способность этой молекулы.
2. Молекула образуется за счет трехцентровых связей, например KI3. В этой молекуле анион иода связан с молекулой иода трехцентровой четырехэлектронной связью. Аналогичные трехцентровые, но двухэлектронные связи присутствуют в молекуле B2H6.
3. В образовании химических связей принимают участие d-орбитали. В этом случае правило октетов (в пределе, то есть в случае участия всех пяти d-орбиталей) преобразуется в правило 18-электронов. Поскольку в целом ряде случаев участие d-орбиталей в образовании химических связей у некоторых элементов остается спорным вопросом, возникает иллюзия невыполнения правила октетов. Классическими примерами выполнения правила 18-электронов являются молекулы Fe(CO)5, Ni(CO)4, Co2(CО)8, Fe(C5H5)2 (ферроцен)и многие другие.
Таким образом, главным в правиле октетов Льюиса является не цифра 8 (или 18), а обобществление электронов как основа образования ковалентной химической связи, и приближение за счет этого к электронной конфигурации инертного газа — восьмиэлектронной или восемнадцатиэлектронной.
Правило К
Заполнение электронами орбиталей в атоме происходит в порядке возрастания суммы главного и орбитального квантовых чисел ~n+l. При одинаковой сумме раньше заполняется орбиталь с меньшим значением ~n.
8)
Периодический закон был сформулирован Д. И. Менделеевым в следующем виде (1871): «свойства простых тел, а также формы и свойства соединений элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса».[1]
С развитием атомной физики и квантовой химии Периодический закон получил строгое теоретическое обоснование. Благодаря классическим работам Й. Ридберга (1897), А. Ван-ден-Брука (1911), Г. Мозли (1913) был раскрыт физический смысл порядкового (атомного) номера элемента. Позднее была создана квантово-механическая модель периодического изменения электронного строения атомов химических элементов по мере возрастания зарядов их ядер (Н. Бор, В. Паули, Э. Шрёдингер, В. Гейзенберг и др.).
В настоящее время Периодический закон Д. И. Менделеева имеет следующую формулировку: «свойства химических элементов, а также формы и свойства образуемых ими простых веществ и соединений находятся в периодической зависимости от величины зарядов ядер их атомов».
Особенность Периодического закона среди других фундаментальных законов заключается в том, что он не имеет выражения в виде математического уравнения. Графическим (табличным) выражением закона является разработанная Менделеевым Периодическая система элементов.
Периодический закон универсален для Вселенной: как образно заметил известный русский химик Н. Д. Зелинский, Периодический закон явился «открытием взаимной связи всех атомов в мироздании».
В 1869 году Д.И.Менделеев сформулировал фундаментальный закон природы - закон периодичности. "Свойства простых тел, также формы и свойства соединений элементов, находятся в периодической зависимости от величины атомных вевов элементов" На основании этого закона и была построена периодическая система химических элементов. Один из вариантов периодической системы представлен ниже.
Закон Мозли — закон, связывающий частоту спектральных линий характеристического рентгеновского излученияатома химического элемента с его порядковым номером. Экспериментально установлен английским физикомГенри Мозли в 1913 году.
Формулировка закона Мозли[править | править исходный текст]
Согласно
Закону Мозли, корень
квадратный из
частоты
спектральной
линии характеристического
излучения элемента есть линейная
функция его
порядкового номера ![]() :
: ![]()
где ![]() — постоянная
Ридберга,
— постоянная
Ридберга, ![]() — постоянная
экранирования,
— главное
квантовое число.
На диаграмме Мозли зависимость
от
представляет
собой ряд прямых (К-, L-, М- и т. д. серии,
соответствующие значениям n = 1, 2, 3,...).
— постоянная
экранирования,
— главное
квантовое число.
На диаграмме Мозли зависимость
от
представляет
собой ряд прямых (К-, L-, М- и т. д. серии,
соответствующие значениям n = 1, 2, 3,...).
Закон Мозли явился неопровержимым доказательством правильности размещения элементов в периодической системе элементов Д. И. Менделеева и содействовал выяснению физического смысла .
В соответствии с Законом Мозли, рентгеновские характеристические спектры не обнаруживают периодических закономерностей, присущих оптическим спектрам. Это указывает на то, что проявляющиеся в характеристических рентгеновских спектрах внутренние электронные оболочки атомов всех элементов имеют аналогичное строение.
Более поздние эксперименты выявили некоторые отклонения от линейной зависимости для переходных групп элементов, связанные с изменением порядка заполнения внешних электронных оболочек, а также для тяжёлых атомов, появляющиеся в результате релятивистских эффектов (условно объясняемых тем, что скорости внутренних электронов сравнимы со скоростью света).
В зависимости от ряда факторов — от числа нуклонов в ядре атома (изотопический сдвиг), состояния внешних электронных оболочек (химический сдвиг) и пр. — положение спектральных линий на диаграмме Мозли может несколько изменяться. Изучение этих сдвигов позволяет получать детальные сведения об атоме.

Причина изменения свойств также объясняется строением атомов химических элементов.
Каждый период начинается элементом щелочным металлом (исключение – первый период), в атомах которых на внешнем энергетическом уровне имеются один s – электрон. Общая электронная формула строения внешнего энергетического уровня щелочных металлов ns1 , где n – номер периода.
Каждый период заканчивается элементом благородным газом. В атомах элементов благородных газов на внешнем энергетическом уровне имеются два s- и шесть p-электронов. Общая электронная формула строения внешнего энергетического уровня благородных газовns2np6 , где n - номер периода (исключение: гелий He - ns2).
Период - это горизонтальная последовательность элементов по возрастанию порядкового (атомного) номера элемента, атомы которых имеют одинаковое число энергетических уровней, численно равное номеру периода.
В периодах металлические свойства уменьшаются, а неметаллические свойства увеличиваются.
В больших периодах изменения свойств происходят медленнее, что объясняется появлением десяти d-элементов (4-й, 5-й периоды) и четырнадцати f-элементов (6-й, 7-й периоды).
По группам (в главных подгруппах) металлические свойства увеличиваются, а неметаллические уменьшаются.
Группа - это вертикальная последовательность элементов по возрастанию порядкового (атомного) номера, обладающая схожими свойствами.
Главная подгруппа - это вертикальная последовательность s- и p-элементов с одинаковым числом электронов на внешнем энергетическом уровне, равным номеру группы.
Побочная подгруппа - это вертикальная последовательность d- и f-элементов, которые имеют одинаковое суммарное количество валентных электронов.
Следовательно, возможна третья формулировка Периодического закона, которая отражает причину периодического изменения свойств.
Свойства химических элементов и образованных ими соединений находятся в периодической зависимости от строения внешних энергетических уровней атомов
9)
Классификация химических элементов основана на их свойствах и свойствах их соединений. Химические свойства очень сложны и многообразны, поэтому все попытки классифицировать элементы, исходя только из химических свойств образуемых ими веществ, оказывались неудачными. Только привлечение характеристики, лежащей вне области химии - относительного атомного веса элементов - стало первым шагом для создания стройной системы химических элементов.
Понятие атомного веса ввел на рубеже XVIII и XIX веков Дж. Дальтон. К этому времени были известны десятки химических элементов. Однако химикам не удавалось продвинуться в их классификации дальше, чем разделение элементов на металлы и неметаллы, причем признаками этих классов элементов служили скорее физические свойства образованных ими простых веществ, чем химические. И все же для некоторых элементов наблюдалось явное сходство химических свойств. Похожими друг на друга были соединения натрия и калия (тогда еще не полученных в чистом виде), хлора и фтора.
За первую половину XIX века химики открыли 25 новых химических элементов. В течение короткого времени были выделены платиновые металлы, получены в чистом виде щелочные и щелочноземельные металлы. К середине XIX века число известных элементов приблизилось к шестидесяти. Многие химики пытались найти связь между химическими свойствами и атомным весом давно известных и вновь открытых элементов. Однако создать естественную систему химических элементов удалось лишь Д.И. Менделееву.
химический элемент
Определения в Интернете
Хими́ческий элеме́нт — совокупность атомов с одинаковым зарядом ядра и числом протонов, совпадающим с порядковым номером в таблице Менделеева. Каждый химический элемент имеет свои название и символ, которые приводятся в Периодической системе элементов Менделеева. ...
Период — строка периодической системы химических элементов, последовательность атомов по возрастаниюзаряда ядра и заполнению электронами внешней электронной оболочки.

Семейства химических элементов |
|||
|
Щелочные металлы |
|
Неметаллы |
|
Щёлочноземельные металлы |
|
Галогены |
|
Переходные металлы |
|
Инертные газы |
|
Постпереходные металлы |
|
Лантаноиды |
|
Полуметаллы — металлоиды |
|
Актиноиды |
|
Суперактиноиды |
|
|
10)
Периодическая таблица систематизирует не только элементы, но и самые разнообразные их свойства. Химику часто бывает достаточно иметь перед глазами Периодическую таблицу для того, чтобы правильно ответить на множество вопросов (не только экзаменационных, но и научных).
Заглянем еще раз в Периодическую таблицу. Помимо глубокой фундаментальной связи между элементами, она отражает ряд полезных для изучения химии закономерностей. Рассмотрим важнейшие из них (рис. 4-6).
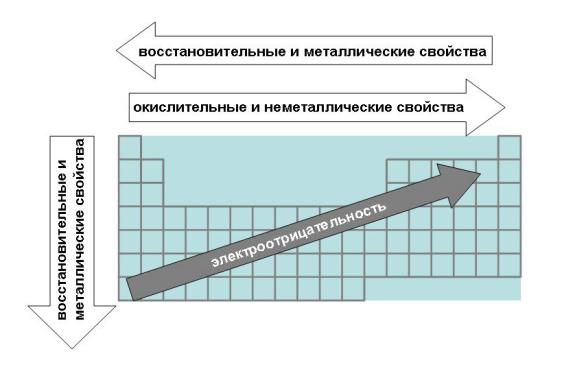
Рис.4-6. Закономерности Периодической таблицы, связанные с электроотрицательностью, металлическими и окислительно-восстановительными свойствами элементов.
а) Закономерности, связанные с металлическими и неметаллическими свойствами элементов.
1. При перемещении вдоль периода СПРАВА НАЛЕВО металлические свойства элементовУСИЛИВАЮТСЯ. В обратном направлении возрастают неметаллические.
Это объясняется тем, что правее находятся элементы, электронные оболочки которых ближе к октету. Элементы в правой части периода менее склонны отдавать свои электроны для образования металлической связи и вообще в химических реакциях.
Например, углерод - более выраженный неметалл, чем его сосед по периоду бор, а азот обладает еще более яркими неметаллическими свойствами, чем углерод.
Слева направо в периоде также увеличивается и заряд ядра. Следовательно, увеличивается притяжение к ядру валентных электронов и затрудняется их отдача.
Н![]() аоборот,
s-элементы в левой части таблицы имеют
мало электронов на внешней оболочке и
меньший заряд ядра, что способствует
образованию именно металлической связи.
За понятным исключением водорода и
гелия (их оболочки близки к завершению
или завершены!), все s-элементы являются
металлами; p-элементы могут быть как
металлами, так и неметаллами, в зависимости
от того - в левой или правой части таблицы
они находятся.
аоборот,
s-элементы в левой части таблицы имеют
мало электронов на внешней оболочке и
меньший заряд ядра, что способствует
образованию именно металлической связи.
За понятным исключением водорода и
гелия (их оболочки близки к завершению
или завершены!), все s-элементы являются
металлами; p-элементы могут быть как
металлами, так и неметаллами, в зависимости
от того - в левой или правой части таблицы
они находятся.
У d- и f-элементов, как мы знаем, есть "резервные" электроны из "предпоследних" оболочек, которые усложняют простую картину, характерную для s- и p-элементов. В целом d- и f-элементы гораздо охотнее проявляют металлические свойства.
Подавляющее число элементов является металлами и только 22 элемента относят к неметаллам: это H, B, C, Si, N, P, As, O, S, Se, Te, а также все галогены и инертные газы.
Некоторые элементы в связи с тем, что они могут проявлять лишь слабые металлические свойства, относят к полуметаллам.
Что такое полуметаллы? Если выбрать из Периодической таблицы p-элементы и записать их в отдельный "блок" (это сделано в “длинной” форме таблицы), то обнаружится закономерность, показанная на рис. 4-7. Левая нижняя часть блока содержит типичные металлы, правая верхняя - типичные неметаллы. Элементы, занимающие места на границе между металлами и неметаллами, иногда называют полуметаллами.
Р![]() ис.
4-7. Полуметаллы расположены примерно
вдоль диагонали, проходящей от левого
верхнего к правому нижнему углу блока
р-элементов в Периодической таблице.
ис.
4-7. Полуметаллы расположены примерно
вдоль диагонали, проходящей от левого
верхнего к правому нижнему углу блока
р-элементов в Периодической таблице.
Полуметаллы имеют ковалентную кристаллическую решетку при наличии металлической проводимости (электропроводности). Валентных электронов у них либо недостаточно для образования полноценной "октетной" ковалентной связи (как в боре), либо они не удерживаются достаточно прочно (как в тeллуре или полонии) из-за больших размеров атома. Поэтому связь в ковалентных кристаллах этих элементов имеет частично металлический характер.
Некоторые полуметаллы (кремний, германий) являются полупроводниками. Полупроводниковые свойства этих элементов объясняются многими сложными причинами, но одна из них - существенно меньшая (хотя и не нулевая) электропроводность, объясняемая слабой металлической связью. Роль полупроводников в электронной технике чрезвычайно важна.
2. При перемещении СВЕРХУ ВНИЗ вдоль групп УСИЛИВАЮТСЯ МЕТАЛЛИЧЕСКИЕсвойства элементов. Это связано с тем, что ниже в группах расположены элементы, имеющие уже довольно много заполненных электронных оболочек. Их внешние оболочки находятся дальше от ядра. Они отделены от ядра более толстой "шубой" из нижних электронных оболочек и электроны внешних уровней удерживаются слабее.
б) Закономерности, связанные с окислительно-восстановительными свойствами. Изменения электроотрицательности элементов.
3. Перечисленные выше причины объясняют, почему СЛЕВА НАПРАВО УСИЛИВАЮТСЯ ОКИСЛИТЕЛЬНЫЕ свойства, а при движении СВЕРХУ ВНИЗ - ВОССТАНОВИТЕЛЬНЫЕсвойства элементов.
Последняя закономерность распространяется даже на такие необычные элементы, как инертные газы. У "тяжелых" благородных газов криптона и ксенона, которые находятся в нижней части группы, удается "отобрать" электроны и получить их соединения с сильными окислителями (фтором и кислородом), а для "легких" гелия, неона и аргона это осуществить не удается.
В
 правом верхнем углу таблицы находится
самый активный неметалл-окислитель
фтор (F), а в левом нижнем углу - самый
активный металл-восстановитель цезий
(Cs). Цезий настолько активен, что
самовозгорается на воздухе (посмотрите
опыт из "Единой коллекции цифровых
образовательных ресурсов"). Элемент
франций (Fr) должен быть еще более активным
восстановителем, но его химические
свойства изучать крайне трудно из-за
быстрого радиоактивного распада.
правом верхнем углу таблицы находится
самый активный неметалл-окислитель
фтор (F), а в левом нижнем углу - самый
активный металл-восстановитель цезий
(Cs). Цезий настолько активен, что
самовозгорается на воздухе (посмотрите
опыт из "Единой коллекции цифровых
образовательных ресурсов"). Элемент
франций (Fr) должен быть еще более активным
восстановителем, но его химические
свойства изучать крайне трудно из-за
быстрого радиоактивного распада.
4. По той же причине, что и окислительные свойства элементов, ихЭЛЕКТРООТРИЦАТЕЛЬНОСТЬ ВОЗРАСТАЕТ тоже СЛЕВА НАПРАВО, достигая максимума у галогенов. Не последнюю роль в этом играет степень завершенности валентной оболочки, ее близость к октету.
5. При перемещении СВЕРХУ ВНИЗ по группам ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬ УМЕНЬШАЕТСЯ. Это связано с возрастанием числа электронных оболочек, на последней из которых электроны притягиваются к ядру все слабее и слабее.
в) Закономерности, связанные с размерами атомов.
6. Размеры атомов (АТОМНЫЕ РАДИУСЫ) при перемещении СЛЕВА НАПРАВО вдоль периода УМЕНЬШАЮТСЯ. Это объясняют тем, что электроны все сильнее притягиваются к ядру по мере возрастания заряда ядра. Даже увеличение числа электронов на внешней оболочке (например, у фтора по сравнению с кислородом) не приводит к увеличению размеров атома. Наоборот, размеры атома фтора меньше, чем атома кислорода (рис. 4-8).
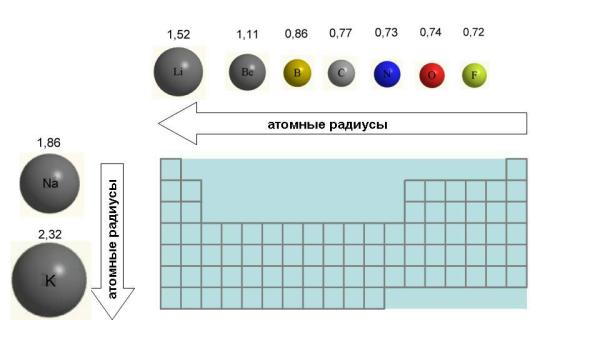
Рис. 4-8. Изменение атомных радиусов на примере элементов 2-го периода и 1-й группы Периодической таблицы. Атомные радиусы даны в ангстремах (1 А = 10-8 см).
7. При перемещении СВЕРХУ ВНИЗ АТОМНЫЕ РАДИУСЫ элементов РАСТУТ, потому что заполнено больше электронных оболочек.
г) Закономерности, связанные с валентностью элементов.
8. Элементы одной и той же подгруппы (в короткой форме таблицы) или группы (в длинной) имеют аналогичную конфигурацию внешних электронных оболочек и, следовательно, одинаковую валентность в соединениях с другими элементами.
9. s-Элементы имеют валентности, совпадающие с номером их группы (в любой форме таблицы).
10. p-Элементы имеют наибольшую возможную для них валентность, равную номеру группы в короткой форме Периодической таблицы. Кроме того, они могут иметь валентность, равную разности между числом 8 (октет) и номером их группы в короткой форме таблицы (этот номер совпадает с числом электронов на внешней оболочке).
11. d-Элементы обычно обнаруживают несколько разных валентностей, которые нельзя точно предсказать по номеру группы.
12. Не только элементы, но и многие их соединения - оксиды, гидриды, соединения с галогенами - обнаруживают периодичность. Для каждой ГРУППЫ элементов можно записать формулы соединений, которые периодически "повторяются" (то есть могут быть записаны в виде обобщенной формулы). Например:
|
LiCl |
BeO |
BCl3 |
H2O |
. HF |
|
NaCl |
MgO |
AlCl3 |
H2S |
... HCl |
|
KCl |
CaO |
GaCl3 |
H2Se |
... HBr |
|
. . . . . . |
. . . . . . |
. . . . . . |
. . . . . . |
. . . . |
Обобщенная формула |
RCl |
RO |
RCl3 |
H2R |
HR |
|
хлориды |
оксиды |
хлориды |
гидриды |
гидриды |
11)
Теория химической связи занимает важнейшее место в современной химии. Она объясняет, почему атомы объединяются в химические частицы, и позволяет сравнивать устойчивость этих частиц. Используя теорию химической связи, можно предсказать состав и строение различных соединений. Понятие о разрыве одних химических связей и образовании других лежит в основе современных представлений о превращениях веществ в ходе химических реакций.
Химическая связь - это взаимодействие атомов, обусловливающее устойчивость химической частицы или кристалла как целого. Химическая связь образуется за счет электростатического взаимодействия между заряженными частицами: катионами и анионами, ядрами и электронами. При сближении атомов начинают действовать силы притяжения между ядром одного атома и электронами другого, а также силы отталкивания между ядрами и между электронами. На некотором расстоянии эти силы уравновешивают друг друга, и образуется устойчивая химическая частица.
При образовании химической связи может произойти существенное перераспределение электронной плотности атомов в соединении по сравнению со свободными атомами. В предельном случае это приводит к образованию заряженных частиц - ионов (от греческого "ион" - идущий).
