
- •Понятие об идеальном газе. Основные законы идеальных газов
- •Стационарный одномерный поток
- •44. Опишіть та охарактеризуйте теплопровідність.
- •45. Опишіть та охарактеризуйте політропні процеси.
- •46. Наведіть аналітичний вираз роботи адіабатного процесу. Проаналізуйте даний процес.
- •Адиабатный процесс
- •47. Опишіть та охарактеризуйте термодинамічний процес.
- •48. Ts діаграма водяної пари. Проаналізуйте її фізичний зміст.
- •49. Відношення теплоємності. Проаналізуйте їх фізичний зміст.
- •50. Опишіть та охарактеризуйте основні параметри нагрітої пари.
45. Опишіть та охарактеризуйте політропні процеси.
Політрóпний
процéс — термодинамічний
процес, під
час якого питома теплоємність ![]() з газу залишається
незмінною. Величина
з газу залишається
незмінною. Величина
![]()
називається показником політропи. Окремими явищами політропного процесу є ізопроцеси і адіабатний процес.
![]()
Це рівняння називається рівнянням політропного процесу.
Политропный процесс характеризуется одной и той же долей количества подводимой теплоты, расходуемой на изменение внутренней энергии системы. [1]
Политропные процессы позволяют исследовать многообразные явления, протекающие в тепловых машинах. [2]
Политропный процесс характеризуется постоянным показателем п политропы. В произвольном же термодинамическом обобщенном процессе показатель политропы является переменной величиной. С этой целью воспользуемся методом, поясненным на рис. 12 в для совершенного и реального газов. [3]
Политропный процесс в s - - Т - диаграмме изображается наклонной линией, направление которой зависит от показателя политропы. [4]
Политропные процессы при 1 п k имеют различные знаки изменения температуры и теплоты. Это значит, что если в таком процессе расширения к газу подводится теплота, то температура его понижается, так как совершаемая газом работа больше подводимой теплоты и на совершение работы затрачивается часть внутренней энергии. Для аналогичного процесса сжатия, наоборот, если работа сжатия больше отводимой теплоты, то температура тела повышается. Политропные процессы этой группы при 1 п k происходят при отрицательной теплоемкости рабочего тела. Так как теплоемкость с dq / dT, то при различных знаках dq и dT теплоемкость процесса отрицательна. [5]
Политропный процесс является наиболее общим, другие ( изо-хорный, изобарный, изотермический, адиабатный) есть его частные случаи.
Время расширения воздуха в двигателях весьма мало, и практически теплоотдача стенок на процесс не оказывает влияния. [7]
Политропный процесс - процесс, удовлетворяющий уравнению pv const, где под п подразумевают произвольное, но для данного процесса постоянное число. [8]
Политропный процесс является обобщаю-щим процессом, протекающим при самых разнообразных условиях. [9]
Иногда политропный процесс задается зависимостью р f ( и), и возникает необходимость определения показателя политропы. [10]
Политропным процессом называется такой термодинамический процесс изменения состояния физической системы, при котором в течение всего процесса сохраняется постоянство теплоемкости. [11]
Политропным процессом, представляющим значительный практический интерес, является процесс i const, называемый дросселированием и наблюдаемый во всех случаях движения пара при наличии трения без совершения полезной работы. [12]
46. Наведіть аналітичний вираз роботи адіабатного процесу. Проаналізуйте даний процес.
Адиабатный процесс
Адиабатный процесс — процесс, при котором отсутствует теплообмен между системой и окружающей средой.
И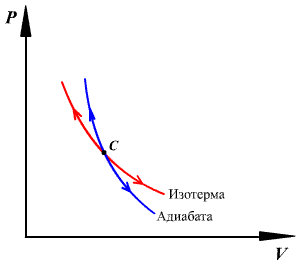 з
первого начала термодинамики следует,
что работа газа при адиабатном процессе
совершается за счет его внутренней
энергии:
з
первого начала термодинамики следует,
что работа газа при адиабатном процессе
совершается за счет его внутренней
энергии:
![]() (1).
С
другой стороны, из уравнения
Клапейрона-Менделеева следует:
(1).
С
другой стороны, из уравнения
Клапейрона-Менделеева следует:
![]() (2).
Разделим
уравнение (2) на уравнение (1):
(2).
Разделим
уравнение (2) на уравнение (1):
![]() ,
где
,
где
![]() .
Проинтегрируем
полученное уравнение:
.
Проинтегрируем
полученное уравнение:
![]() .
Таким
образом, при адиабатном процессе
.
Таким
образом, при адиабатном процессе
![]() или
или ![]() —
уравнение Пуассона.
С учетом уравнения
Клапейрона-Менделеева (
—
уравнение Пуассона.
С учетом уравнения
Клапейрона-Менделеева (![]() ,
,![]() )
уравнение
Пуассона может быть представлено в
виде:
)
уравнение
Пуассона может быть представлено в
виде:
![]() или
или ![]()
![]() или
или ![]() .
.
График адиабатного
процесса — более крутая кривая, чем
гипербола при изотермическом процессе.
Это следует из выражения производной ![]() ,
полученной из уравнения Пуассона.
,
полученной из уравнения Пуассона.
Работа газа при адиабатном
процессе равна убыли внутренней
энергии:
![]() .
.
Из анализа, приведенного в [55], следует, что существующие аналитические зависимости описываютадиабатный процесс расширения ( сжатия) влажного пара, состояние которого в любой момент времени является равновесным. В этой же работе показано, что во многих интересующих практику случаях такое рассмотрение процесса не отвечает физической реальности и, в частности, в таких процессах, как истечение вскипающих потоков жидкости, высоковлажного пара, и процессах распространения возмущений в двухфазной пароводяной смеси.
