
- •Министерство образования республики беларусь белоруский государственный университет
- •Противоопухолевые комплексы платины
- •Оглавление
- •Введение
- •История
- •Механизмы действия противоопухолевых комплексов платины (II, IV)
- •Гипотеза Розенберга
- •Гипотеза биопроцессов
- •Основной механизм комплексов Pt(II)
- •Особенности структур противоопухолевых комплексов платины (II, IV) и основные принципы их дизайна
- •Особенности структуры комплексов
- •Комплексы платины (IV)
- •Механизм устойчивости к противоопухолевым препаратам на основе комплексов платины (II, IV).
- •Стерически затрудненные комплексы платины (II. IV).
- •Tpанc-комплексы платины (II).
- •Комплексы платины (II, IV) с производными 1,2-диаминоциклогексана
- •Модифицирование лабильных групп комплекса.
- •Полинуклеарные комплексы платины (II)
- •Водорастворимые комплексы платины (II. IV)
- •Заключение Список используемой литературы:
Tpанc-комплексы платины (II).
При сопоставлении активности цис- и трансплатина и их аналогов довольно длительное время использовалось эмпирическое соотношение структура-активность, согласно которому транс-комплексы платины (II) неактивны [25, 134, 136-141]. Однако было показано, что некоторые транс-соединении активны in vitro и in vivo [21]. Экспериментальные данные, которые не соответствовали общепринятому утверждению о том, что наличие двух уходящих групп из цис-положения - необходимое условие для противоопухолевой активности комплексов платины (II), стали все чаще появляться с конца 1990-х гг. Эти “исключения”, которые нередко обладают активностью в отношении устойчивых к цисплатину опухолевых клеток, можно разделить на 4 группы:
1) транс-[Pt(L)(L')CI2], где L и/или L' - пиридиноподобные лиганды [142-146];
2) комплексы платины (IV) с общей формулой транс- [Pt(L)(L')CI2X2], где X - гидроксильные или карбоксилатные лиганды, L - аммин, L' - амин [138, 147];
3) транс-[Pt(L)(L’)CI2], где L - алкилзамещенный амин, L' - изопропиламин [56, 148];
4) транс-[Pt(L)(L’)CI2], где L и/или L' - иминоэфирные лиганды [29, 139, 149].
Ниже дана сравнительная характеристика основных особенностей комплексообразования противоопухолевых транс-комплексов платины (II, IV) и их цис-изомеров.
Синтез трансплатина осуществлялся одновременно с синтезом цисплатина [150]. Трансплатин был получен путем термического разложения хлорида тетрааммиаката платины (II):
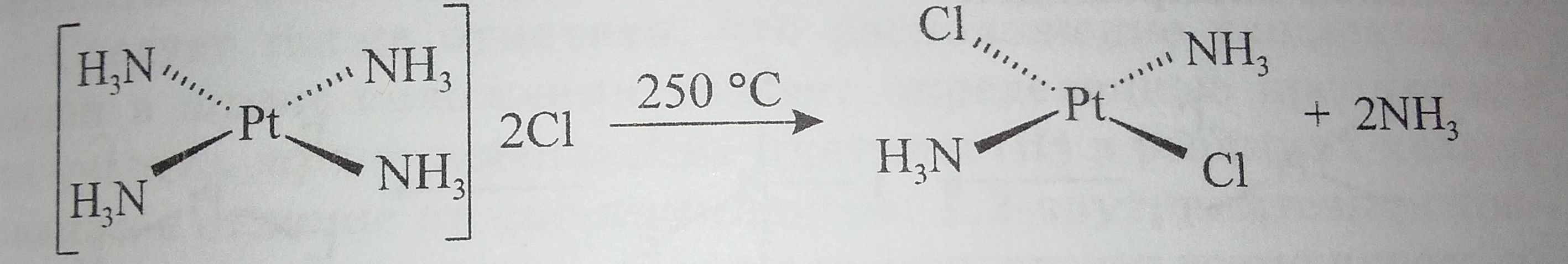
Выход был достаточно низкий за счет интенсивного разложения до Pt(0), но он мог быть увеличен благодаря проведению разложения при 190-195 °C и пониженном давлении [151].
Вторая и наиболее общая процедура синтеза трансплатина заключается а действии НСI водный раствор [Pt(NH3)4CI2] [152-153].
Получение производных тиомоченины Курнакова [831] используется для установлеиия различия между двумя изомерами:
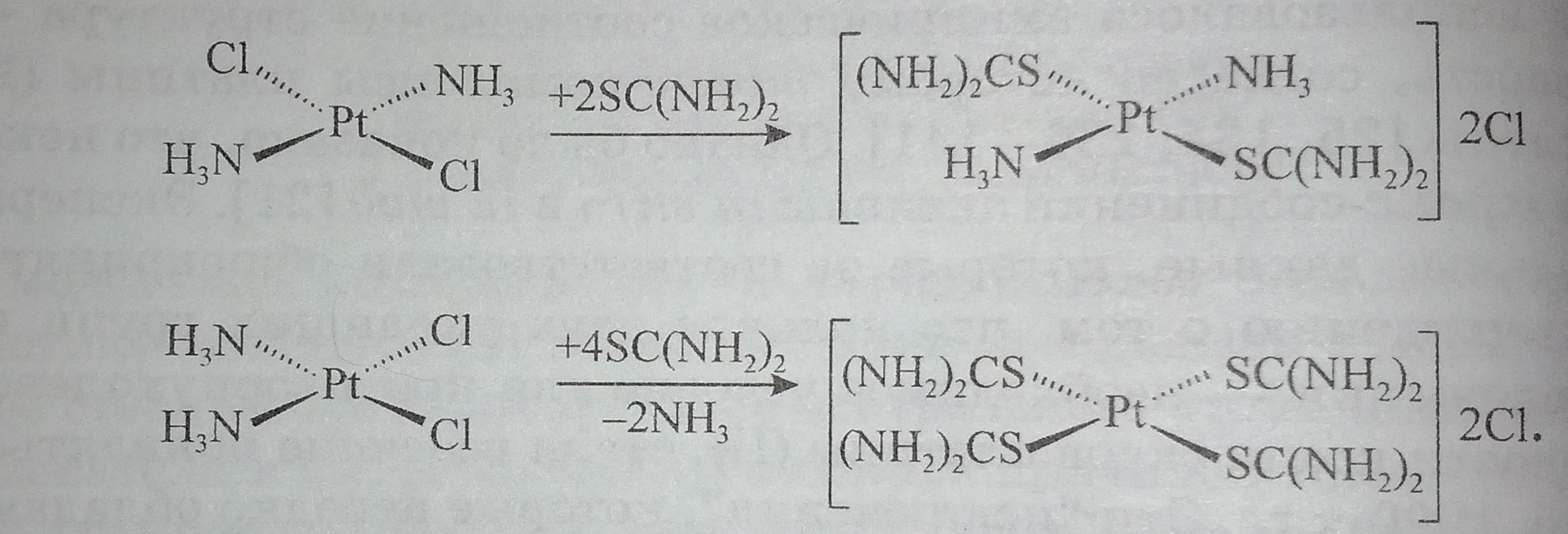
В случае цисплатина реакция приводит к полному замещению лигандов, в случае же трансплатина замещаются только хлоридные лиганды. Результат теста Курнакова может привести к неверному заключению о том, что аммин-лиганды сильнее связаны с транс-, чем в цис-комплексе, но это не так. С использованием 15N-ЯMP показано, что прочность этого связывания выше в цис-изомере, чем в транс-изомере [154]. Кроме того, обмен протонов аммин-лиганда осуществляется быстрее в цис-, чем транс-изомере, что свидетельствует о большей кислотности этой группы. По-видимому, в тесте Курнакова удаление аммин-лиганда из цис-изомера энергетически выгоднее, чем из транс-изомера [21].
На основании сравнения рассмотренных выше свойств транс- и цис-комплексов платины (II) можно сделать несколько общих выводов [21]: транс-комплексы должны реагировать быстрее с нуклеофилами только в двух определенных формах (дихлоро- и хлоро-аква); моноаддукты транскомплексов с ДНК в отличие от аддуктов цис-комплексов, будут легко удаляться при действии транс-лабилизирующих нуклеофилов, таких как тиомочевина и глутатион:
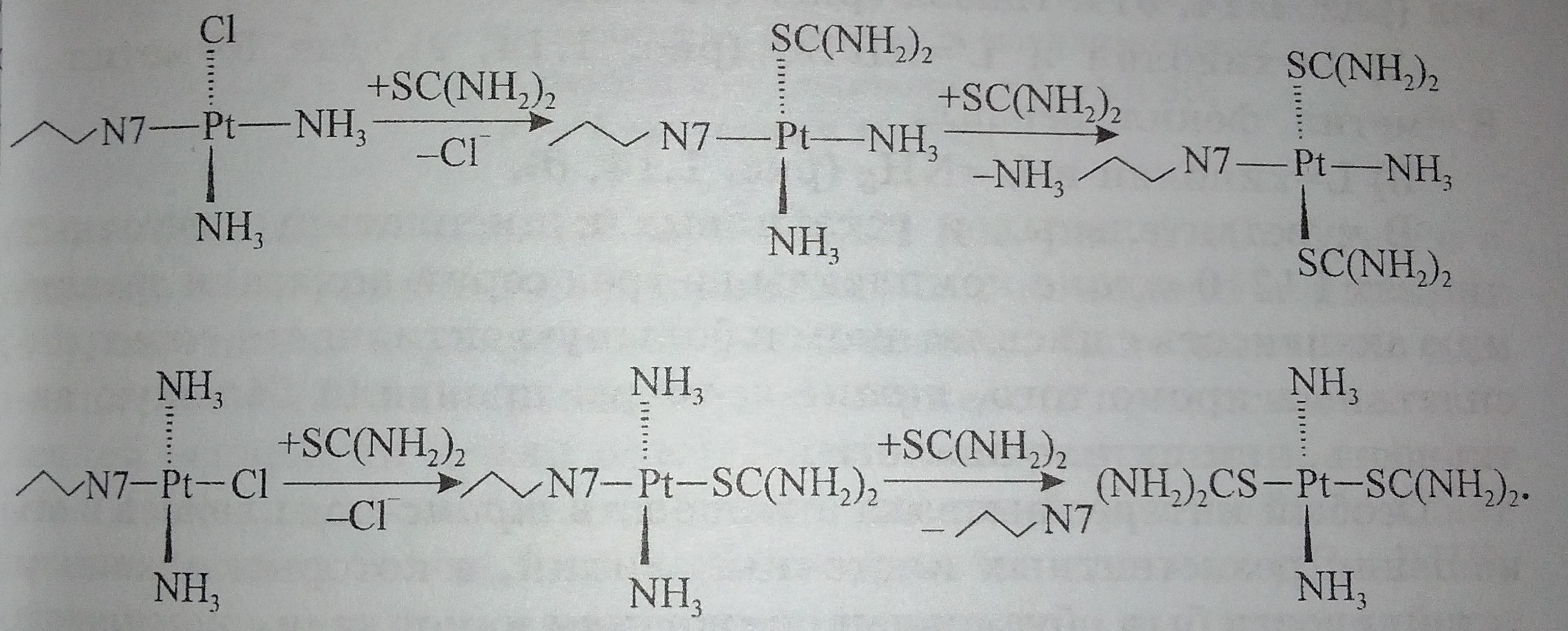
Таким образом, репарация моноаддуктов трансплатина может протекать химическим путем, тогда как для моноаддуктов цисплатина может потребоваться участие энзимов.
Следует также отметить, что расположение уходящих лигандов в транс-положении создает определенные препятствия для участия транс-комплексов платины (II) в реакциях хелатирования в отличие от цис-комплексов: 1,2-внутринитевые сшивки полностью запрещены, тогда как существует возможность образования 1,3-внутринитевых сшивок.
Причиной активности некоторых транс-соединений нередко считают изомеризацию в активную цис-форму. Однако такое предположение не всегда оправдано, поскольку, как следует из рассмотренных ниже примеров, цис-изомер может быть менее активным, чем соответствующий транс-изомер. Различие между цисплатином и трансплатином заключается в том, что трансплатин кинетически более реакционоспособен, чем цисплатин и более подвержен дезактивации [33, 156].
Тщательное моделирование с использованием лиганда, создающего стерическое препятствие, может уменьшить реакционую способность транс-комплексов платины (II) [33]. Поскольку; транс-изомер образует аддукты платина (II)-ДНК, отличные oт аналогов цисплатина, можно надеяться, что транс-комплексы смогут преодолеть устойчивость определенных опухолей к цисплатину [21, 156, 157].
Было проведено сравнительное исследование цитотоксичности трех серий транс-комплексов с общей формулой [Pt(L)(L')CI2] [25, 134, 142, 143]:
L=L', где L и L' - пиридин (рис. 6, а), N-метилимидазол (рис. 6, б) и тиазол (рис. 6, в);
L=хинолин и L'=RR'SO (рис. 6, г), где R=метил и К'=метил, фенил, бензил;
L=хинолин и L'=NH3 (рис. 6, д).
В чувствительных и устойчивых к цисплатину клеточных линиях L1210 транс-комплексы из трех серий показали сравнимую активность с цисплатином и большую активность, чем трансплатин, а кроме того, транс-изомеры проявили большую активность, чем их цис-аналоги.
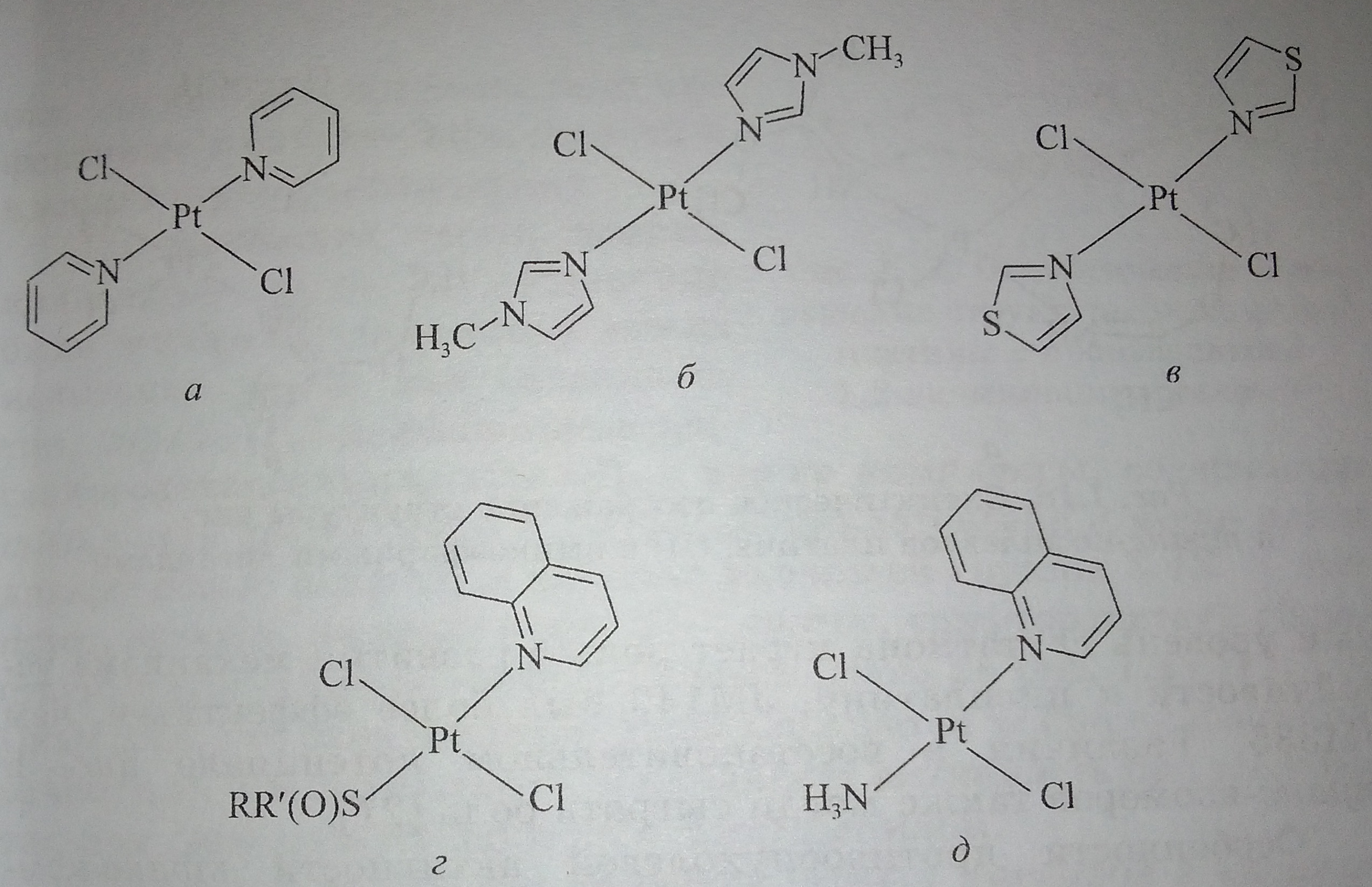
Рис 6. Схематическое изображение структуры транс-комплексов платины (II) с общей формулой [PtCI2(L)(Lʹ)]: а - L и L' – пиридин; б - L и L' - N-метилимидазол; в - L и L' – тиазол; г - L=хинолин и L'=RR'SO; д - L=хинолин и L'=NH3.
Особый интерес вызвала активность транс-комплексов в отношении резистентных клеточных линий, в которых механизм устойчивости был обусловлен снижением накопления комплекса платины (II), ее интенсивным удалением и/или повышенной толерантностью к аддуктам платина (II)-ДНК [134].
Большую активность, чем трансплатин, а также соответствующий цис-аналог JM149 (рис. 7, б), проявляет в отношении клеточных линий карциномы яичников комплекс JM335. транс, транс, транс-аммин(циклогексиламин)дихлородигид роксоплатина (IV) (рис. 7, а) [138].
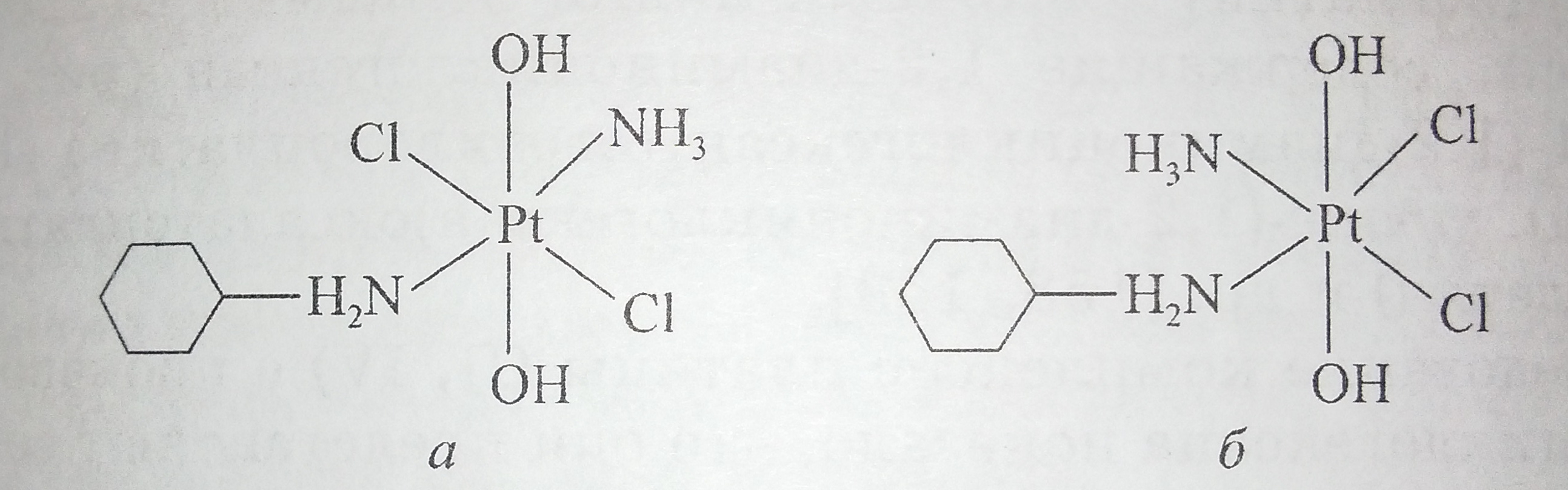
Рис. 7. Схематическое изображение структуры цис- и транс-комплексов платины (IV): а – JM335; б – JM149.
Отсутствие перекрестной устойчивости наблюдалось в тех образцах, где она была связана с пониженным накоплением комплекса платины (II). Это согласуется с результатами, полученными при исследовании рассмотренных выше соединений платины (IV) JМ216 и JM221. Однако в отличие от аммин/аминосодержащих цис-комплексов платины (IV), отсутствие перекрестной устойчивости было выявлено для комплекса JM335 в клетках, где устойчивость приписывали усиленной репарации и/или повышенной толерантности к платина (II)-ДНК аддуктам. Данный факт лишний раз подтверждает предположение о том, что особые аддукты платина (II)-ДНК, образуемые транс-комплексами, позволяют им преодолевать устойчивость опухолей к цисплатину. В клетках, где повышенный уровень глутатиона играет роль в развитии механизма устойчивости к цисплатину, JM149 был более эффективен, чем JM335. Различия в восстановительном потенциале цис- и транс-изомеров также могли сыграть роль [21].
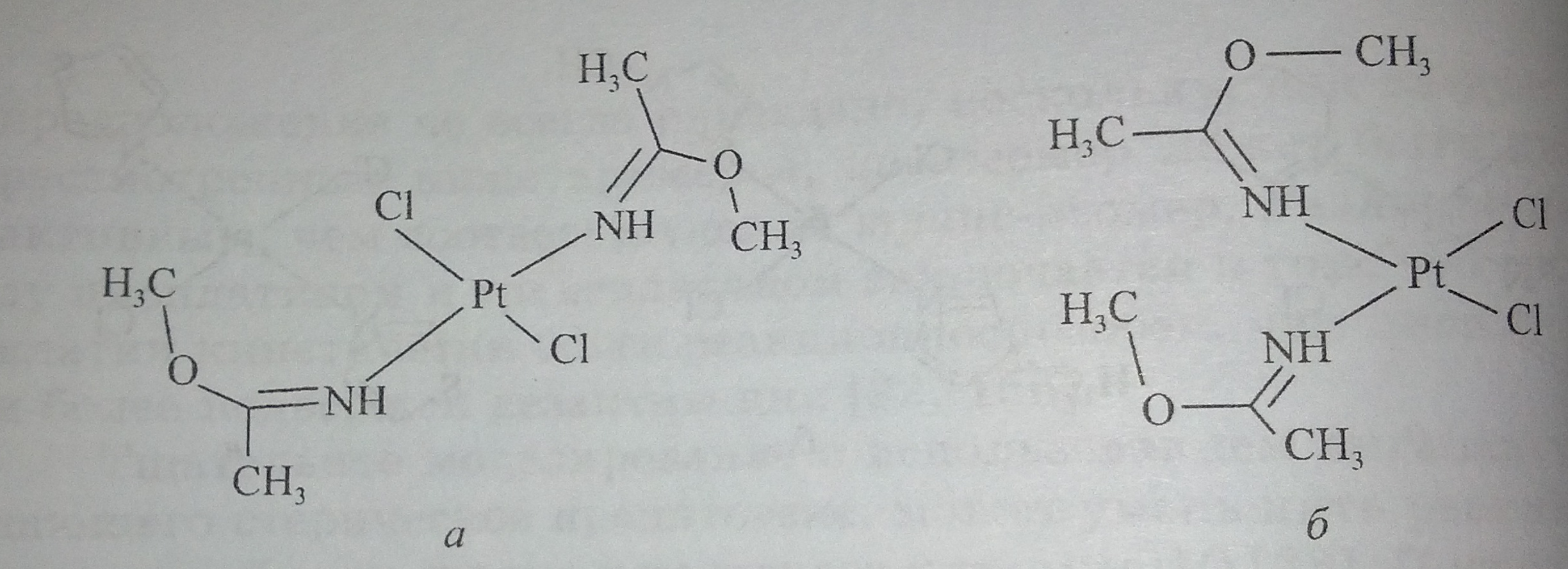
Рис. 8. Схематическое изображение структуры цис- и транс- комплексов платины (II) с иминоэфирными лигандами
Особенности противоопухолевой активности комплексов исследовались для комплексов платины (II) с имино-эфирными лигандами [25, 139]. Взаимодействие этих комплексов с ДНК (как цис-, так и транс-изомеров) осуществлялось значительно медленнее, чем в случае цисплатина и трансплатина. Это связывают с большими стерическими затруднениями, создаваемыми иминоэфирными лигандами. В отношении клеточных линий лейкемии транс-изомер (рис. 8, а) проявил большую противоопухолевую активность, чем цис-соединение (рис. 8, б). Против приобретенной устойчивости клеточных линий лейкемии к цисплатину транс-изомер проявил активность in vivo, то время как цис-аналог оказался неактивным [25].
