- •8. Концентрирование азотной кислоты
- •Температура кипения водных растворов азотной кислоты
- •8.1. Концентрирование азотной кислоты при помощи водоотнимающих веществ
- •8.1.1. Концентрирование азотной кислоты с помощью серной кислоты
- •8.1.2. Теоретические основы процесса
- •8.1.3. Технологическая схема концентрирования азотной кислоты с помощью серной кислоты
- •8.1.4. Технологический режим процесса концентрирования азотной кислоты с помощью серной кислоты
- •Основная аппаратура отделения концентрирования
- •Факторы, влияющие на работу концентрационной колонны
- •8.2. Концентрирование азотной кислоты с применением нитрата магния
- •8.2.1. Физико-химические основы процесса концентрирования азотной кислоты с применением нитрата магния
- •8.2.2. Технологическая схема концентрирования азотной кислоты с применением нитрата магния
- •9. Прямой синтез концентрированной азотной кислоты
- •9.1. Физико-химические основы процесса
- •9.2. Выделение избыточной реакционной воды
- •9.3. Окисление оксида азота II
- •9.4. Абсорбция оксидов азота концентрированной азотной кислотой
- •9.5. Выделение оксидов азота
8.1.3. Технологическая схема концентрирования азотной кислоты с помощью серной кислоты
Наибольшее распространение получила схема, приведенная на рис. 33.
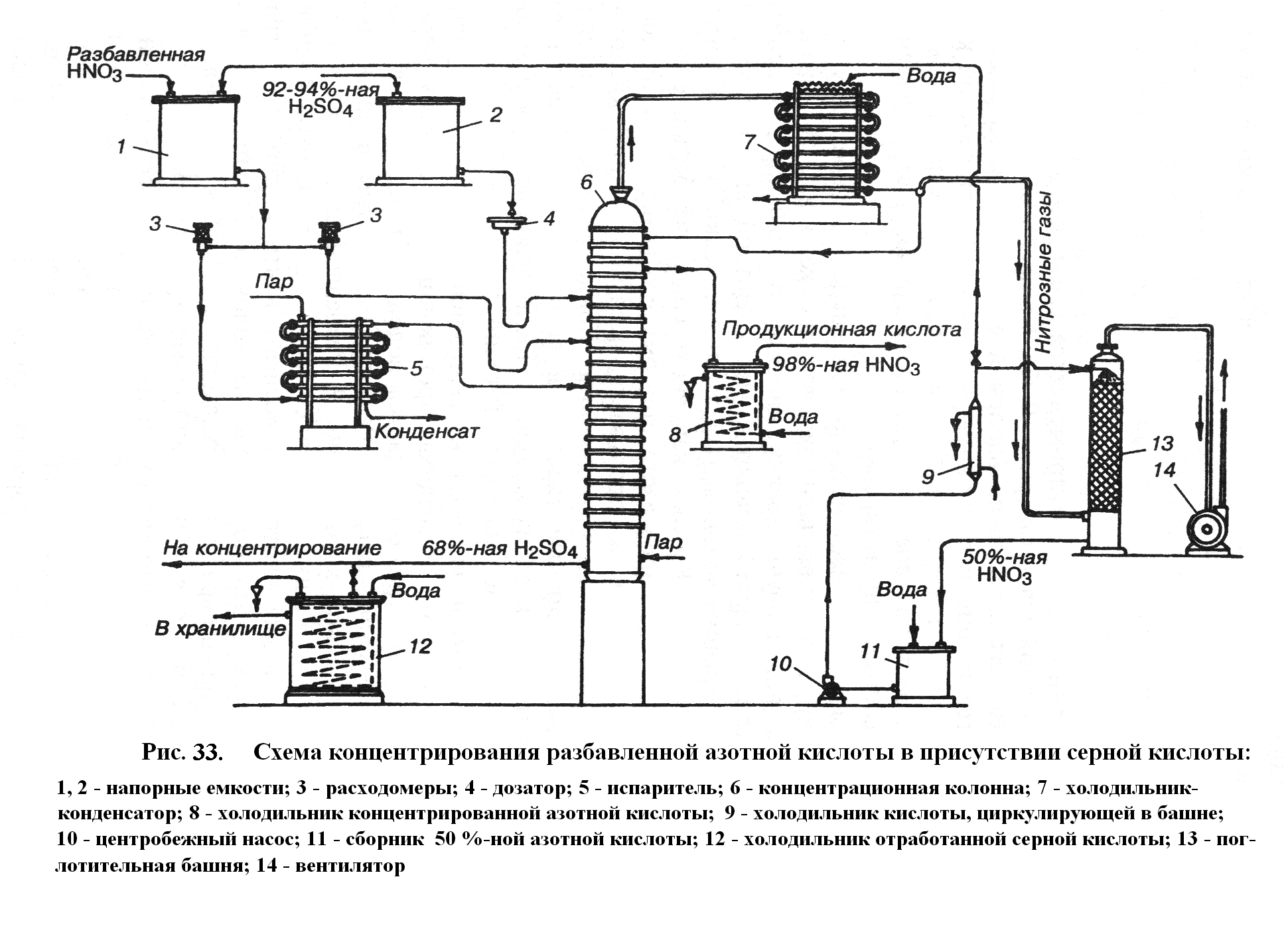
Процесс концентрирования НNO3 ведут в колоннах 6, изготовленных из ферросилида. Необходимое тепло подводится с острым паром (Т=250 С, р=0,15 МПа). Для снижения расхода пара азотную кислоту перед входом в колонну подогревают в испарителе 5, также изготовленном из ферросилидовых труб.
Выходящие из колонны пары НNO3 с температурой 70–85 С содержат до 2 % водяного пара. Пары Н2О и НNO3 конденсируются в холодильнике-конденсаторе 7. В парах содержится некоторое количество растворенных оксидов азота и поэтому конденсат возвращают на верхнюю тарелку колонны 6 для отдувки NOx парами азотной кислоты, идущими вверх, в конденсатор. Пройдя (вниз) две отбелочные (т.е. удаляющие NOx) тарелки НNO3, свободная от оксидов азота, выводится из колонны, охлаждается до 35–40 С в холодильнике 12 и поступает на склад.
Несконденсировавшиеся пары НNO3, оксиды азота и инертные газы направляются в абсорбционную башню 13, орошаемую водой, где образуется 40–45 % (иногда до 50 %) мас. НNO3, которая отправляется на концентрирование, а часть на циркуляцию в абсорбционную башню. Газы после башни выбрасываются в атмосферу.
8.1.4. Технологический режим процесса концентрирования азотной кислоты с помощью серной кислоты
Температура паров НNO3, С: на выходе из колонны на выходе из конденсатора
Остаточное давление в верхней части колонны, мм рт. ст.
|
70–85 30–45
20–50 |
Температура отработанной Н2SO4 на выходе из колонны, С
|
150–170
|
Концентрация отработанной Н2SO4, % мас. |
65–70 |
|
|
Давление пара, поступающего в испаритель, МПа |
0,4–0,6 |
|
|
Основная аппаратура отделения концентрирования
азотной кислоты с помощью серной кислоты.
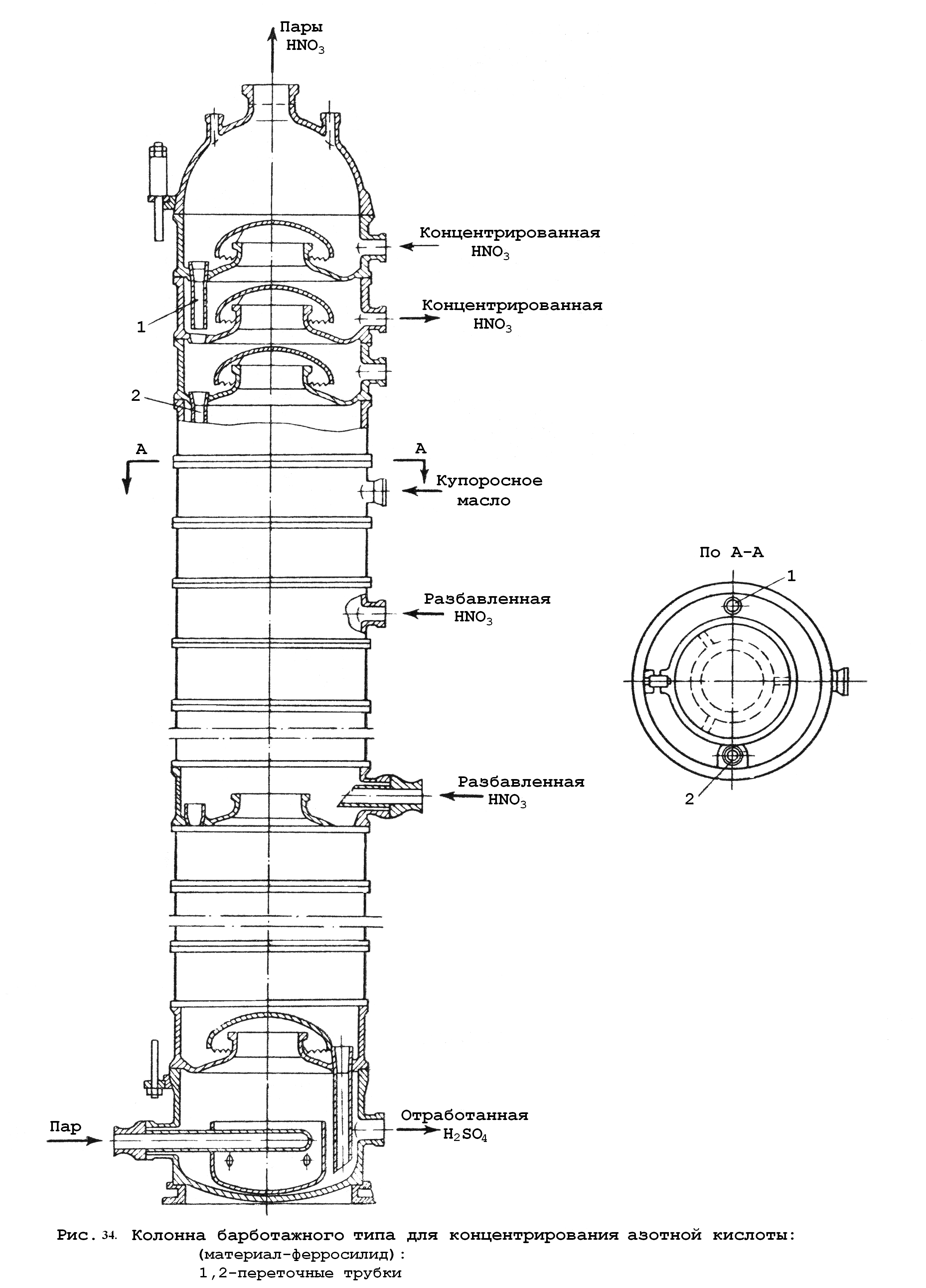
Концентрационная колонна. Колонна барботажного типа (рис. 34) с одним зубчатым колпачком на тарелке состоит из 18–25 царг высотой 360 мм. D=850–1000 мм (толщина стенок 25 мм); суммарная высота 22-х царг составляет 9600 мм. Нижняя и верхняя царги имеют Н=760 мм (цель – сепарация).
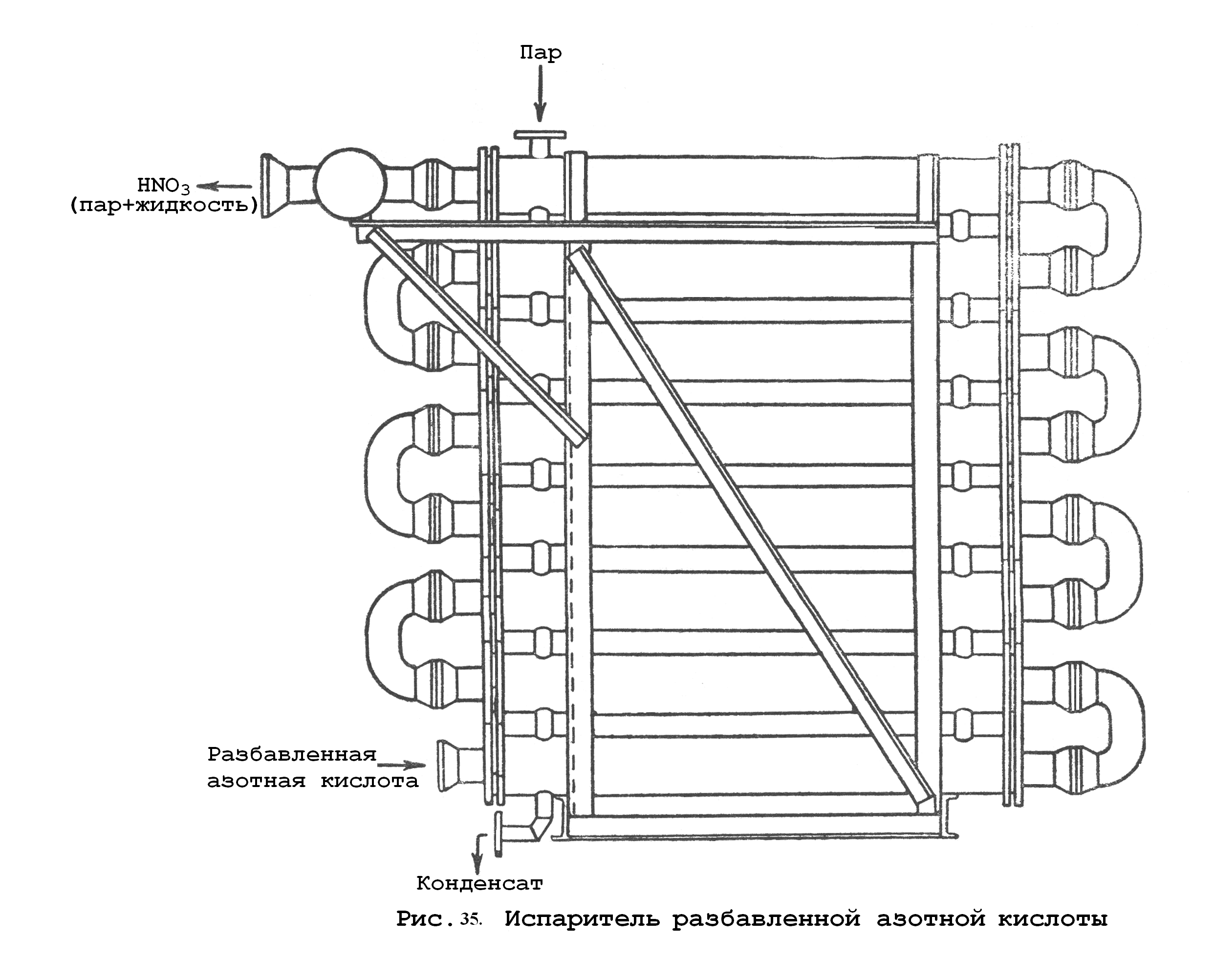
Испаритель. Тип «Труба в трубе» (рис. 35). Внутренние трубы выполнены из ферросилида (d=80 мм; l=2000 мм). Наружные трубы – углеродистая сталь (d=165 мм). На одну колонну необходимо 11,5–13,0 м2 поверхности теплообмена. Для уменьшения потерь тепла, трубы испарителя теплоизолируются совелитом.
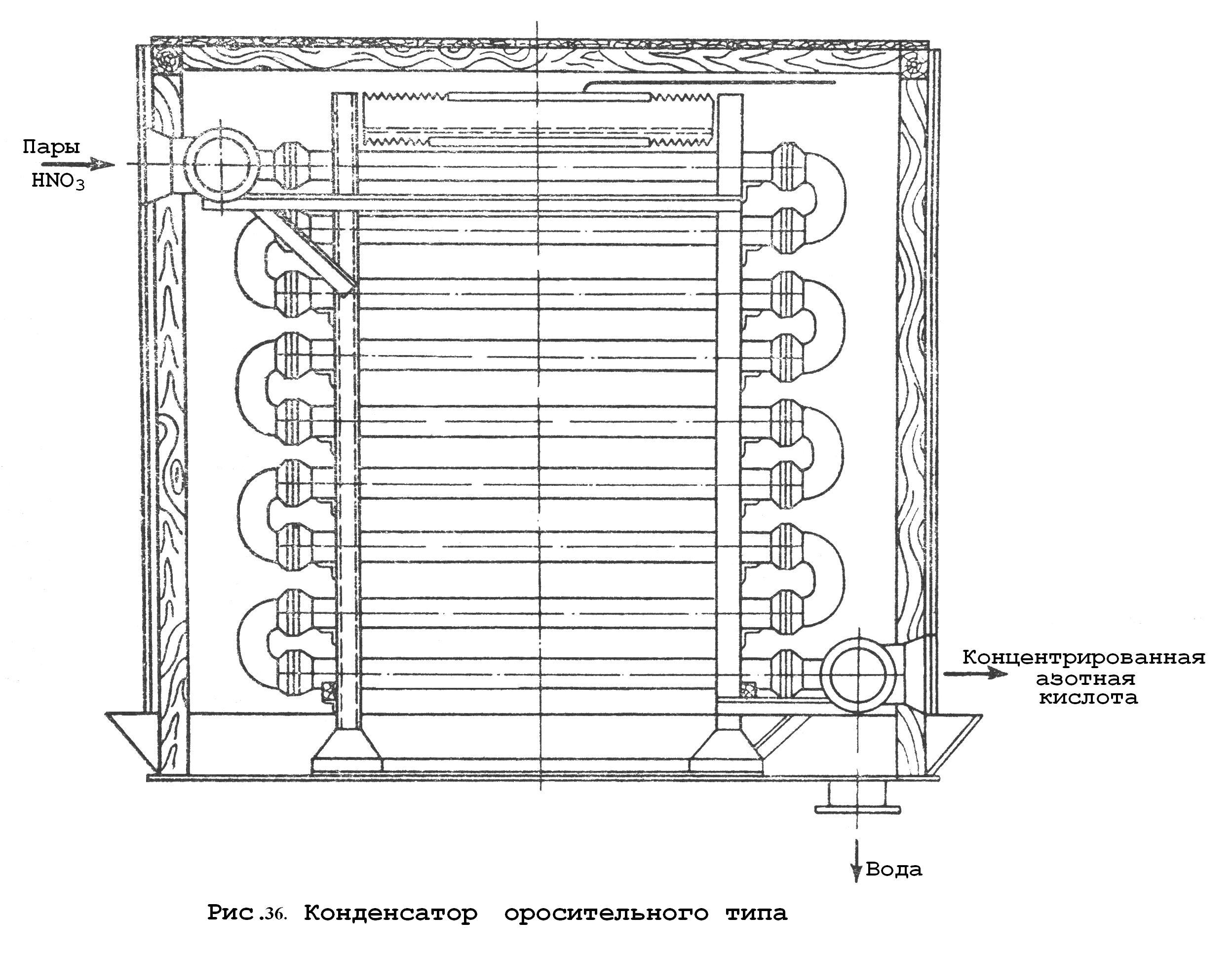
Холодильник-конденсатор оросительного типа (рис. 36) выполнен из ферросилидовых труб (d=100×12 мм; l=2000 мм).
Пары направляются в верхний коллектор, из нижнего коллектора выходит концентрированная азотная кислота.
Самостоятельно: рассмотреть процесс концентрирования Н2SO4.