
- •Лекция 1. Особенности атомно-кристаллического строения металлов.
- •1. Кристаллическое строение металлов
- •2. Полиморфные и магнитные превращения в металлах
- •Лекция 2. Строение реальных металлов. Дефекты кристаллического строения
- •Лекция 3. Кристаллизация металлов
- •Законы кристаллизации
- •Строение металлического слитка
- •Методы исследования металлов
- •Определение химического состава.
- •Изучение структуры.
- •Физические методы исследования
- •Лекция 4. Общая теория сплавов. Строение, кристаллизация и свойства сплавов. Диаграмма состояния. Строение металлических сплавов
- •Контрольная работа № 1 до этой темы Кристаллизация сплавов
- •Понятие о диаграммах состояния сплавов
- •Количественный структурно-фазовый анализ сплава
- •Лекция 5. Диаграммы состояния двухкомпонентных сплавов
- •5.1 Диаграмма состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии (сплавы твердые растворы с неограниченной растворимостью)
- •5.2 Диаграмма состояния сплавов с отсутствием растворимости компонентов в твердом состоянии (механические смеси)
- •5.3 Диаграмма состояния сплавов с ограниченной растворимостью компонентов в твердом состоянии
- •5.4 Диаграмма состояния сплавов, компоненты которых образуют химические соединения
- •5.5 Диаграмма состояния сплавов, испытывающих фазовые превращения в твердом состоянии (переменная растворимость)
- •Связь между свойствами сплавов и типом диаграммы состояния (закон Курнакова)
- •Железоуглеродистые сплавы
- •Компоненты и фазы в сплавах железа с углеродом
- •Диаграмма состояния железо-цементит
- •Сплавы системы железо-углерод и их структура
- •1) С содержанием углерода менее 0,02% (точка р)- техническое железо.
- •2) Содержащие 0,02…2,14 % углерода - углеродистые стали.
- •3) Сплавы, содержащие углерода более 2,14 % (до 6,67 %), заканчивающие кристаллизацию образованием эвтектики (ледебурита), называют чугунами.
- •Превращения, протекающие при охлаждении сплавов
- •Стали. Влияние углерода и примесей на свойства сталей
- •Назначение легирующих элементов.
- •Распределение легирующих элементов в стали.
- •Классификация и маркировка сталей Классификация сталей
- •По химическому: составу: углеродистые и легированные.
- •По содержанию углерода:
- •По способу выплавки:
- •По назначению:
- •Маркировка сталей
- •Качественные углеродистые стали
- •Качественные и высококачественные легированные стали
- •Легированные конструкционные стали
- •Легированные инструментальные стали
- •Быстрорежущие инструментальные стали
- •Шарикоподшипниковые стали
- •Автоматные стали
- •Строение, свойства, классификация и маркировка серых чугунов
- •Технология термической обработки стали
- •1. Отжиг
- •2. Нормализация
- •3. Закалка
- •Способы закалки
- •Дефекты закалки
- •4. Отпуск
- •5. Старение
- •6. Обработка холодом
Количественный структурно-фазовый анализ сплава
Пользуясь диаграммой состояния можно для любого сплава при любой температуре определить не только число фаз, но и их состав и количественное соотношение. Для этого используется правило отрезков.
Для проведения количественного структурно-фазового анализа через заданную точку проводят горизонталь (коноду) до пересечения с ближайшими линиями диаграммы ограничивающими данную двухфазную область (ликвидус, солидус или оси компонентов).
Правило отрезков может быть использовано только для тех областей диаграммы, в которых сплавы находятся в двухфазном состоянии.
Первое положение правила отрезков — определение состава фаз.
Необходимо определить состав фаз для сплава в точке m:
Через точку m проводим горизонтальную линию (коноду) до пересечения с ближайшими линиями диаграммы - это линии ликвидус и солидус.
Точки пересечения с и d проецируют на ось концентраций.
Проекция точки с – точка с' покажет состав твердой β-фазы (твердая фаза содержит ≈11%В и 89%А).
Проекция точки d – точка d ' покажет состав жидкой фазы (жидкая фаза содержит ≈ 44%В и 56%А).
Состав жидкой фазы изменяется по линии ликвидуса, а состав твердой фазы – по линии солидуса.
С понижением температуры состав фаз изменяется в сторону увеличения содержания компонента В.
Пользуясь вторым положением правила отрезков, можно определить количественное соотношение фаз также для любой температуры
Необходимо определить количественное соотношения жидкой и твердой фазы при заданной температуре (в точке m):
Количественная масса фаз обратно пропорциональна отрезкам проведенной коноды.
Количество всего сплава (Qсп) определяется отрезком cd.
Если принять, что отрезок cd выражает количество (Qсп) всего сплава, то
- количеству выделившихся кристаллов β-твердого раствора (Qтв) соответствует отрезок md,
- количеству жидкой фазы (Qж) - отрезок cm.
Для определения относительного количества фаз пользуются отношениями:
- относительное количество твердой
фазы![]() ;
;
- относительное количество жидкой фазы
![]() .
.
Лекция 5. Диаграммы состояния двухкомпонентных сплавов
5.1 Диаграмма состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии (сплавы твердые растворы с неограниченной растворимостью)
Полная взаимная растворимость металлов в твердом состоянии возможна лишь для изоморфных металлов. При их сплавлении образуется непрерывный ряд твердых растворов замещения (Cu-Ni).

Рис.5.1 Диаграмма состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии (а); кривые охлаждения типичных сплавов (б)
Анализ диаграммы
1. Количество компонентов: К = 2 (компоненты А и В).
2. Число фаз: Ф = 2 (жидкая фаза Ж, кристаллы твердого раствора α)
3. Основные линии диаграммы:
C1D – линия ликвидус, выше этой линии сплавы находятся в жидком состоянии;
C2D – линия солидус, ниже этой линии сплавы находятся в твердом состоянии.
4. Характерные сплавы системы:
а) Чистые компоненты А и В кристаллизуются при постоянной температуре (кривые охлаждения сплавов I и II).
Кривая I (рис. 53) получена при охлаждении компонента А. Выше температуры 1 металл находится в жидком состоянии. Кристаллизация начинается при температуре в точке 1 и заканчивается через какое-то определенное время, зависящее от количества металла в тигле, в точке 1'.
Согласно правилу фаз С = К - Ф + 1 имеем: компонент 1 (металл А) фазы 2 (жидкий металл и образующиеся кристаллы А), следовательно, С = 1-2+1=0, т. е. кристаллизация должна происходить при постоянной температуре. Ниже температуры 1ʹ происходит только охлаждение кристаллов компонента А. Аналогично происходит охлаждение и кристаллизация компонента В (сплав III).
б) Остальные сплавы кристаллизуются аналогично сплаву II.
Процесс кристаллизации сплава I:
- При температурах выше т. 1 сплав находится в состоянии однородного жидкого раствора.
- При температуре, соответствующей т. 1, жидкий раствор становится насыщенным по отношению к α-фазе, начинают образовываться центры кристаллизации твердого раствора α. На кривой охлаждения отмечается перегиб (критическая точка 1), связанный с уменьшением скорости охлаждения затвердевающего сплава вследствие выделения скрытой теплоты кристаллизации.
- В интервале температур т.1–2 продолжается процесс кристаллизации, протекающий при понижающейся температуре. Согласно правилу фаз число степеней свободы С = 2-2+1=1 т.к. К=2, Ф=2 (жидкая и кристаллы твердого раствора α), поэтому кристаллизация сплавов должна происходить в интервале температур.
- При достижении температуры соответствующей т. 2, кристаллизация заканчивается и ниже этой температуры охлаждается насыщенный твердый раствор α без каких-либо превращений.
- При дальнейшем понижении температуры охлаждается сплав в твердом состоянии, состоящий из однородных кристаллов твердого раствора α.
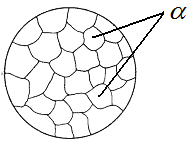 Рис. 5.2. Схема
микроструктуры сплава – однородного
α -твердого
раствора
Рис. 5.2. Схема
микроструктуры сплава – однородного
α -твердого
раствора
