
- •1.Классификация методов очистки атмосферного воздуха от промышленных загрязнений. Показатели, используемые для санитарной оценки воздушной среды.
- •2. Очистка газов от аэрозолей в сухих механических аппаратах. Очистка газов в сухих механических пылеуловителях.
- •3. Очистка газов от аэрозолей в мокрых пылеуловителях и в электрофильтрах.
- •4. Абсорбционные методы очистки газов от диоксида серы: нерекуперативные и рекуперативные методы.
- •5. Абсорбционные методы очистки газов от сероводорода и галогенов.
- •6. Адсорбционные и хемосорбционные методы очистки отходящих газов. Типы адсорбентов. Регенерация адсорбентов.
- •7. Адсорбционные методы очистки отходящих газов от диоксида серы, оксидов азота, галогенов и сероводорода.
- •8. Адсорбционные методы очистки отходящих газов от летучих органических соединений. Адсорбционное оборудование.
- •9. Методы каталитической очистки газов от диоксида серы и оксида углерода и оксидов азота.
- •10. Термическое обезвреживание отходящих газов промышленности.
- •Достоинства метода прямого сжигания:– простота аппаратурного оформления;
- •11. Классификация сточных вод и методов очистки сточных вод. Основные принципы выбора схем очистки.
- •12. Удаление взвешенных частиц из сточных вод отстаиванием, фильтрованием.
- •13. Методы очистки сточных вод коагуляцией, флокуляцией и флотацией.
- •14. Химические методы очистки сточных вод: нейтрализация, окисление и восстановление.
- •15. Адсорбционные методы очистки сточных вод. Очистка сточных вод на ионитах.
- •16.Электрохимические методы очистки сточных вод.
- •17. Методы удаления ионов тяжелых металлов из сточных вод.
- •18. Биохимические методы очистки сточных вод (основные положения, факторы, влияющие на скорость биохимического окисления, аппаратурное оформление).
- •19. Обработка и утилизация осадков сточных вод со станций бос.
- •20. Термические методы очистки сточных вод (методы концентрирования и термоокислительные методы).
- •21. Федеральный закон « Об отходах производства и потребления».
- •22. Федеральный классификационный каталог отходов. Классы токсичности отходов.
- •Название виду отхода присваивают с учетом его происхождения и химического состава.
- •23. Механические и механотермические методы подготовки отходов к переработке.
- •24. Термические методы переработки промышленных отходов.
- •25. Переработка отходов производства серной кислоты.
- •26 Переработка отходов производства фосфорной кислоты и кальцинированной соды.
- •27. Биохимические методы переработки отходов.
- •28. Переработка отходов высокомолекулярных органических содержаний (переработка пластмасс, изношенных шин)
- •29. Методы переработки гальваношламов и ртуть содержащих отходов.
- •30. Полигоны тбо и полигоны промышленных отходов. Проектирование и эксплуатация пром. Полигонов и полигонов тбо
4. Абсорбционные методы очистки газов от диоксида серы: нерекуперативные и рекуперативные методы.
Для
очистки отходящих газов от СО2
предложено большое количество
хемосорбционных методов, однако на
практике нашли применение лишь некоторые
из них. Это связано с тем, что объемы
отходящих газов велики, а концентрация
в них S02
мала, газы характеризуются высокой
температурой н значительным содержанием
пыли. Для абсорбции могут быть использованы
вода, водные растворы и суспензии солей
щелочных и щелочноземельных
металлов.Абсорбция водой. Абсорбция
водой диоксида серы сопровождается
реакцией:
![]() Растворимость
SO2
в воде мала.
Растворимость
SO2
в воде мала.
Нерекуперационные методы. Известняковые и известковые методы Для приготовления суспензий применяется измельченный известняк с размером частиц 0,1 мм. Предложено несколько схем очистки газов. Наиболее простая с образованием шлама. Абсорбер орошается суспензией с рН = 6-6,2. Шлам из абсорбера частично поступает в циркуляционный сборник, куда подается свежий известняк, а частично направляется на отделение воды в центрифугу или на фильтр.
 Рекуперационные
методы очистки с регенерацией
хемосорбентов. В
этих процессах поглотитель регенерируют
и повторно используют для очистки, а
извлекаемый компонент перерабатывают
в товарные серосодержащие продукты:
серную кислоту, элементную серу, сжиженный
диоксид серы и сульфаты. Методы
классифицируют по типу хемосорбентов.
Рассмотрим некоторые из них.Магнезитовый
метод.
СО2
в этом случае поглощают оксид-гидрооксидом
магния. В процессе хемосорбции образуются
кристаллогидраты сульфита магния,
которые сушат, а затем термически
разлагают на SО2-содержащий
газ и оксид магния. Газ перерабатывают
в серную кислоту, а оксид магния возвращают
на абсорбцию.В абсорбере протекают
следующие реакции:
Рекуперационные
методы очистки с регенерацией
хемосорбентов. В
этих процессах поглотитель регенерируют
и повторно используют для очистки, а
извлекаемый компонент перерабатывают
в товарные серосодержащие продукты:
серную кислоту, элементную серу, сжиженный
диоксид серы и сульфаты. Методы
классифицируют по типу хемосорбентов.
Рассмотрим некоторые из них.Магнезитовый
метод.
СО2
в этом случае поглощают оксид-гидрооксидом
магния. В процессе хемосорбции образуются
кристаллогидраты сульфита магния,
которые сушат, а затем термически
разлагают на SО2-содержащий
газ и оксид магния. Газ перерабатывают
в серную кислоту, а оксид магния возвращают
на абсорбцию.В абсорбере протекают
следующие реакции:
MgO + H2O → Mg(ОН) 2, MgSO3 + H2O + SO2 = Mg(HSO3)2,
Mg (HSО3)2 + Mg (OH)2 = 2MgSО3 + 2H2O.
Растворимость сульфита магния в воде ограничена, избыток его в виде MgSO3·6H2O и MgSO3·3H2O выпадает в осадок.
Т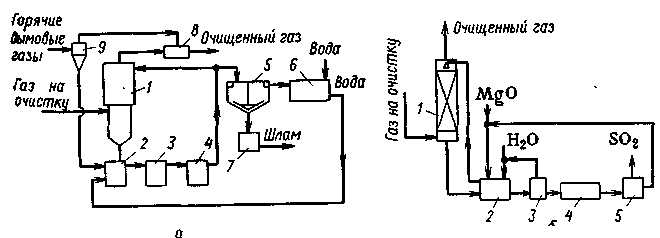 ехнологическая
схема процесса представлена на рис.
ехнологическая
схема процесса представлена на рис.
Рис.
Схемы установки очистки газа от диоксида
серы и
оксида магния: 1 – абсорбер, 2 –
нейтрализатор, 3 – центрифуга, 4 –
сушилка, 5 – печьПри
этом идет реакция:
![]()
Цинковый метод. Абсорбентом служит суспензия оксида цинка, при этом идет реакция:
SO2+ZnO+2,5H2O = ZnSO3 + 2,5 Н20
Образующийся
сульфит цинка нерастворим в воде, его
отделяют в гидроциклонах, а затем сушат
и обжигают при 350 °С. Сульфит цинка
разлагается по реакции:
![]()
Образующийся СО2 перерабатывают, а оксид цинка возвращают на абсорбцию.Достоинством метода является возможность проводить процесс очистки при высокой температуре (200-250 °С). Недостаток – образование сульфата цинка, который экономически не целесообразно подвергать регенерации, а необходимо непрерывно выводить из системы и добавлять в нее эквивалентное количество диоксида цинка.
Абсорбция хемосорбентами на основе натрия. Достоинством этого метода является использование нелетучих хемосорбентов, обладающих большой поглотительной способностью.
Na2CO3 + SО2 = Na2SO3 + O2, Na2SO3 + SО2 + H2O = 2NaHS03.
При абсорбции гидроксидом натрия также образуются сульфит-бисульфитные растворы. Газы вступают в реакцию с сульфитом и бисульфитом, что ведет к увеличению содержания бисульфита:
SO2 + NaHSО3 + Na2SO3 + H2O = 3NaHSO3.
Образующийся раствор взаимодействует с оксидом цинка: NaHSO3 + ZnO → ZnSO3 + NaOH
Сульфит цинка обжигают: ZnSО3 = ZnO + SO2.
Диоксид серы перерабатывают в серную кислоту или серу, а оксид цинка возвращают в процесс.
Двойной
щелочной метод.
Сущность его заключается в использовании
при абсорбции SO2
растворов солей натрия, калия или аммония
с последующей регенерацией отработанных
абсорбентов оксидом или карбонатом
кальция. В качестве продуктов рекуперации
получают гипс, сульфит кальция или их
смесь. Регенерированный абсорбент
возвращают в цикл абсорбции, а соли
кальция удаляют из системы. Регенерация
абсорбента происходит по следующим
реакциям:![]()
![]()
![]()
Аммиачные методы. В этих методах поглощение диоксида серы производится аммиачной водой или водными растворами сульфит-бисульфита аммония с последующим его выделением. Достоинством метода является высокая эффективность процесса, доступность сорбента и получение необходимых продуктов (сульфит и бисульфит аммония).
Абсорбция расплавленными солями. Для очистки газов при высокой температуре используется эвтектическая смесь карбонатов щелочных металлов состава (в %): LiCO3 – 32; Na2СO3 – 33; К2СО3 – 35.. При содержании SO2 в газе от 0,3 до 3% смесь абсорбирует 99% SO2. Процесс состоит из стадий абсорбции, восстановления и регенерации абсорбента. Абсорбция SO2 производится карбонатами с образованием сульфитов и сульфатов металлов. Абсорбцию проводят в оросительном скруббере при скорости газа 7,5 м/с. Реакции, проходящие в скруббере, экзотермичны, что позволяет частично компенсировать потерю тепла.На стадии восстановления используют генераторный газ. Процесс проводят при 600 °С. Происходит восстановление сульфатов до сульфидов металлов:
![]()
![]()
![]()
Реакции
восстановления протекают медленно. На
стадии регенерации сульфиды реагируют
со смесью СО2
и
воды при 425 °С:
![]()
Реакция протекает быстро. Полученный расплав солей вновь возвращают в процесс, газ, выходящий из реактора регенерации, содержит 30% H2S, оксид углерода и воду. Его направляют на установку для получения серы.
