
- •Обжиг никелевых сульфидных концентратов Задание
- •Исходные данные
- •I. Расчет материальных балансов
- •Рациональный (минеральный) состав концентрата
- •1.4. Расчет дутья (на 100 кг концентрата)
- •1.5. Расчет состава обжиговых газов
- •1.6. Расчет параметров кипящего слоя
- •1.8.5. Состав обжиговых газов на часовую производительность
- •129. Водяные пары в газах, т/ч
- •Литература
Обжиг никелевых сульфидных концентратов Задание
Произвести расчет полного обжига никелевого сульфидного концентрата в печи кипящего по следующей схеме:
1) Расчет минерального (рационального) состава концентрата
Расчет материального баланса обжига.
Расчет необходимого числа обжиговых печей
Расчет теплового баланса печи
Исходные данные
Таблица 1
Состав концентрата (по сухому), % (масс.)
-
Материалы
Ni
Cu
Co
Fe
S
Проч
Сумма
Концентрат
63,5
4,2
1,6
2,4
23,5
4,8
100,0
Состав (качественный): Ni3S2, Ni, Cu2S, Cu, CoS, FeS, Fe3O4.
Плотность частиц обжигаемой шихты тв = 6500 кг/м3.
Температура при обжиге t = 1150 оС. (Т = 1423 К)
Эквивалентный диаметр частиц d = 6,6ּ10-4 t – 0,38 = 0,346 мм.
Влажность концентрата 7,0 %.
Площадь пода печи Sq = 24,0 м2.
Годовая производительность цеха по концентрату 180 тыс.т / год.
Унос пыли от массы шихты, % - 30,0.
На рис. 1 приведена принципиальная технологическая схема применительно к расчету.
Р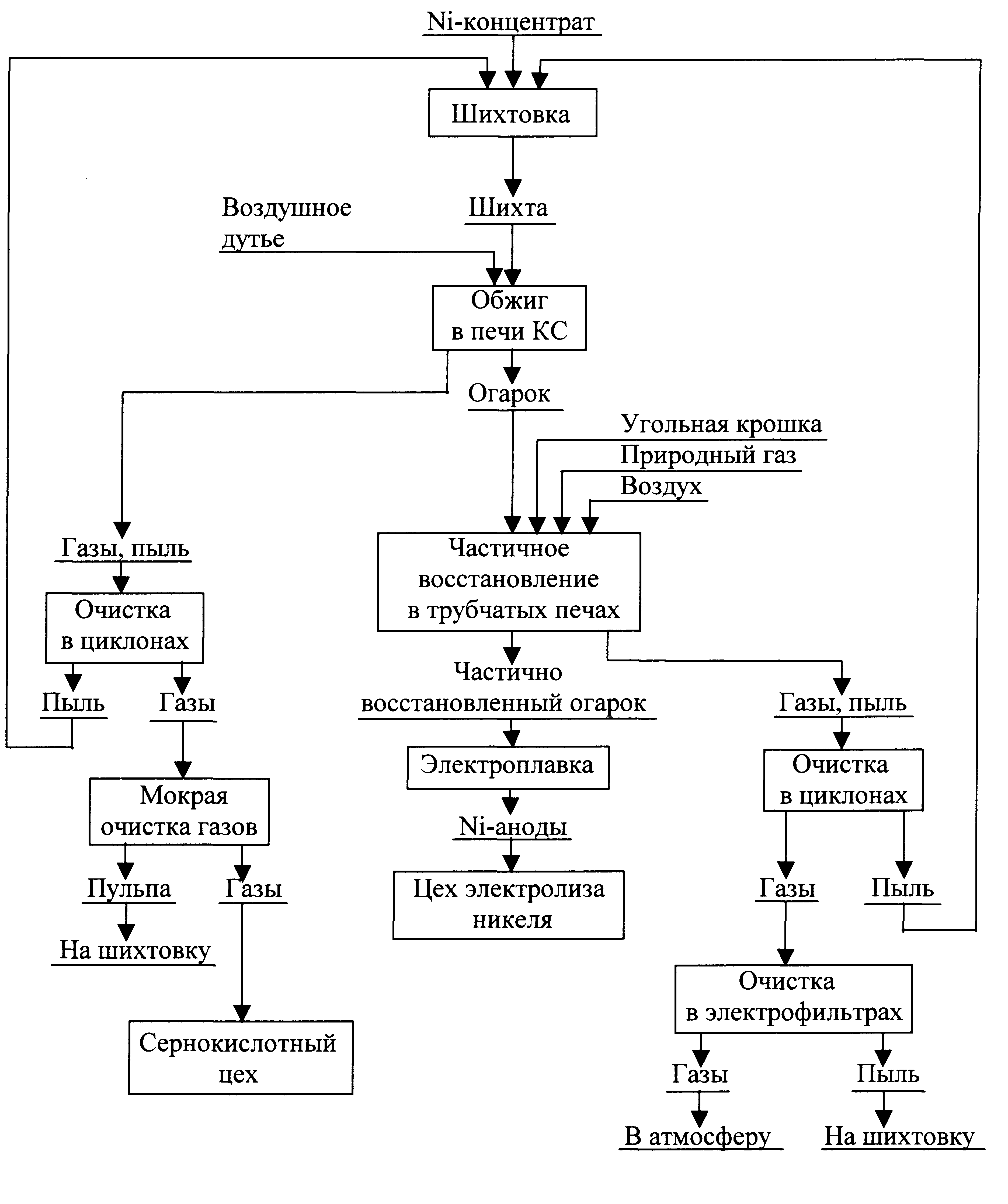 ис.
1. Принципиальная технологическая схема
обжига никелевых
ис.
1. Принципиальная технологическая схема
обжига никелевых
концентратов от флотационного разделения Cu-Ni файнштейна
I. Расчет материальных балансов
Рациональный (минеральный) состав концентрата
(на 100 кг сухого концентрата, кг.)
По данным [1] 10 % меди находится в концентрате в металлическом виде, а 90 % - в виде Cu2S; кобальт целиком в виде CoS; железо поровну (по 50 %) в виде FeS и Fe3O4; никель в виде Ni3S2, а остаток в металлическом виде.
Медь в Cu2S, кг
![]()
Масса Cu2S, кг.
![]()
Здесь 159,158 – молекулярная масса Cu2S;
63,546 – атомная масса Cu.
Сера в Cu2S, кг.
![]()
Медь в металлической форме, кг
![]()
5. Масса CoS, кг
![]()
6. Сера в CoS, кг
![]()
7. Масса железа в виде FeS, кг
![]()
8. Масса FeS, кг
![]()
9. Сера в FeS, кг
![]()
10. Масса железа в виде Fe3O4, кг
![]()
11. Масса Fe3O4, кг
![]()
12. Кислород в Fe3O4, кг
![]()
13. Сера в Ni3S2, кг
![]()
14. Масса Ni3S2, кг
![]()
где 240,202 – молекулярная масса Ni3S2;
32,066 – атомная масса S.
15. Никель в Ni3S2, кг
![]()
16. Никель в металлическом состоянии, кг
![]()
16’. Прочие (по разности), кг
![]()
Таблица 2
Рациональный состав Ni-концентрата
-
Соеди-
Нения
Ni
Cu
Co
Fe
S
O
Проч.
Сумма
Ni3S2
57,616
-
-
-
20,986
-
-
78,602
Ni
5,884
-
-
-
-
-
-
5,884
Cu2S
-
3,780
-
-
0,954
-
-
4,734
Cu
-
0,420
-
-
-
-
-
0,420
CoS
-
-
1,600
-
0,871
-
-
2,471
FeS
-
-
-
1,200
0,689
-
-
1,889
Fe3O4
-
-
-
1,200
-
0,458
-
1,658
Проч
-
-
-
-
-
-
4,342
4,342
Сумма
63,500
4,200
1,600
2,400
23,500
0,458
0,022
100,000
1.2. Рациональный состав огарка (Sог = 0,2 %)
По данным [1] принимаем, что в огарок переходит без изменения вся металлическая медь и 10 % металлического никеля. Содержание серы в огарке по технологическим причинам принимаем 0,2 %.
17. Масса серы в огарке, кг
Принимаем выход огарка 95,5% от массы концентрата при содержании в нем серы 0,2 %, что соответствует производственным данным. Тогда
![]()
18. Масса Ni3S2 в огарке, кг
![]()
19. Никель в Ni3S2 , кг
![]()
20. Металлический никель в огарке, кг
![]()
21. Суммарная масса окисляющегося при обжиге никеля, кг
![]()
22. Кислород для образования NiO, кг
![]()
23. Масса NiO в огарке, кг
![]()
24. Металлическая медь в огарке, кг
![]()
25. Окисляется меди, кг
![]()
26. Кислород в Cu2O, кг
![]()
27. Масса Cu2O, кг
![]()
28. Кислород для окисления кобальта, кг
![]()
29. Масса CoO в огарке, кг
![]()
30. Кислород, необходимый для окисления железа до Fe2O3, кг
![]()
31. Масса Fe2O3 в огарке, кг
![]()
32. Суммарная масса кислорода в оксидах огарка, кг
![]()
33. Выход огарка на 100 кг концентрата, кг
![]()
34. Проверка содержания серы в огарке, %
![]()
Таблица 3
Рациональный состав огарка (S = 0,2 %)
-
Соеди-
нения
Ni
Cu
Co
Fe
S
O
Проч.
Сумма
NiO
62,388
-
-
-
-
17,007
-
79,395
Ni3S2
0,524
-
-
-
0,191
-
-
0,715
Ni
0,588
-
-
-
-
-
-
0,588
Cu2O
-
3,780
0,476
4,256
Cu
-
0,420
-
-
-
-
-
0,420
CoO
-
-
1,600
-
-
0,434
-
2,034
Fe2O3
-
-
-
2,400
-
1,031
-
3,431
Проч
-
-
-
-
-
-
4,800
4,800
Сумма
63,500
4,200
1,600
2,400
0,191
18,948
4,800
95,639
1.3. Рациональный состав циклонной пыли (Sп = 2,0 %)
35. Масса серы в пыли, кг
Согласно предварительным расчетам выход огарка при содержании в нем серы 0,2 % составляет 95, 5кг на 100 кг концентрат.
Тогда
![]()
36. Масса Ni3S2 в пыли, кг
![]()
37. Никель в Ni3S2, кг
![]()
38. Металлический никель в пыли (10 % от Niк-т), кг
![]()
39. Суммарная масса окисляющегося никеля, кг
![]()
40. Кислород в NiO, кг
![]()
41. Масса NiO, кг
![]()
42. Металлическая медь в пыли, кг
![]()
43. Масса окисляющейся меди, кг
![]()
44. Кислород в Cu2O, кг
![]()
![]()
45. Масса Cu2O, кг
![]()
46. Кислород для окисления кобальта, кг
![]()
47. Масса CoO, кг
![]()
48. Кислород для окисления железа в Fe2O3, кг
![]()
49. Масса Fe2O3, кг
![]()
50. Суммарная масса кислорода в оксидах металлов, кг
![]()
51. Выход огарка из 100 кг концентрата, кг
![]()
52. Проверка содержания серы в огарке, %
![]()
Таблица 4
Рациональный состав пыли (S = 2,0 %) на 100 кг концентрата
-
Соеди-
нения
Ni
Cu
Co
Fe
S
O
Проч.
Сумма
NiO
57,668
-
-
-
-
15,721
-
73,389
Ni3S2
5,244
-
-
-
1,910
-
-
7,154
Ni
0,588
-
-
-
-
-
-
0,588
Cu2O
-
3,780
0,476
4,256
Cu
-
0,420
-
-
-
-
-
0,420
CoO
-
-
1,600
-
-
0,434
-
2,034
Fe2O3
-
-
-
2,400
-
1,031
-
3,431
Проч
-
-
-
-
-
-
4,800
4,800
Сумма
63,500
4,200
1,600
2,400
1,910
17,662
4,800
96,072
