
Сандар
(MnOH)2SO3 тұзы қалай аталады? В) марганец гидроксосульфиті
“f”-электрон бұлты деңгейiндегi орбиталь санын көрсет: D)7
0,01М CuSO4 ерiтiндiсiндегi мыстың электродтық потенциалын (В) анықтаңыз: E0Cu2+/Cu=+0.34B. С)+0,28
0,01М HNO3 ерiтiндiсiнiң рОН мәнiн есептеңiз.B) 12
0,01М ZnSO4 тұзы ерiтiндiсiндегi мырыштың электрод потенциалын есептеңiз: E0Zn2+/Zn = - 0,76B. С)-0,82
0,01М КОН ерiтiндiсiнiң рН мәнiн есептеңiз. А) 2
0,25 моль молекулалық хлордағы хлордың атомдық саны:D)1,51. 1023;
0,25М NaOH ерiтiндiсiнiң титрiн анықтаныз.А) 0,01
0,5 л 1Н Na2SO4 ерiтiндiсiн дайындау үшiн қанша грамм Na2SO4 өлшеп алу керек? С) 35,5
0,5 моль күкiрт қышқылының массасы (г) қандай? M(H2SO4)=98 г/моль B)49 г
0,5 моль сутегiнiң (қ.ж.) көлемiн анықтаңыз.В)11,2
1 л ерiтiндiде 6,3 г HNO3 (М.м.=63 г/моль) ерiтiлген. Осы ерiтiндiнiң молярлық концентрациясын анықтаңыз. В) 0,1
1 литр ерiтiндiде 98 г H2SO4 болса (MH2SO4=98 г/моль) осы ерiтiндiнiң молярлық концентрациясы қандай?С) 1М
1 литр құрамында 49 г H2SO4 бар. Осы ерiтiндiнiң нормальдық концентрациясы неге тең? Mr(H2SO4)=98 г/моль. А)1
1 мл 40%-тiк ерiтiндiде 0,45 г ерiген зат бар. Ерiтiндiнiң тығыздығын табыңыз.А) 0,85 г/мл
1 сағ бойы AlCl3 балқымасынан 13,4 А. ток жiбергенде бөлiнетiн алюминийдiң массасы:А)4,5 г
100 г Н2О да 10 г глицеринді С3Н8О3 ерiткенде глицерин ерiтiндiсiнiң қату температурасы қанша градусқа төмендейдi? (МС3Н8O3=92 г/моль). КН2О=1,860С.Е) 9,20С
100 мл ерiтiндiде 3,4 г AgNO3 болса, осы ерiтiндiнiң нормалдығы қандай? M(AgNO3) =170 г/моль А) 0,2
100 мл ерiтiндiде 3,4 г AgNO3 ерiтiлген. Ерiтiндiнiң нормалдығы қандай? M(AgNO3 )=170 г/моль). А) 0,2
100 мл ерiтiндiде 49 г H2SO4 бар болса, осы ерiтiндiнiң нормалдығы қандай?А)10
11,2 л көмiртегi (IV) оксидiнiң қалыпты жағдайдағы мөлшерi нешеге тең?В)0,5
15 минут 5 А. токты күмiс нитраты ерiтiндiсiнен өткiзгенде 5,04 г күмiс бөлiндi. Ток шығымы қандай? А)85% С)100%
160 г суда 40 г тұз ерiтiлген. Ерiтiндiдегi заттың массалық үлесi қандай (, %)? D)25
180С температурада Mg(OH)2 –магний гидроксидiнiң суда ерiгiштiгi 1,7*10-4 моль/л. Осы температурадағы Mg(OH)2-ерiгiштiк көбейтiндiсiн анықта (молл/л).А)1,96*10-11
2 моль су мөлшерiн 2А ток күшiмен ыдыратуға қанша уақыт (сағ-мөлшерiмен) қажет?А)53,6
2 моль темiр сульфидiнiң (FeS) массасын көрсетiңiз. В)176 г
2 моль хлордың (Cl2) қалыпты жағдайдағы көлемi қандай?D)44,8
2,5 А токты қалайы хлоридiнен SnCl2 30 мин өткiзгенде 2,77 г қалайы бөлiндi. Қалайының эквивалентiн тап.А)29,7
20 %-тiк ерiтiндi дайындау үшiн 400 г суда NaNO3-тiң қандай мөлшерiн ерiту керек? D) 80г
200 г Н2О да 40 г қантты С12Н22О11 ерiткенде қант ерiтiндiсiнiң қайнау температурасы қанша градусқа өседi? (МС12H22O11=342 г/моль). ЕН2О=0,520. В) 0,60С
200 г суда 5,4 г зат ерiтiлген және ерiтiндiнiњ ќайнау температурасы 100,0780С. Ерiген заттыњ молекулалыќ массасын есептењiз. Судыњ эбуллиоскопиялыќ константасы 0,520 D) 180;
250 г суға 54 г глюкоза (C6H12O6) ерiтiлген. Осы ерiтiндi қандай температурада (0С) кристалданады? В)-2,23
250 мл ерiтiндiдегi 10,5 г натрий фторидiнiң нормалдық концентрациясы неге тең? MNaF=42 г/моль.С)1
250 мл сулы ерiтiндiде 10,5 г натрий фторидi ерiтiлген. (Мr(NaF)=42). Ерiтiндiнiң нормальдық концентрациясын анықтаңыз.А)1
250С температурада 0,5М глюкоза (С6Н12О6) ерiтiндiсiнiң осмос қысымы неге тең? В) 1,24
298 К-де PbO2-нi цинкпен PbO(к)+2Zn(к)Pb(к)+2ZnO(к) реакциясы бойынша тотықсыздандыруға бола ма?В)-99,2; болады
2CO(г) +O2 (г) 2CO(г)+Q жүйесiндегi тепе-теңдiктi солға, яғни бастапқы заттар жағына ығыстыру үшiн:D)температураны өсiредi
2NO(г)+O2(г)2NO2(г) жүйесiндегi қысымды 4 есе өсiрсе реакция жылдамдығы қанша есе өседi?Е)64
2NO+O22NO2+Q-реакция тепе-теңдiгi солға қарай қай жағдайда ығысады?В)температураны көтергенде
2SO2 + O2 2SO3 системасында заттардыњ тепе-тењдiк күйдегi концентрациялар: [SO2] = 0,04 моль/л, [O2] = 0,06 моль/л, [SO3] = 0,02 моль/л. Тепе-тењдік констан-тасын есептењіз.B) 4,17;
2SO2(г)+O2(г)2SO3(г) жүйесiнiң қысысымын 2 есе азайтқанда реакция жылдамдығы қалай өзгередi D)8 есе кемидi
2А+ВА2В –реакция жылдамдығы қалай өзгередi, егер А–заты концентрациясын 2 есе арттырып, ал B заты концентрациясын 2 есе азайтса?А) 2 өсе өсед
2А2(г)+В2(г)=2А2В(г)-реакциядағы А-заты концентрациясын 4 есе төмендету нәтижесiнде тура және керi реакция жылдамдығы өзгермеуi үшiн B2 заты концентрациясын неше есе арттыру қажет? В) 16 есе
2РН3(г)+4О2(г)=р2О5(г)+3Н2О(с) реакция теңдеуiн пайдаланып фосфиннiң (Н0298 РН3, кДж/моль) түзiлуiнiң стандартты жылуын табыңыз егер Нх.р.=-2360 кДж; Н0298 Р2О5(г)=-1492 кДж/моль; Н0298 Н2О(с)=-285,8 кДж/моль болса. D)+5,3
30 г бейэлектролит (электролит емес) 500 г суда ерiтiлген. КН2О=1,860С. Ерiтiндi –1,860С-та қатады. Ерiтiлген заттың молекулалық массасын анықтаңыз (г/моль).В) 60
34 г аммиак (NH3) қалыпты жағдайда қандай көлем (л) алады?А)44,8 л
3H2(г)+N2(г) 2NH3(г) жүйесiндегi тепе-теңдiктi оңға, яғни аммиак түзiлу жағына ығыстыру үшiн:А)қысымды өсiредi
3H2(г)+N2(г)2NH3(г) реакциясының жылдамдығы сутегi концентрациясын 2 есе өсiргенде қанша есе өседi? D)8
4 энергетикалық деңгейде қанша деңгейше бар? D)4
400 г 50 % H2SO4 ерiтiндiсiнен (массасы бойынша) буландырып 100 г суды бөлiп алдық. Қалған ерiтiндiдегi H2SO4 массалық үлесi (%) неге тең?В)66,7
44,5 г AlCl3 –гі хлор атомының саны неге тең? В)6,02 . 1023;
4HCl(г)+O2(г)2H2O(г)+2Cl2(г) реакциясының жылдамдығы HCl концентрациясын 2 есе өсiргенде қанша есе өседi?D)16
4NН3(г)+5NO2(г)=4NO(г)+6H2O(Бу) жүйесiнiң қысымын 2 есе өсiрсе реакция жылдамдығы қанша есе өседi?Е)512
5 л газдың қалыпты жағдайдағы массасы 7,15 г. Осы газдың азотпен салыстырғандағы тығыздығын табыңыз.А)1,14
5,6 г күкiрт темiрмен қосылғанда 17,59 кДж жылу бөлiнген. Мына реакция бойынша: Fe+S=FeS темiр сульфидiнiң түзiлу жылуын есептеңiз, В)56 кДж/моль
5,6 л азот оксидiнiң (NO) қ.ж. мөлшерiн () табыңыз?С)0,25 моль
500 мл 0,25Н Na2CO3 ерiтiндiсiнде қанша Na2CO3 (г) ерiтiлген? В)6,63
56 г азоттың (N2) қ.ж. моль санын көрсетiңiз.В)2,0
80 г электролит емес зат 2 кг суда (Н2О) ерiтiлген. Бұл заттың молярлық массасы 80 г/моль. KH2O=1,860. Ерiтiндiнiң қату температурасын анықтаңыз (t). D) -0,930
ААААА
Ag/AgNO3 (0,001M)//AgNO3 (0,1M)/Ag галлBаникалық элементтiң ЭҚК (B) есепте, егер E0Ag/Ag+=+0,80В тең болса.С)0,12
AgNO3 ерiтiндiсiн электролиздегенде анод маңында қайсы зат концентрленедi? B)HNO3
AgNO3 ерiтiндiсiнен массасы 108 г күмiстi 6 мин. iшiнде бөлiп алу үшiн кандай ток күшiн жұмсау керек?А)268 А
AgNO3 тұзының ерiтiндiсiнен 1,5 А токты 1 мин бойы жiбергенде катодта бөлiнетiн күмiстiң массасы қандай? Е)0,1 г
Al2(SO4)3 диссоциацияланғанда қанша катион түзіледі?В)2
Al2O3 MgOK2O қатарында оксидтердің негіздік қасиеттері артады:В)өседі;
AuCl3 ерiтiндiсiн 30 минут бойы электролиздегенде катодта 0,5 г Au бөлiну үшiн қажеттi ток күшiн анықтаңыз. С)0,4А
AuCl3 және KCl ерiтiндiсiнiң қоспасын электролиздегенде, электродта қандай заттар бөлiнедi?D)Au және Cl2
ВВВВВВ
BCl3-молекуласында орбитальдардың гибридтiк түрi қандай? В)sp2
BF3 молекуласындағы орбитальдардың гибридтену күйi: В) sp2
Bаленттiк электрондар формуласы …s23p5 болатын элементтiң min және max тотығу дәрежелерiн көрсетiңiз.А)(-2)-(+6)
ССССССС
Ca(OH)2
– каллций гидроксидiнiң эквиваленттiк
массасының мәнiн көрсетiңiз:D)
M(![]() Са(ОН)2
)=37 г/моль
Са(ОН)2
)=37 г/моль
CaCO3 (қ) CaO(қ) + CO2 (г) реакциясының тепе-теңдік константасының өрнегін табыңыз: А) K pCO2;
CH3COONa натрий ацетатының молярлық массасы қандай? B) M(NaCH3COO)=82 г/моль
ClO3- ионы Cl- -на тотықсызданғанда қатысатын Н+ моль саны неге тең?Е)6
Cu(NO3)2 ерiтiндiсiн электролиздегенде электродтарда (катод және анодта) қандай заттар бөлiнедi: В)Cu және O2
CuCl2 ерiтiндiсiн электролиздегенде катодта бөлiнетiн зат:А)Cu
CuSO4 ерiтiндiсiн электролиздегенде электродтарда (катод және анодта) қандай заттар бөлiнедi:В)Cu және O2
FFFFFFF
Fe(HSO3)3 тұзының атын атаңыз. D) темiр (III) гидросульфиты
Fe2(SO4)3 тұзының диссоциациясы нәтижесiнде барлығы қанша ион түзiледi? Е) 5
Fe2O3 қайсы затпен әрекеттеседi? С) H2SO4
Fe2O3(к)+3CO(г)=2Fe(к)+3CO2(г) реакциясы бойынша темiр (III) оксидiнiң түзiлуiнiң стандартты энтальпиясын табыңыз:Нх.р.=-28,42 кДж; Н0298 СО(г)=-110,4 кДж/моль; Н0298 СО2(г) =-393,1 кДж/моль.А)-819,7
Fe3O4(қатты)+4CO(г) 3Fe(қатты)+4CO2 (г) тепе-теңдiкте тұрған реакция қысымын өсiрсе тепе-теңдiк қалай қарай ығысады?B)ығыспайды
FeCl3 ерiтiндiсi арқылы 2 минут бойы 1,5 А ток күшiн жiбергенде катодта темiрдiң қандай мөлшерi бөлiнедi? С)0,03 г
HHHHHH
H2(г)
+ CI2(г)
2HCI(г)
реакцияныњ тепе-тењдік константасын
жазыњыз.С)
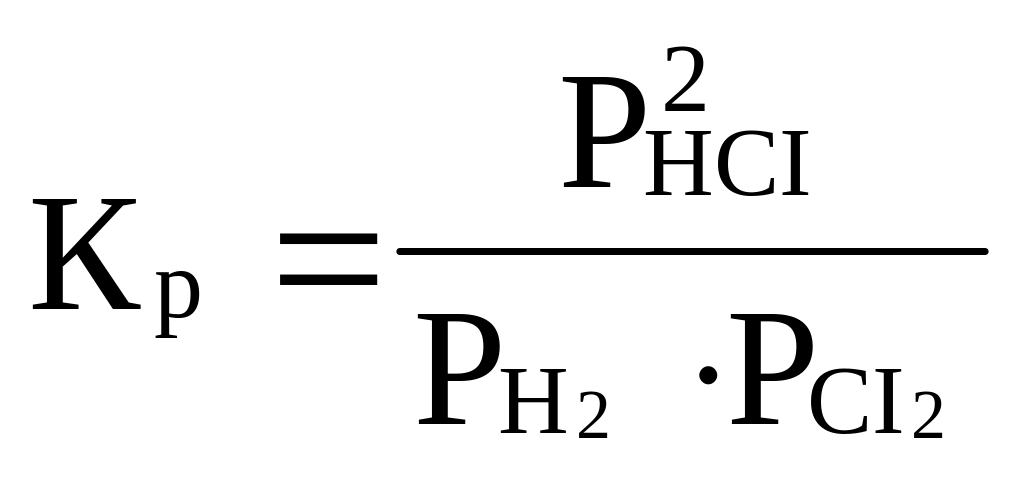 ;
;
H2(г) + I2(к) 2HI(г) реакциясыныңтепе-теңдік константасының өрнегін көрсет:В) Kp p2HI/pH2;
H2O – H2S – H2Se – H2Te - қатарда байланыс тұрақтылығы қалай өзгередi?В)төмендейдi
H2S+H2SO3S+H2O тотығу – тотықсыздану реакциясын теңестiрiп түзiлген күкiрттiң моль санын анықтаңыз. С)3
H2SO4 қайсы затпен әрекеттеседi? B) CuO
H2SO4-күкiрт қышқылының молярлық массасы қандай? B)M(H2SO4)=98 г/моль
HCl ерітіндісі диссоциацияланғанда қанша ион түзіледі? В)2
HCl молекуласындағы химиялық байланыс түрiн көрсетініз:В)коваленттiк, полюстi KKKKKKK
KMnO4+H2S+H2SO4MnSO4+K2SO4+S+H2O. Осы реакциядағы тотықтырғыштың моль санын табыңыз.А)2
KMnO4+NaNO2+H2SO4MnSO4+NaNO3+K2SO4+H2O тотығу-тотықсыздану реакциясына қатысатын электрондар санын анықтаңыз. В)10
KMnO4+NaNO2+КОНК2MnO4+NaNO3+H2O тотығу-тотықсыздану ряакциясындағы тотықтырғыштың моль санын табыңыз. В)2
MMMMMM
Mg(NO3)2 тұзы ерiтiндiсi электролизiнде анодта бөлiнетiн затты көрсетiңiз. С)O2
Mg0+HNO3Mg(NO3)2+NH4NO3+H2O реакция теңдеуiн аяқтап, тотықсыздандырғыш алдындағы коэффициентiн анықтаңыз: B)4
MgCl2 ерiтiндiсiн электролиздегенде катодта бөлiнетiн зат: Е)H2
MgCO3(қ) MgO(қ) + CO2 (г) реакциясының тепе-теңдік константасының өрнегін жазыңыз:Д) K pCO2;
NNNNNNN
N2 + 3H2 2NH3 реакциясында тепе-тењдік орнаѓандаѓы заттар концентрация-лары: [N2] = 0,03 моль/л, [H2] = 0,10 моль/л, [NH3] = 0,4 моль/л. Тепе-тењдік константасын есептењіз.A) 5333;
N2-молекуласында қанша -байланысы бар?С) екi -байланысы
Na2O2+CO2Na2CO3+O2 реакцияның қай типiне жатады: D)диспорпорциалану
Na3PO4 толық диссоциаланғанда түзiлетiн ион саны: С) 4
NaBr+NaBrO3+H2SO4Br2+Na2SO4+H2O тотығу-тотықсыздану реакциясындағы тотықтырғыштың моль санын анықтаңыз.С)1
NaCl балқымасының электролизi кезiнде катодта қандай процесс жүредi? Егер I=10 A, =1сағ, F=96500 Кл. болса, онда катодта түзiлетiн заттың массасы:А)8,58
NaCrO2+PbO2+2NaOHNa2PbO2+NaCrO4+2H2O тотығу-тотықсыздану реакция-сындағы тотықтырғыштың моль санын анықтаңыз. С)4
NaNO3 ерiтiндiсiн электролиздегенде катод пен анодта бөлiнетiн заттар: D) H2 және O2
NaNO3 және K2SO4 тұздары ерiтiндiлерiнiң қоспаларын электролиздегенде электродта бөлiнетiн заттарды көрсетiңдер.D) H2 және O2
NaOH-пен әрекеттесетiн затты көрсетiңiз?Е) HCl
NH3(г)+HCl(г)=NH4Cl(к) реакциясы G0298NH3=-16,48 кДж/моль,G0298HCl(г)=-95,3 кДж/моль, G0298NH4Сl=-203,22 кДж/моль болғанда стандартты жағдайда өз бетiнше жүре ала ма? В)-91,44; жүредi
NH4+ ионы түзiлуi кезiнде қайсы атом немесе ионның электрон жұбы донор қызметiн атқарады?С) N
NO2(г)N2O(г) реакциясының температура 298К кезiндегi стандартты жылу эффектiсiн табыңыз, егер H0298 N2O(г)=+9,4 кДж/моль, H0 298 NO2(г) =+33,9 кДж/моль болса. B)-58,4
SSSSSSSS
S2- ионына қандай электрондық формула сәйкес келедi? D)3s23p6
S2- -ионына сәйкес келетiн электрондық формула:А)3s23p6
![]() Sb
сурьманың ең кіші және ең үлкен тотығу
дәрежесiн көрсетiңiз. B)(-3)-(+5)
Sb
сурьманың ең кіші және ең үлкен тотығу
дәрежесiн көрсетiңiз. B)(-3)-(+5)
Sn2+ ионының электрондық формуласын көрсет:А)4d105s25p0;
SO2
+ 0,5O2
SO3;
![]() кДж/моль, реакциясы бойынша SO3-њ
шыѓымын арттыру үшін ќандай параметрлерді
ќалай өзгерту керек?D)
О2
мен
SO2-њ
концентрацияларын және жалпы ќысымды
арттыру, ал температураны төмендету
керек;
кДж/моль, реакциясы бойынша SO3-њ
шыѓымын арттыру үшін ќандай параметрлерді
ќалай өзгерту керек?D)
О2
мен
SO2-њ
концентрацияларын және жалпы ќысымды
арттыру, ал температураны төмендету
керек;
ZZZZZZZZZ
Zn/Zn+2 0=-0,76 B мен сутектiк электрод 0=0,00 жартылай элементтен тұратын гальваникалық элементтiң Э.Қ.К. неге тең? В)+0,76
Zn/Zn2+ (0,01 моль/л) // Ag+ (0,01 моль/л)/Ag гальваникалық элементiнiң E0Zn2+/Zn=-0,76 В; E0Ag+/Ag=+0,80 B болса, онда ЭҚК неге тең?А)1,50 В
Zn/Zn2+ (0,01 моль/л) // Cd2+ (0,01 моль/л)/Cd гальваникалық элементiнiң E0Cd2+/Cd=-0,43 B; E0Zn2+/Zn=-0,76 B болса, онда ЭҚК неге тең?В)0,33 В
AAAAAAAA
А2(г)+В2(г)2АВ(г) –реакцияның тепе-теңдiгi қай бағытқа ығысады, егер бiр уақытта қысымды 2 есе, температураны 100С-ке арттырса? Тура реакцияның температуралық коэффициентi 2-ге, керi реакцияның 3-ке тең.А)солға қарай
АВ2-типi молекулалардың қайсысы сызықтық формада болады?А)CaCl2
Авогадро тұрақтысын көрсетiңiз: B)6,02*1023моль-1
Азот атомының қанша дара электроны бар? В)3
Азот молекуласында қанша - байланыс бар? B)2
Азоттың қандай көлемiнде (қ.ж.) 6,02*1024 атом болады?А)22,4 л
Азоттың төменгi және жоғарғы тотығу дәрежесi неге тең?А)-3; +5
Алтын атомы ядросында
неше нейтрон болады
![]() ? D)118
? D)118
Алтын
атомындағы (![]() Au)
протон мен нейтрон сандарының қосындысын
көрсетiңiз. С)197
Au)
протон мен нейтрон сандарының қосындысын
көрсетiңiз. С)197
Амфотерлік оксидті көрсет. С)Al2O3
Ауа бойынша газдың салыстырмалы тығыздығы 1,5 болса, осы газдың молярлық массасын табыңыз. Мауа=29 г/моль.C)44
ӘӘӘӘӘӘӘ
Әлсiз электролиттi көрсетiңiз.С) Al(OH)3
Әрекеттесушi атомдардың ядросын қосатын сызықтың бойымен атомдық орбитальдардың қабысуынан түзiлетiн коваленттiк байланысты қалай аталады?А)-байланыс
Әрекеттесушi заттар концентрациясын арттырғанда реакция жылдамдығы: В)артады
БББББББББББББ
Бiрге болғанда қайсы металл катионы бiрiншi болып тотықсызданады?Е)Cu2+
Бiрдей жағдайдағы қышқылдардың қайсысында ионының Н+ концентрациясы ең аз болады?Е) H2CO3 Kд=5,6*10-11
Байланыс аралығы 1200 болатын молекула:D)AlCl3
Бас кBант саны мәнi n=4-ке тең атомда жалпы қанша электрон болуы мүмкiн?Е)32
Берiлген заттардың қайсысы гидролизiнде қышқыл тұз түзiледi? D) K2S
Берiлген заттардың қайсысы үшiн стандартты түзiлу энтальпиясы нөлге тең? В)N2
Берiлген реакция бойынша: Н3РО4+Са(ОН)2=СаНРО4+2Н2О фосфор қышқылының эквивалентiнiң молярлық массасын табыңыз: А)49
Берiлген реакциядағы тотықсыздандырғыш эквивалентi неге тең?K2Cr2O7+SnCl2+H2SO4Sn(SO4)2+CrCl3+K2SO4 (M(K2Cr2O7)=294г/моль; M(SnCl2)=190 г/моль). D)190/2
Берiлген реакциялар iшiнен нейтралдау (бейтараптану) реакциясын көрсетiңiз. D) 2KOH+H2SO4K2SO4+2H2O
Берiлген реакциялардың қайсысы энтропияның яғни ретсiздiк дәрежесiнiң өсуiмен жүредi?С)2NH3(г)N2(г)+3H2(г)
Берiлген реакцияның 2NO(г)+O2(г)=2NO2(г) -жылдамдығы қалай өзгередi, егер көлемдi 3 есеге азайтса?D) 27 есе артады
Берiлген реакцияның N2(г)+3Н2(г) 2NН3(г) жылдамдығы қалай өзгередi, егер жүйедегi қысымды 3 есе арттырса? С)81
Берiлген схемадан тотықсыздану процесiн көрсетiңiз. С)MnO4-MnO2
Берiлген схемадан, тотығу процесiн көрсетiңiз.А)NO2-NO3-
Берiлген тотығу-тотықсыздану реакциясы нәтижесiнде қандай элементтер тотығу дәрежелерiн өзгертедi?Na2SO4+SiO2+C Na2SiO3+CO2+SO2 D)S және C
Берiлген тұздардың қайсысы калийдiң дигидрофосфаты деп аталады?А) KH2PO4
Берилий гидроксидi түзiлетiн теңдеу қайсысы?D) Be(NO3)2+Ca(OH)2
Берілген ЕК арқылы қайсы ерітіндіде күміс ионы көп екенін анықта.В)AgCl 1,7*10-10
Бойль-Мариотт
мен Гей-Люссак заңының өрнегiн көрсетiңiз.
D)![]() ВВВВВВВВ
ВВВВВВВВ
Вант-Гофф ережесiне сәйкес, температураны әрбiр 100С-ке көтергенде реакция жылдамдығы: В) 2-4 есе өседi
ВН3 молекуласының валенттік бұрышы 1200. Гибридтену түрін атаңыз.С) sp2;
Ггггггггг
Газ
көлемiн қалыпты жағдайға келтiруде
қолданылатын формуланы табыңыз.Е)![]()
Газдық фазада жүрiп жатқан реакцияның температурасын 320 дан 340К өсiргенде реакция жылдамдығы қанша есе өседi?=3.Е)9
Газдың ауа бойынша салыстырмалы тығыздығы 2,21. Осы газдың молекулалық массасын табыңыз. D)64
Газдың көлемiн қалыпты жағдайға келтiретiн формуланы көрсетiңiз. В)
Газдың сутегiмен салыстырылып алынған тығыздығы 22. 1 л осы газдың қалыпты жағдайдағы массасын табыңыз. B)1,96
Гибридтi
бұлт қандай пiшiн алады? С )
)
Галлваникалық элементтiң (Zn0/Zn2+//Mg2+/Mg0) электр қозғаушы күшi неге тең, егер E0Zn/Zn2+=-0,76B, E0Mg/Mg2+=-2,37B?B)+1,61
Гальваникалық элементтiң Э.Қ.К.-ң өлшем бiрлiгi? D)вольт
Гальваникалық элементте қай металдар жұбында никель анод болады?С)Ni және Cu
Гальваникалық элементтегi электродтық потенциалдар: ок-ля=+0,54 В, в-ля= -0,73 В. Жүйенiң ЭҚК есепте.А)1,27 В
Гетерогендi реакция үшiн S(к)+O2(г)=SO2(г) әсер етушi массалар заңының қайсы өрнегi дұрыс?В)V=K*C(O2)
Гидроксид ионының концентрациясы рОН=10-4 болса, ерiтiндiнiң рН-ы қандай? D) 10
Гидролизге ұшырамайтын тұзды көрсетiңiз.А) KNO3
Гидролизге ұшырамайтын тұзды көрсетіңіз.Е)KCl
Гидролиздену реакциясын көсетiңiз. D) Zn(NO3)+H2O
Гидролизі қышқыл орта (рН<7) көрсететін тұзды көрсет: С)MgCl2
Гидролизі сiлтiлiк орта (рН>7) көрсететін тұзды көрсет: В)Na2S
Гомогендi
реакция үшiн :2NO(г)+O2(г)=2NO2(г)![]() әсер
етушi массалар заңының қайсы өрнегi
дұрыс? С)V=K*C2NO*CO2
әсер
етушi массалар заңының қайсы өрнегi
дұрыс? С)V=K*C2NO*CO2
Еееееееее
Егер Н+ концентрациясы 10-3 болса, хлорлы сутегi қышқылының ерiтiндiсiнiң рН нешеге тең?Е) 3
Егер
Н0х.р.=722
кДж, S0298=361
Дж/моль*К болса,
ТiO2+2С=Ti+2CO
процесiнiң
тепе-теңдiктегi температурасын
![]() теңдеуiмен есептеңiз. А)2000
теңдеуiмен есептеңiз. А)2000
Егер катодта 5,6 л (қ.ж.) көлем сутегi бөлiнсе, натрий суллфаты ерiтiндiсi электролизiнде катод маңында түзiлетiн NaOH массасын анықтаңыз.D)20
Егер элементтiң электрондық формуласы …4d25s2 мен аяқталса, қай периодта және топта орналасады: D)4 және 5
Екi түздың бiрiгiп гидролизденуi кезiнде қандай газ бөлiнедi AlCl3+(NH4)2S+HOH? С) H2S
Екiншi топ элементтерi оксидiнiң қайсысы реакцияға түскiш-активтi?D)CdO H0 түз .298=-256,0 кДж/моль
Ең әлсiз қышқылды атаңыз. Е) H2SiO3 Kд=2*10-12
Ең күштi электролитті табыңыз.А) KOH =95%
Ерiген зат мөлшерiнiң ерiткiш массасына қатынасы:С) моляльдық концентрация
Ерiген зат эквивалент санының ерiтiндi көлемiне қатынасы: В) нормальдық концентрация
Ерiтiндi сiлтiлiк орта болатын тұзды көрсетiңiз (рН7). B) K2CO3
Ерiтiндiде рОН=3 болғанда, сутегi ионы концентрациясы неге тең? Е) 10-11
Ерiтiндiде сутегi ионы концентрациясы 1*10-3 моль/л. Ерiтiндiнiң рН-неге тең? С)3
Ерiтiндiнiң рН бiр мәнге өсуi үшiн ерiтiндiдегi сутегi ионы концентрациясын қалай өзгерту қажет? D)10 есе төмендету
Ерiтiндiнiң эквиваленттiк концентрациясын анықтаңыз, егер 100 мл ерiтiндiде 6,3 г HNO3 болса. М(HNO3) = 63 г/моль)B)1,0
Ерiтіндiнiң рОН-ы 3-ке тең болса, сутегi иондары концентрациясы неге тең? Е) 10-11
Ереже бойынша, атомдарда 4р-деңгейiнен кейiн қай деңгейшеге электрондар толтырылады?D)5s
Еру кестесін пайдаланып реакцияның иондық теңдеуiн жазғанда қайсы қосылыстың молекула түрiнде жазылатынын анықтаңыз.D) AgCl
Жылу эффектiсiнiң (Нх.р.) өлшем бiрлiгiн көрсетiңiз.А)Дж
Заттың эквивалентiнiң молярлық массасының өлшем бiрлiгi қандай? А)г/моль
