
- •12 Значение периодической системы
- •Главное квантовое число
- •19 Орбитальное квантовое число
- •Закрепление
- •50 Константа диссоциации
- •Определение
- •[Править]Диссоциация электролитов с многовалентными ионами
- •[Править]Связь константы диссоциации и степени диссоциации
- •История
- •[Править]Уравнения, связывающие pH и pOh [править]Вывод значения pH
- •[Править]pOh
- •[Править]Значения pH в растворах различной кислотности
- •Степень гидролиза
- •Восстановление
- •[Править]Окислительно-восстановительная пара
- •[Править]Виды окислительно-восстановительных реакций
- •[Править]Примеры [править]Окислительно-восстановительная реакция между водородом и фтором
- •[Править]Окисление, восстановление
- •57 Составление уравнений окислительно-восстановительных реакций.
- •58 Важнейшие окислители и восстановители. Классификация окислительно-восстановительных реакций
- •60 Электролиз
60 Электролиз
[править]
Материал из Википедии — свободной энциклопедии
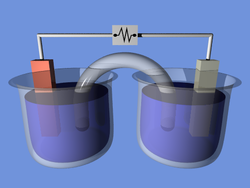
![]()
Схематическое изображениеэлектролитической ячейки для исследования электролиза
Электро́лиз — физико-химический процесс, состоящий в выделении наэлектродах составных частей растворённых веществ или других веществ, являющихся результатом вторичных реакций на электродах, который возникает при прохождении электрического тока через раствор либо расплав электролита.
Упорядоченное движение ионов в проводящих жидкостях происходит в электрическом поле, которое создается электродами — проводниками, соединёнными с полюсами источника электрической энергии. Анодом при электролизе называется положительный электрод, катодом — отрицательный[1]. Положительные ионы — катионы — (ионы металлов, водородные ионы, ионыаммония и др.) — движутся к катоду, отрицательные ионы — анионы — (ионы кислотных остатков и гидроксильной группы) — движутся к аноду.
Явление электролиза широко применяется в современной промышленности. В частности, электролиз является одним из способов промышленного полученияалюминия, водорода, а также гидроксида натрия, хлора, хлорорганических соединений[источник не указан 1309 дней], диоксида марганца[2], пероксида водорода. Большое количество металлов извлекаются из руд и подвергаются переработке с помощью электролиза (электроэкстракция, электрорафинирование). Также, электролиз является основным процессом, благодаря которому функционирует химический источник тока.
Электролиз находит применение в очистке сточных вод (процессы электрокоагуляции, электроэкстракции, электрофлотации
