
- •Методические указания
- •«Химия»
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. … ; … .
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. ; … .
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель.
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. …; ….
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. ….; …..
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. …; … .
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. … ; … .
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. …;
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. … ; …. .
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. …; …
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. … ; … .
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. …; … .
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. … ; … .
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. …; …. .
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. … ; … .
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. …; .…
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. …; .
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. … ; .
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. …; … .
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. ….. ; .
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. … ; .
- •По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. … ; .
Федеральное агентство по образованию
ГОУ ВПО Тюменский архитектурно-строительный университет
Кафедра общей и специальной химии

Методические указания
к контрольной работе № 2
по курсу
«Химия»
для студентов инженерных специальностей 1 курса
Тюмень 2007
Методические указания к контрольной работе №2 по курсу «Химия» для студентов всех специальностей 1 курса: Долматова Н.Н., Качалова Г.С., Турнаева Е.А. дневное отделение – 1 курс, 2 семестр, Тюмень: ТюмГАСУ, 2007 год, 34с.
Рецензент: к.х.н., доцент Полещук Ирина Николаевна
(степень, звание, Фамилия, Имя, Отчество)
Учебно-методический материал утвержден на заседании кафедры :
Протокол №_______ от «_____» ________________2007 г.
Учебно-методический материал утвержден на УМС университета:
Протокол №________от «_____»________________2007 г.
Тираж 200 экземпляров
Предлагаемое методическое указание разработано для студентов дневного отделения инженерных специальностей университета и соответствует учебной программе по курсу «Общая химия». Руководство содержит 27 вариантов заданий, предназначенных для самостоятельного выполнения с целью закрепления полученного теоретического материала по следующим темам:
«Окислительно-восстановительные реакции»,
«Электрохимические процессы: гальванический элемент, коррозия металлов, электролиз»,
«Кальций, магний и их соединения»,
«Жесткость природных вод»,
«Высокомолекулярные соединения».
Вариант 1.
По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель.
 ;
;
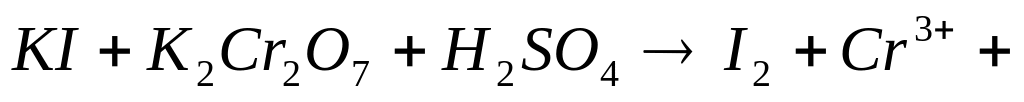 ….
….Составьте схему, запишите уравнения электродных процессов, рассчитайте ЭДС гальванического элемента, составленного из магниевого и медного электродов, погруженных в растворы своих солей с одинаковой концентрации.
Объясните, есть ли разница в протекании коррозии химически чистого и технического железа. Ответ подтвердите электронными уравнениями.
Как протекает гидролиз расплавов и растворов солей? Приведите примеры, запишите уравнения процессов, происходящих в анодном и катодном пространстве.
Какие из природных соединений кальция служат для получения извести? Ответ подтвердите соответствующими уравнениями реакций.
Наличием каких солей объяснятся возникновение жесткости природных вод?
Какой процесс называют полимеризацией? Приведите пример образования полимера из мономеров этим способом.
Вариант 2.
По приведенной схеме химического процесса составьте уравнение окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель. … ; … .
Как изменится масса цинковой пластины при взаимодействии ее с растворами следующих солей: а) NaCl, б) Mg(NO3)2, в ) CuSO4? Почему? Составьте электронные и молекулярные уравнения процессов.
Как происходит коррозия оцинкованного и луженого железа во влажной среде? Составьте электронные уравнения процессов, укажите продукты коррозии.
В каких случаях при электролизе водных растворов солей состав электролита не меняется, на катоде выделяется водород, а на аноде - кислород? Приведите пример и составьте схему электролиза.
Сколько оксида кальция получится при окислении 5,5 г металлического кальция?
Вычислите общую жесткость воды, если в 0,2 л содержится 14,6 мг гидрокарбоната кальция, 2,85 мг гидрокарбоната магния и 10,18 мг хлорида кальция.
Что такое поликонденсация? Приведите пример получения высокомолекулярного соединения этим методом.
Вариант 3.
По приведенной схеме химического процесса составьте уравнения окислительно-восстановительной реакции методом ионно-электронного баланса. Укажите окислитель и восстановитель.
 ;
;
 ….
….Составьте схему, запишите уравнения электродных процессов, рассчитайте ЭДС гальванического элемента, составленного из магниевых электродов, погруженных в растворы электролитов с концентрацией катионов магния 0,1М и 0,0001 М. Как называется такой гальванических элемент?
В раствор серной кислоты поместили пластину из чистого цинка и пластину, покрытую медью. В каком случае коррозия цинка происходит более интенсивно? Почему? Запишите электронные уравнения процесса.
Какая масса алюминия выделится при электролизе расплава хлорида алюминия при прохождении через электролит 193 000 Кл электричества? Составьте схему электролиза.
Составьте молекулярные и ионные уравнения реакции, проходящей при пропускании избытка углекислого газа через водный раствор гидроксида кальция.
Какими солями обусловлены временная и постоянная жесткость воды? Какими методами можно уменьшить жесткость? Приведите примеры, составьте уравнения реакций.
Какие органические соединения называют полимерными? Какими методами можно их получить?
Вариант 4.
