
- •Колядина н.М., Ковальчукова о.В., Страшнова с.Б., Шебалдина л.С. Лабораторные работы по общей и биоорганической химии
- •Часть 2. Органическая химия
- •Рекомендации к выполнению лабораторных работ
- •Лабораторная работа № 1 Предельные и непредельные углеводороды (алканы, алкены и алкины)
- •Опыт 1. Получение метана и изучение его свойств
- •Опыт 2. Горение алканов
- •Опыт 3. Получение этилена и изучение его свойств
- •Опыт 4. Горение алкенов
- •Опыт 5. Получение ацетилена и изучение его свойств
- •Опыт 6. Горение ацетилена
- •Задачи и упражнения
- •Лабораторная работа № 2 Ароматические углеводороды (арены)
- •Опыт 1. Окисление аренов
- •Опыт 2. Взаимодействие аренов с галогенами
- •Опыт 3. Нитрование бензола
- •Задачи и упражнения
- •Лабораторная работа № 3 Спирты. Фенолы
- •Опыт 1. Растворимость спиртов в воде
- •Опыт 2. Окисление спиртов
- •Опыт 3. Получение алкоголятов натрия и изучение их свойств
- •Опыт 4. Получение хелатных комплексов многоатомных спиртов (гликолятов)
- •Опыт 5. Получение иодоформа из этанола (иодоформная проба)
- •Опыт 6. Растворимость фенола в воде
- •Опыт 7. Получение фенолята натрия
- •Опыт 8. Бромирование фенола
- •Задачи и упражнения
- •Лабораторная работа № 4 Альдегиды. Кетоны
- •Опыт 1. Окисление формальдегида и ацетона гидроксидом диамминсеребра
- •Опыт 2. Окисление формальдегида и ацетона гидроксидом меди (II)
- •Опыт 3. Взаимодействие формальдегида с аммиаком (получение уротропина)
- •Опыт 4. Получение ацетона
- •Опыт 5. Получение иодоформа из ацетона и этанола
- •Опыт 6. Получение 2,4-динитрофенилгидразонов
- •Опыт 7. Получение гидросульфитных производных альдегидов и кетонов
- •Что произойдет, если на полученные в этих опытах кристаллы подействовать разбавленным раствором кислоты? Задачи и упражнения
- •Лабораторная работа № 5 Моно- и дикарбоновые кислоты. Аминокислоты
- •Опыт 1. Диссоциация карбоновых кислот
- •Опыт 2. Получение эфиров жирных кислот
- •Опыт 3. Восстановительные свойства карбоновых кислот
- •Опыт 4. Получение комплексного соединения меди (II) с α-аминопропионовой кислотой
- •Опыт 5. Осаждение белка солями тяжелых металлов (денатурация белков)
- •Задачи и упражнения
- •Лабораторная работа № 6 Качественные реакции органических веществ
- •I. Элементный анализ органических соединений Опыт 1. Открытие углерода и водорода в составе органического соединения
- •Опыт 2. Открытие галогенов
- •II. Качественные реакции функциональных групп органических соединений Опыт 1. Обнаружение кратных связей
- •Опыт 2. Обнаружение одноатомных спиртов (иодоформная проба)
- •Опыт 3. Обнаружение многоатомных спиртов. Получение гликолятов
- •Опыт 4. Обнаружение фенолов реакцией с хлоридом железа (III)
- •Опыт 5. Обнаружение альдегидов и кетонов
- •Опыт 6. Обнаружение карбоксильных групп
- •Содержание
- •Надежда Михайловна Колядина
- •Ольга Владимировна Ковальчукова
- •Светлана Болеславна Страшнова
- •Лидия Сергеевна Шебалдина
- •Лабораторные работы
- •Часть 2. Органическая химия
- •Тематический план 2005 г., №
- •117923, Гсп-1, Москва, ул. Орджоникидзе,3
- •117923, Гсп-1, Москва, ул. Орджоникидзе,3
Опыт 3. Получение этилена и изучение его свойств
а) Получение этилена. В сухую пробирку поместите 1 мл этанола, 3 мл концентрированной серной кислоты и несколько фарфоровых кипелок, необходимых для равномерного кипения при нагревании. Пробирку закройте пробкой с газоотводной трубкой и, чтобы жидкость не
вылилась, закрепите на штативе под углом к поверхности стола. Этилен получают нагреванием реакционной смеси по реакции:

б) Химические свойства этилена. Для изучения химических свойств этилена так же, как в опыте 1б, приготовьте две пробирки с растворами перманганата калия и бромной воды по 0,5 мл. Пробирку с газом осторожно нагрейте, конец газоотводной трубки опустите на 1-2 минуты в раствор перманганата калия, затем на такое же время - в бромную воду. Напишите уравнения реакций, отметьте, изменилась ли окраска растворов. Сделайте вывод о взаимодействии этилена с водными растворами окислителя и галогена.
Опыт 4. Горение алкенов
а) Горение этилена. Не прекращая нагревание реакционной смеси, подожгите выделяющийся этилен у конца газоотводной трубки, затем прекратите нагревание пробирки. Запишите уравнение реакции и отметьте цвет и характер пламени горящего этилена.
б) Горение циклогексена. Налейте в фарфоровую чашечку 2 мл циклогексена и подожгите. Проследите за характером пламени. Напишите уравнение горения гептана. Сравните цвет и характер пламени при горении метана и гептана. Наблюдения запишите в лабораторный журнал.
Опыт 5. Получение ацетилена и изучение его свойств
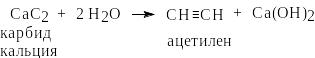
а) Получение ацетилена. В сухую колбу Вюрца поместите несколько кусочков карбида кальция. Широкое горло колбы закройте резиновой пробкой со вставленной в неё капельной воронкой. В капельную воронку при закрытом кране налейте 10-15 мл воды. На газоотводную трубку наденьте резиновый шланг со стеклянной трубочкой на конце. Ацетилен получают при взаимодействии карбида кальция с водой по реакции:
б) Химические свойства ацетилена. Для изучения химических свойств ацетилена так же, как в опыте 1б, приготовьте две пробирки с растворами перманганата калия и бромной воды по 0,5 мл. Осторожно откройте кран капельной воронки, так чтобы капли воды попадали на карбид кальция со скоростью не более 1-ой капли в секунду. Конец газоотводной трубки опустите на 1-2 минуты в раствор перманганата калия, затем на такое же время - в бромную воду. Напишите уравнения реакций, отметьте, изменилась ли окраска растворов. Сделайте вывод о взаимодействии ацетилена с водными растворами окислителя и галогена.
в) Качественные реакции алкинов. Получение ацетиленида сребра. Приготовьте в пробирке 1 мл свежего раствора гидроксида диамминсеребра (I) (реактив Толленса) и пропустите через раствор выделяющийся ацетилен. Наблюдайте выпадение осадка ацетиленида серебра. В лабораторном журнале отметьте цвет осадка и запишите уравнение реакции.
Приготовление раствора гидроксида диаммин серебра (I): к 5 каплям 1%-го раствора нитрата серебра добавьте 5 капель 10%-го раствора гидроксида натрия. К полученному бурому осадку прибавьте по каплям концентрированный раствор аммиака до полного его растворения.
б). Получение ацетиленидов меди (I). В две пробирки и налейте по 1 мл раствора комплексной соли - хлорида диаминомеди (I) [Сu(NH3)2]Cl. В первую пробирку пропустите ацетилен, а во вторую - добавьте 1 мл фенилацетилена. В лабораторном журнале отметьте цвет выпавших осадков и запишите уравнения реакций. Испытайте осадки ацетиленидов действием 2Н раствора соляной кислоты. Запишите уравнения реакций.
Сделайте обобщающий вывод о кислотных свойствах алкинов.
